врожденная невропатия лицевого нерва код по мкб 10 у детей
Невралгия тройничного нерва
14-16 октября, Алматы, «Атакент»
150 участников из 10 стран. Новинки рынка стоматологии. Цены от производителей
Общая информация
Краткое описание
Невралгия тройничного нерва (тригеминальная невралгия) – пароксизмальная колющая боль продолжительностью несколько секунд, часто вызывается вторичными чувствительными стимулами, соответствует зоне иннервации одной или нескольких ветвей тройничного нерва на одной стороне лица, без неврологического дефицита [2,4]. Основной причиной заболевания является конфликт между сосудом и корешком тройничного нерва (нейроваскулярный конфликт). В редких случаях лицевая боль вызвана другими патологическими состояниями (опухоль, сосудистые мальформации, герпетическое поражение нерва) [4].
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: нет.
Диагностические критерии [5]
Магнитно-резонансная томография головного мозга выполняется для определения этиологии тригеминальной невралгии.
Жалобы и анамнез
Жалобы:
Пароксизмальные приступы боли в области иннервации одной или нескольких ветвей тройничного нерва.
• Исключение других причин болей при обследовании;
Инструментальные исследования:
МРТ является стандартным методом для выявления нейроваскулярного конфликта в зоне тройничного нерва, и исключения другой причины (например, опухоль, сосудистая мальформация и др.) заболевания.
Показания для консультации специалистов:
Дифференциальный диагноз
Дифференциальный диагноз [13]
Дифференциальный диагноз проводится с патологическими состояниями, характеризующимися лицевой и/или краниальной болью. К таким заболеваниям (Таблица 1) относятся пульпит, темпоромандибулярная боль, нейропатическая тригеминальная боль, пароксизмальная гемикрания.
Таблица 1. Сравнение признаков тригеминальной невралгии с симптомами других заболеваний
Лечение
Цели лечения
Устранение или уменьшение боли путем микроваскулярной декомпрессии (код операции 04.41) или чрескожной радиочастотной термокоагуляции тройничного нерва (код операции 04.20). Выбор хирургического метода лечения зависит от возраста и сопутствующей патологии пациента, причины тригеминальной невралгии, характера болей, а также желания пациента [1, 7-10].
Тактика лечения
Немедикаментозное лечение:
Диета при отсутствии сопутствующей патологии – соответственно возрасту и потребностям организма.
Медикаментозное лечение [3,6,11,14]
Медикаментозное лечение, оказываемое на амбулаторном уровне
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
Карбамазепин 200 мг, доза и кратность зависят от частоты и интенсивности лицевой боли, перорально.
Перечень дополнительных лекарственных средств (менее 100% вероятности применения):
Прегабалин 50-300 мг, доза и кратность зависят от частоты и интенсивности лицевой боли, перорально.
С целью уменьшения лицевой боли до операции пациенты обычно принимают энтерально препарат Карбамазепин [12], доза и кратность приема которого зависят от интенсивности и частоты приступов лицевой боли.
Антибиотикопрофилактика: Цефазолин 2 г, внутривенно, за 1 час до разреза.
Послеоперационная анальгетическая терапия: НПВС или опиоидные средства.
Послеоперационная противорвотная терапия (метоклопрамид, ондансетрон), внутривенно или внутримышечно, по показаниям в возрастной дозировке.
Гастропротекторы в послеоперационном периоде в терапевтических дозировках по показаниям (омепразол, фамотидин).
Медикаментозное лечение, оказываемое на этапе скорой неотложной помощи: нет.
Другие виды лечения
Другие виды лечения, оказываемые на амбулаторном уровне:
Блокады точек выхода нерва.
Другие виды лечения, оказываемые на стационарном уровне: радиохирургия (Гамма нож).
Другие виды лечения, оказываемые на этапе скорой неотложной помощи: Не проводится.
Хирургическое вмешательство
Хирургическое вмешательство, оказываемое в амбулаторных условиях: Не проводится.
Хирургическое вмешательство, оказываемое в стационарных условиях
Методы хирургического лечения невралгии тройничного нерва:
Целью микроваскулярной декомпрессии является устранение конфликта между сосудом и тройничным нервом. При радиочастотной термокоагуляции выполняется селективное термическое поражение нерва, тем самым достигается прерывание проводимости болевых импульсов.
Дальнейшее ведение
Первый этап (ранний) медицинской реабилитации – оказание МР в остром и подостром периоде травмы или заболевания в стационарных условиях (отделение реанимации и интенсивной терапии или специализированное профильное отделение) с первых 12-48 часов при отсутствии противопоказаний. МР проводится специалистами МДК непосредственно у постели больного с использованием мобильного оборудования или в отделениях (кабинетах) МР стационара. Пребывание пациента на первом этапе завершается проведением оценки степени тяжести состояния пациента и нарушений БСФ МДК в соответствии с международными критериями и назначением врачом-координатором следующего этапа, объема и медицинской организации для проведения МР [15].
Последующие этапы медицинской реабилитации – темы отдельного клинического протокола.
Наблюдение невропатолога в поликлинике по месту жительства.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
Отсутствие или уменьшение интенсивности и частоты приступов лицевой боли в области иннервации тройничного нерва.
Препараты (действующие вещества), применяющиеся при лечении
Группы препаратов согласно АТХ, применяющиеся при лечении
| (N02) Анальгетики |
| (J01) Противомикробные препараты для системного применения |
Госпитализация
Показания для госпитализации
Показания для плановой госпитализации:
Руководство по ведению пациентов с острой нейропатией лицевого нерва (2020)
Fieux M, et al. French Society of ENT (SFORL) guidelines. Management of acute Bell’s palsy. European Annals ofOtorhinolaryngology, Head and Neck diseases (2020)
Введение
Паралич Белла является наиболее распространенной формой нейропатии лицевого нерва, тем
не менее, в 8–12% случаев причиной становится наличие объемного образования [1,2] (уровень
доказательности 4). Более чем в 70% случаев паралич Белла имеет благоприятный прогноз с
полным восстановлением в течение 6 месяцев [3,4] (уровень доказательности 3); практически
полного восстановления (до степени I-II по шкале Хауса-Браакмана) достигают более 80%
больных [5] (уровень доказательности 3). Таким образом, прогноз заболевания благоприятный,
однако отсутствие полного восстановления нарушает социальную адаптацию и ухудшает качество
Клиническое обследование
Паралич Белла представляет собой одну из форм нейропатии лицевого нерва, которая
характеризуется быстрым развитием (в течение 24–48 часов) слабости верхней и нижней групп
мимических мышц половины лица и вегетативных нарушений. Началу заболевания может
предшествовать боль в ухе или в заушной области, нарушение вкуса, гиперакузия. Диагноз
устанавливается путем исключения других причин. Клиническое обследование должно включать
оценку силы мимической мускулатуры, в первую очередь для подтверждения периферического
уровня поражения с подробным неврологическим и отоларингологическим обследованием [5,9, 10] (уровень доказательности 2).
Критерии периферического уровня поражения:
Подтверждение периферического уровня поражения лицевого нерва:
Оценка скорости развития симптоматики позволяет предположить возможную этиологию поражения лицевого нерва, например, объемное образование. Истинный паралич Белла развивается достаточно быстро, в отличие от нейропатии.
Чаще всего должен проводиться дифференциальный диагноз [11] (уровень доказательности 2).
Согласно рекомендациям Американской академии отоларингологии (2013), максимальное время
развития симптоматики – 72 часа [6] (уровень доказательности 1). Несмотря на то, что в 6%
случаев паралич Белла может рецидивировать [9] (уровень доказательности 2), наличие в анамнезе
пациента нейропатии лицевого нерва ставит под сомнение диагноз идиопатического паралича
Белла [12] (уровень доказательности 4).
Изолированная нейропатия лицевого нерва не должна сопровождаться ипсилатеральным
снижением слуха, в связи с чем проведение аудиометрии является обязательным для исключения
кондуктивной тугоухости, которая позволяет предположить наличие опухоли лицевого нерва в
пирамиде височной кости, или нейросенсорной тугоухости, наличие которой позволяет сделать
предположение о сдавлении лицевого нерва объемным образованием, расположенным в области
мосто-мозжечкового угла. Тимпанометрия позволяет оценить акустический рефлекс стременной
мышцы, что предоставляет дополнительную информацию для топического диагноза [13,14]
(уровень доказательности 4).
Для клинической оценки тяжести острой нейропатии лицевого нерва рекомендовано
применение классификации Хауса-Браакмана (House-Brackmann facial nerve grading system) [15],
тогда как для последующего динамического наблюдения за пациентом и оценки степени
восстановления наиболее удобна классификация Саннибрука (the Sunnybrook classification).
Лабораторное обследование
В американском (2013) и канадском (2014) руководствах по ведению пациентов с параличом
Белла [6,7] (уровень доказательности 1) не рекомендовано проведение у больных каких-либо
Нейровизуализационное обследование
Согласно американскому и канадскому руководствам по ведению пациентов с параличом
Белла [6,7] (уровень доказательности 4), проведение нейровизуализационного обследования у
пациентов с отсутствием другой очаговой неврологической симптоматики и с нормальными
показателями аудиометрии нецелесообразно. Тем не менее, в недавно опубликованных работах
сообщается, что в 8–12% случаев нейровизуализационное обследование пациентов с типичной
клинической картиной паралича Белла выявляло наличие объемных новообразований, 30% из
которых являлись злокачественными [2] (уровень доказательности 4). МРТ головного мозга с
контрастным усилением является методом выбора, поскольку позволяет детально оценить
состояние церебральных структур по ходу нерва, а также структуру околоушной слюнной железы.
Для паралича Белла характерно, но не специфично, накопление контрастного вещества лицевым
нервом на стороне клинических симптомов [20–22] (уровень доказательности 4). В случае наличия
у пациента типичной картины паралича Белла проведение экстренного нейровизуализационного
обследования нецелесообразно [23] (уровень доказательности 4), диагностика должна быть
проведена в течение 1 месяца от дебюта симптомов.
Оценка степени тяжести
Электронейромиография (ЭНМГ) является основным инструментальным методом оценки
тяжести и прогноза заболевания, однако она не должна проводиться в ранние сроки [24] (уровень
доказательности 4). Отсутствие потенциала двигательных единиц (ПДЕ) при произвольном
мышечном сокращении не имеет прогностического значения вплоть до 15 дня от дебюта
симптомов [25] (уровень доказательности 4).
В соответствии с мнением экспертов и литературными данными, на основании результатов
ЭНМГ выделяются следующие варианты нейропатии лицевого нерва при параличе Белла и ее
— миелинопатия с благоприятным прогнозом;
— сочетание миелино — и аксонопатии с относительно благоприятным прогнозом;
— тяжелая аксонопатия с неблагоприятным прогнозом [26] (уровень доказательности 4).
В случае тяжелой нейропатии лицевого нерва (V-VI степень по шкале Хауса-Браакмана) для оценки прогноза восстановления ЭНМГ следует выполнять на 9–20 день от дебюта симптомов (Мнение экспертов).
Для наибольшей прогностической ценности результатов протокол ЭНМГ должен включать:
Медикаментозное лечение
Тактика ведения пациентов с параличом Белла остается предметом обсуждений ввиду его
спонтанного благоприятного прогноза, наблюдаемого у большинства пациентов. Частота полного
восстановления нарушенных функций коррелирует с исходной тяжестью симптомов и колеблется
от 61% при тотальной прозоплегии до 94% при менее выраженной тяжести прозопареза [5]
(уровень доказательности 3). Большинство авторов подтверждают эффективность
глюкокортикоидной терапии при лечении пациентов с параличом Белла [6,7, 27,28] (уровень
доказательности 1). В исследовании Giri P. и соавт. (2015) было продемонстрировано отсутствие
различий в эффективности внутривенной и пероральной глюкокортикоидной терапии [29]
(уровень доказательности 2). Также в многоцентровых рандомизированных двойных слепых
плацебо-контролируемых исследованиях было показано отсутствие значимой эффективности
монотерапии ацикловиром или валацикловиром у пациентов с параличом Белла [31–33] (уровень
В американском и канадском руководствах по ведению пациентов с параличом Белла
рекомендовано назначение комбинированной глюкокортикоидной и противовирусной терапии на
ранних стадиях заболевания [6,7] (уровень доказательности 2). В недавно опубликованных
работах также подтверждается целесообразность назначения комбинированной терапии после
оценки противопоказаний и возможных побочных эффектов противовирусных препаратов
[34,35,36] (уровень доказательности 2).
Медикаментозное лечение синдрома Рамсея-Ханта
Синдром Рамсея-Ханта протекает тяжелее классического паралича Белла, у 50–85% пациентов
сопровождается развитием осложнений [11,37,38] (уровень доказательности 3) и характеризуется
высокой склонностью к рецидивам [11] (уровень доказательности 3).
Уход за глазами
К основным осложнениям, развивающимся у пациентов с параличом Белла и синдромом
Рамсея-Ханта, относится офтальмологическая патология в виде кератита, язв роговицы,
панофтальмии. Профилактика осложнений включает назначение пациентам систематического
использования глазных капель, защитного геля или искусственной слезы с частотой до нескольких
раз в день, особенно в ночное время [6,27,39–41] (уровень доказательности 4).
Профилактика офтальмологических осложнений паралича Белла и синдрома Рамсея-Ханта
включает раннее назначение пациентам систематического
использования местной терапии (глазных капель, защитного геля или
искусственной слезы, ночной окклюзии глаза). При выявлении признаков
воспаления глазного яблока пациент должен быть направлен к офтальмологу.
Наблюдение офтальмологом должно продолжаться в течение нескольких недель
от начала выздоровления (Мнение экспертов).
Физиотерапевтическое и реабилитационное лечение
В мета-анализе 12 исследований с участием 872 пациентов, проведенном MacIntosh P. W. и
соавт. (2019), сообщалось о высоком риске систематической ошибки ввиду значительных
различий в используемых методах восстановительного лечения, сроках его назначения и
длительности [42] (уровень доказательности 4). Тем не менее, при отсутствии полного
восстановления силы мимической мускулатуры у пациентов с параличом Белла проведение
восстановительного лечения является эффективным и обоснованным [6,43,44] (уровень
Гипербарическая оксигенация
Динамическое наблюдение
Клиническое и офтальмологическое наблюдение должно продолжаться в течение нескольких
месяцев после начала восстановления с целью профилактики и своевременного лечения
осложнений, в особенности – офтальмологических [6,7] (уровень доказательности 4).
Хирургическое лечение
Польза от проведения хирургической декомпрессии лицевого нерва в настоящее время не
доказана. Поскольку на эффективность оперативного лечения влияет множество факторов, таких
как критерии отбора пациентов, сроки и методы выполнения операции, достоверно оценить
пользу от проведения декомпрессии лицевого нерва достаточно сложно. Тем не менее,
декомпрессию лицевого нерва следует рассматривать в качестве альтернативного метода лечения,
что подтверждается результатами мета-анализа LeeS-Y. и соавт. (2019) [48] (уровень
Вопрос о хирургическом вмешательстве может рассматриваться только после постановки
достоверного диагноза паралича Белла, который основывается на комплексной оценке результатов
клинического, электромиографического и нейровизуализационного обследования.
Международный неврологический журнал 7 (45) 2011
Вернуться к номеру
Симпозиум: «Невропатия лицевого нерва и прозопарезы у детей»
Авторы: Морозова Т.М., Евтушенко С.К., Евтушенко О.С., Кафедра детской и общей неврологии ФИПО, Донецкий национальный медицинский университет им. М. Горького
Версия для печати
Проводит: кафедра детской и общей неврологии ФИПО Донецкого национального медицинского университета им. М. Горького.
Рекомендован: детским неврологам, семейным врачам.
Парез мимической мускулатуры (прозопарез) вследствие поражения лицевого нерва у детей занимает первое место в структуре заболеваний периферической нервной системы. Частота невропатии лицевого нерва (НЛН) в детском возрасте в среднем составляет 5–7 человек на 10 тыс. детей, в равной пропорции среди мальчиков и девочек.
В МКБ-10 поражение лицевого нерва (ЛН) представлено кодом G51. В настоящее время идиопатическое поражение ЛН трактуется как паралич Белла, по имени С. Bell, который в 1836 г. впервые описал клинику поражения ЛН (шифр МКБ — G51.0). Паралич Белла составляет от 50 до 75 % всех НЛН. Термин «невропатия/неврит лицевого нерва» используется для обозначения других форм с известной или неуточненной этиологией (шифр МКБ: G51.8 — Другие поражения лицевого нерва и G51.9 — Поражение лицевого нерва неуточненное). Собственный шифр имеют НЛН при воспалении узла коленца (G51.1) и синдроме Мелькерссона — Россолимо (G51.2). Таким образом, идиопатический паралич Белла является диагнозом исключения. Все остальные этиологические факторы прозопареза, в том числе травматические, инфекционные, врожденные, метаболические, иммунологические, аутоиммунные, неопластические, должны быть исключены.
Существует несколько анатомических особенностей, способствующих поражению ЛН: 1) филогенетически нерв является одним из наиболее молодых и ранимых черепных нервов; 2) нерв имеет сложный ход в узком костном канале, занимая 70 % поперечника; 3) магистральные сосуды в условиях узкого костного ложа ведут себя подобно конечным, что способствует первичной и вторичной ишемии.
В последнее время клиницисты склоняются к тому, что НЛН полиэтиологическое, но монопатогенетическое заболевание. Несмотря на множество теорий относительно патогенеза НЛН (ишемическая, сосудистая, воспалительная, токсическая, иммунная, вирусная), паралич Белла в настоящее время рассматривается как туннельный синдром, обусловленный компрессией ишемизированного и отечного нерва в узком фаллопиевом канале. Условия для компрессии лицевого нерва наиболее благоприятны в его нижнем отделе, где на уровне шилососцевидного отверстия эпиневральная оболочка утолщена и очень упруга.
Непосредственным пусковым механизмом в развитии сосудистых нарушений и ишемии нерва могут послужить: переохлаждение, инфекции, аутоиммунные заболевания, гормональные и метаболические расстройства, болевой фактор. В формирующемся патобиохимическом комплексе важное место занимает дезинтеграция метаболизма, активация перекисного окисления липидов, повышение проницаемости мембран для ионов калия, угнетение антиоксидантных систем, развитие миелино- и аксонопатии ЛН и нарушение нервно-мышечной передачи.
Патоморфологически повреждение нерва классифицируется по Sunderland. Существует пять степеней тяжести от нейропраксии (утрата миелина) и аксонотемезиса до тяжелого нейротемезиса с валлеровским перерождением и утратой пери- и эпиневрия. Степень повреждения ЛН коррелирует с выраженностью клиники и неблагоприятным прогнозом восстановления функции.
У детей НЛН развивается на фоне интенсивных процессов роста и миелинизации нервных волокон, что обусловливает особенности течения и прогноз. С одной стороны, детский возраст является прогностически благоприятным в восстановлении функции ЛН. С другой — в 10–20 % случаев в процесс вовлекается тройничный и ЛН на здоровой стороне, у 60 % детей при исследовании зрительных вызванных потенциалов выявляются признаки билатерального нарушения проводимости по зрительному нерву. Эти данные предопределяют риск развития рецидивирующей НЛН и иногда позволяют считать эту патологию вариантом краниальной демиелинизирующей полиневропатии или клинически изолированным синдромом в дебюте рассеянного склероза.
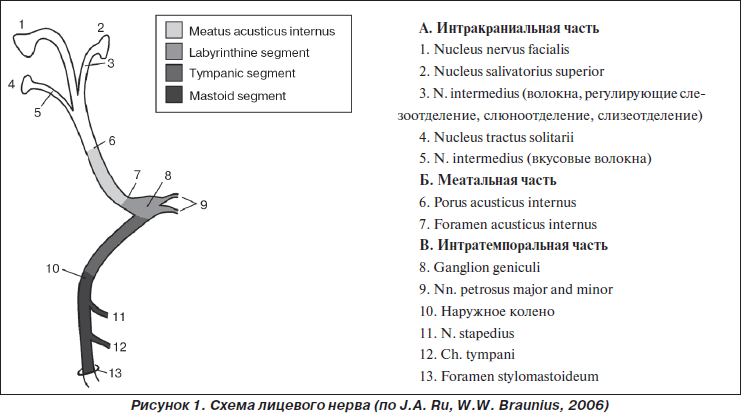
Клинические симптомы при поражении ЛН будут складываться из прозопареза и сопутствующих ему симптомов-спутников, которые определяются топическим уровнем повреждения. Выделяют следующие уровни поражения ЛН:
— супрануклеарные повреждения (центральный паралич ЛН);
— поражение на уровне ядра (процессы в области варолиева моста);
— повреждения корешка ЛН в области задней черепной ямки (мосто-мозжечковый угол);
— повреждения корешка ЛН у входа в канал височной кости;
— повреждения ЛН в фаллопиевом канале проксимальнее отхождения n. petrosus superficialis major (к слезной железе);
— повреждения ЛН в фаллопиевом канале проксимальнее отхождения ветви к m. stapedius;
— повреждения ЛН в фаллопиевом канале между n. stapedius и chorda tympani;
— повреждения ЛН в фаллопиевом канале дистальнее отхождения chorda tympani;
— повреждения ЛН дистальнее foramen stylomasto-ideum.
Схема ЛН от ствола через внутреннее слуховое отверстие и фаллопиев канал (лабиринтный, барабанный и сосцевидный сегменты) к шилососцевидному отверстию представлена на рис. 1.
По данным МР-визуализации с гадолинием выявлено вовлечение ЛН на уровне супрагеникулярного сегмента — 47 %, геникулярного сегмента — 25 %, тимпанической части — 2 %, мастоидальной части — 15 %. В 11 % уровень поражения локализовать не удалось.
Клиническая картина
Заболевание развивается остро, в течение нескольких часов (реже — 3–10 дней). Медленное нарастание прозопареза (в течение недель или месяцев) нехарактерно и в большинстве случаев имеет неопластическую этиологию. Развитию заболевания часто предшествует общее или локальное переохлаждение. Приблизительно в 60 % случаев парез Белла начинается с ноющей или жгучей боли за ухом, которая иногда может иррадиировать в лицо или затылок. Обычно слабость лицевых мышц выявляется утром при пробуждении. Общее самочувствие остается нормальным.
В покое в остром периоде заболевания отмечается сглаженность складок на лбу, расширение глазной щели, опущение брови, нижнего века, крыла носа, угла рта. В результате паралича ушных мышц ушная раковина немного развернута кпереди. Глазная щель полностью не смыкается во время сна, нижнее веко слегка отходит от слизистой глазного яблока, моргание отсутствует или становится редким. При попытке закрыть глаза наблюдается симптом Белла, который заключается в синергическом с закрыванием глаз движением глазного яблока вверх и немного кнаружи. При взгляде вверх наблюдается симптом Негро: глаз на больной стороне как бы поднимается выше, чем на здоровой, и образуется более широкая полоса склеры между роговицей и нижним веком. Следствием поражения круговой мышцы глаза является не только лагофтальм, но и слезотечение, которое объясняется раздражением постоянно открытого глаза, а также тем, что слеза не попадает в носослезный канал. Слезотечение присутствует у 2/3 больных, реже (17 %) возникает сухость глаза, вследствие поражения волокон большого каменистого нерва. Около 30 % больных отмечают искаженное, неприятно усиленное восприятие звуков (гиперакузию) с больной стороны, связанное с парезом стременной мышцы. Во многих случаях нарушается вкусовосприятие на передних 2/3 языка (дисгевзия). Активные движения на стороне поражения отсутствуют или значительно ограничены. При их проверке необходимо обратить внимание на наморщивание лба (функция лобной мышцы), нахмуривание бровей (т.н. мышца гордецов), закрывание и зажмуривание глаза (круговая мышца глаза), наморщивание спинки носа (носовая мышца), движения угла рта при сомкнутых губах и оскал зубов (мышцы, поднимающие и опускающие угол рта), движение губ кпереди (круговая мышца рта). При надувании щек на стороне пареза гипотоничная щечная мышца парусит, а при недостаточном смыкании губ надувание щек становится невозможно, иногда пища выпадает изо рта. При незначительном парезе круговой мышцы глаза наблюдается симптом ресниц, который состоит в том, что больной может закрыть глаза, но при попытке их сильно зажмурить видны кончики ресниц на пораженной стороне.
Выделяют следующие степени тяжести НЛН:
1) легкая — прозопарез, слезотечение;
2) среднетяжелая — прозопарез, дисгевзия, гиперакузия, сухость глаза, боль;
3) тяжелая — прозоплегия и другие симптомы-спутники.
Регресс симптомов, вплоть до полного восстановления, при благоприятном развитии происходит в течение 4–6 недель. В других случаях улучшение наступает спустя 3–6 месяцев и бывает лишь частичным. Благоприятный исход отмечается примерно в 80 % случаев, значительные остаточные явления — в 5–8 % случаев. Рецидивирующее течение наблюдается в 7–9 % случаев.
Неблагоприятными прогностическими факторами НЛН являются:
— тяжелая степень прозопареза;
— высокий уровень поражения (гиперакузия, нарушение слезо- и слюноотделения, дисгевзия);
— избыточные фациальные дисморфии;
— рецидивы прозопареза и семейная предрасположенность;
— позднее начало терапии (после 3 дней);
— отсутствие акустического стапедиального рефлекса;
— электрофизиологические признаки денервации.
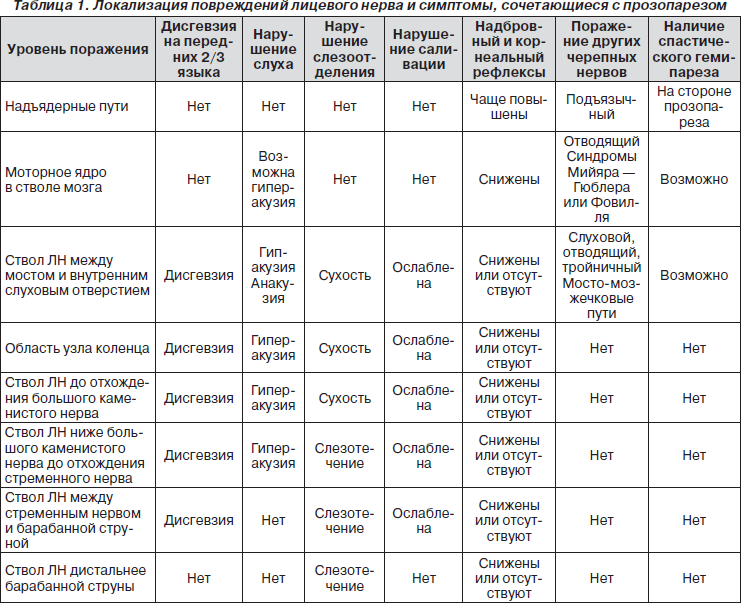
Локализация повреждений лицевого нерва и симптомы-спутники прозопареза представлены в табл. 1.
Одним из главных прогностических критериев осложнений при НЛН является тяжесть и длительность паралича мимической мускулатуры. Если в течение четырех и более недель не началось спонтанного или индуцированного лечением восстановления или оно крайне незначительно, то вероятность развития контрактур или синкинезий очень велика и составляет 28–37 %.
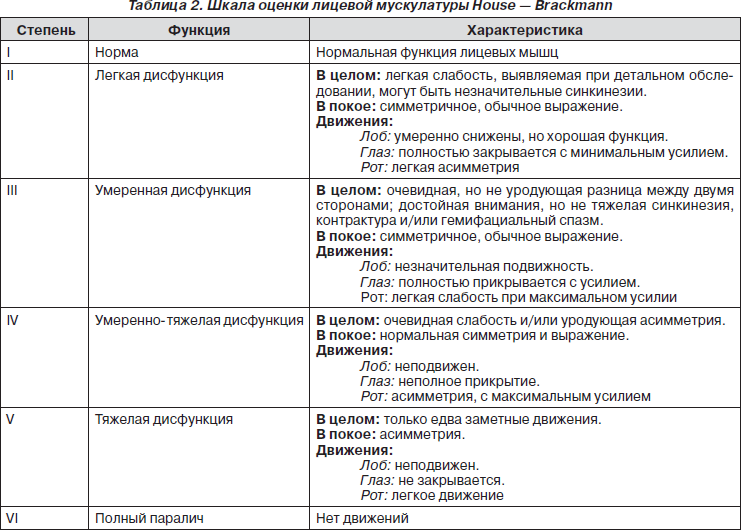
Степень выраженности прозопареза определяется шкалой House — Brackmann (табл. 2).
Контрактура мимических мышц в начальном периоде по своим клиническим признакам лишь количественно отличается от триггерной стадии НЛН. Триггер, с одной стороны, способствует повышению тонуса паретичных мышц, с другой — служит предпосылкой для формирования контрактур. Их первым симптомом является наличие легкой спонтанной боли в лице. Однако в отличие от тех болей, которые нередко наблюдаются в первые дни заболевания, сами мышцы также оказываются болезненными при пальпации. Пациент отмечает незаметные на глаз пульсирующие подергивания отдельных мышечных пучков, ощущение стягивания на пораженной половине лица. Эти пульсации легко определяются приложенным пальцем. Чаще контрактура возникает на фоне неполного восстановления паралича Белла. В далеко зашедших случаях при осмотре больного создается впечатление, что парализованной является не больная, а здоровая сторона. Обнаруживаются следующие признаки контрактуры: глазная щель становится уже; носогубная складка в покое выражена отчетливее; наблюдаются спонтанные гиперкинезы в виде мелких фасцикулярных подергиваний подбородка или век. Механическая возбудимость мимических мышц резко повышается. Ощущение стягивания на пораженной половине лица усиливается, особенно при волнении, на холоде, при физических и умственных нагрузках. Во время массажа отчетливо ощущается, что щека толще, чем на здоровой стороне. При сформировавшейся контрактуре триггерные пункты можно найти в любой мимической мышце. Они прощупываются в виде уплотнений, болезненных при давлении и растяжении.
В процессе реиннервации мышц может появиться и другой крайне нежелательный феномен — патологические синкинезии:
— веко-губная (при закрывании глаза поднимается угол рта на той же стороне);
— веко-лобная (при закрывании глаза наморщивается лоб);
— веко-платизмовая (при зажмуривании глаза сокращается подкожная мышца шеи);
— веко-ушная (при зажмуривании непроизвольно приподнимается ушная раковина);
— синкинезия Гюйе (при зажмуривании крыло носа приподнимается вверх и кнаружи);
— губно-пальпебральная (сужение глазной щели при раздувании щек, при вытягивании губ в трубочку, во время еды);
— лобно-губная (непроизвольное приподнимание угла рта при наморщивании лба);
— симптом крокодиловых слез (слезотечение из глаза на пораженной стороне при жевании или даже при перемещениях нижней челюсти). Этот феномен является образцом патологической моторно-висцеральной синкинезии.
Диагностика
Особое внимание уделяется анамнезу заболевания, быстроте нарастания прозопареза, клинической симптоматики и выявлению симптомов-спутников. Выясняются провоцирующие факторы, предшествующие травмы, соматические и неврологические заболевания, отологическая патология.
Достоверным и значимым методом является электронейромиография (ЭНМГ). Стимуляционная и игольчатая ЭНМГ позволяет оценить динамику течения заболевания, определить стадию и степень денервационного процесса в мимических мышцах, а также оценить эффективность реиннервации. Если величина М-ответа на больной стороне составляет 30 % и более от таковой на здоровой, вероятность полного восстановления составляет 84 %; напротив, если она менее 30 %, то в 88 % случаев восстановление будет неполным. Наиболее точным методом исследования вкуса является электрогустометрия. Если исследуемый не ощущает при 300 мкА кислого или металлического привкуса, то это указывает на наличие у него нарушения вкусовой чувствительности.
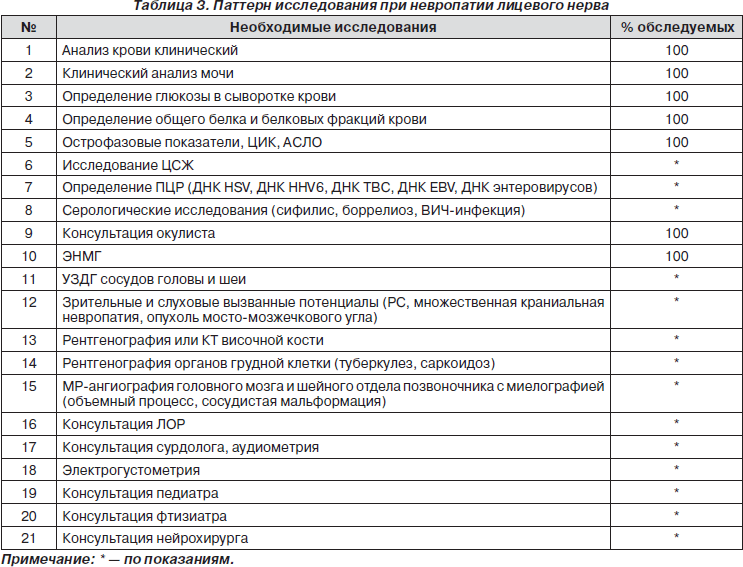
Диагностический алгоритм включает следующие лабораторные и инструментальные исследования и консультации специалистов (табл. 3).
Дифференциальная диагностика прозопареза
Унилатеральный прозопарез:
1. Идиопатический паралич Белла.
2. Семейные формы НЛН.
3. Синдром Мелькерссона — Россолимо — Розенталя (СМРР): аутосомно-доминантный тип; 9р11 с неполной пенетрантностью гена. Характеризуется рецидивирующей НЛН, рецидивирующими характерными отеками лица, губ и других частей тела, хейлитом и складчатым языком. Прозоплегия бывает односторонней и двусторонней; сторона поражения может чередоваться от рецидива к рецидиву. Встречаются больные с различными вариантами неполного СМРР. Для диагностики СМРР у детей пpедлагается использование алгоpитма, включающего: составляющие триады классического симптомокомплекса, сочетающиеся с фациальными дисмоpфиями, признаками невpологического дефицита, вегетативными и соматическими наpушениями, аутоаллеpгическими пpоявлениями и геpедитаpной пpедуготованностью.
4. Инфекционные поражения: Herpes simplex — самая частая причина; боррелиоз, ВИЧ-инфекция; полиомиелит; сифилис и туберкулез; саркоидоз и другие гранулематозные заболевания; болезнь кошачьих царапин и др. Синдром Рамзая Ханта — герпетическое поражение ганглия промежуточного нерва (боль и характерные кожные высыпания в области уха, слизистой полости рта, иногда с вовлечением VIII нерва).
5. Заболевания среднего уха: отиты и (реже) опухоли среднего уха, такие как гломусная опухоль. НЛН вследствие этих заболеваний всегда сопровождается потерей слуха и соответствующими рентгенологическими находками.
6. Рассеянный склероз, клинический изолированный синдром.
7. Дисметаболические нарушения описаны в виде мононейропатии, или картины полинейропатии, или множественной мононевропатии при сахарном диабете, гипотиреозе, уремии, порфирии, артериальной гипертензии.
8. Травмы: перелом и проникающие ранения пирамиды височной кости, ятрогенные повреждения, родовые травмы. ЧМТ, особенно при переломе пирамиды височной кости, часто приводит к поражению лицевого и вестибулокохлеарного нервов.
9. Неопластические и объемные процессы (доброкачественные и злокачественные): невринома, гемангиома, холестеатома, менингиома, метастазы, опухоль слюнной железы, арахноидальная киста.
10. Альтернирующие синдромы (при сосудистых и опухолевых поражениях ствола головного мозга).
12. Заболевания костей черепа.
13. Врожденные синдромы: синдром Мебиуса, кардиофациальный синдром, болезнь мотонейрона, остеопетроз, окулоаурикуловертебральный синдром, CHARGE синдром (колобома, порок сердца, атрезия хоан, генитальная гипоплазия, аурикулярная аномалия), CULLP-синдром (врожденный унилатеральный парез нижней губы).
Синдром Mцbius (СМ) обусловлен врожденной мальформацией ромбовидного мозга и встречается в трех генетических вариантах. Общая характеристика СМ: прозопарез может быть унилатеральным и билатеральным в 90 %. В некоторых случаях возможна наружная офтальмоплегия, чаще вовлекается отводящий нерв. В 9 % может быть врожденный фиброз экстраокулярных мышц. В 34 % ретракционный синдром Duane. В 56 % фарингеальная дисфункция и вовлечение подъязычного нерва. Респираторные нарушения в 19 %. С рождения в 88 % случаев наблюдается мышечная гипотония и в 83 % — нарушение координации.
СМ 1-й тип, доминантный, 13q12.2-q13. Клинические особенности: врожденная асимметричная диплегия лицевой мускулатуры, офтальмоплегия, орофациальные аномалии, когнитивная задержка, периферическая невропатия, артрогрипоз, дефект ребер, респираторные нарушения, кальцификаты в стволе мозга, гипогонадотропный гипогонадизм. Аплазия ядер ствола.
СМ 2-й тип, доминантный, 3q21-q22. Асимметричная слабость лицевой мускулатуры, неравномерное вовлечение ветвей ЛН, отсутствие офтальмоплегии. Ядро ЛН редуцировано, уменьшен в размере лицевой нерв. Структуры ромбовидной ямки и кортикоспинальный тракт не нарушены.
СМ 3-й тип, доминантный, 10q21.3-q22. Унилатеральный или билатеральный прозопарез, офтальмоплегия, врожденная глухота или прогрессирующая тугоухость с возрастом.
Кардиофациальный синдром (синдром Cayler — Di George, делеция 22q11.2, доминантный или мультифакториальный). Врожденный полный прозопарез или парез нижней губы в легком случае, порок сердца, мышечная гипотония, миопатия, фациальная дисморфия, гипоплазия тимуса, аномалии Т-клеток, в 10 % микроцефалия, когнитивные нарушения.
Синдром Carey — Fineman-Ziter, А-Р. Клинически непрогрессирующая миопатия, гипотония. Гипоплазия грудных и плечевых мышц (вариант Poland). Макроцефалия, офтальмоплегия, птоз, билатеральная лицевая слабость, дисфагия, микрогнатия, глоссоптоз, ращепленное небо (50 %), сколиоз (40 %), плоскостопие (40 %), брахидактилия (70 %), задержка моторного развития.
Двусторонняя слабость мимических мышц у детей, развившаяся одновременно или последовательно, встречаясь в 0,3–2 % от всех прозопарезов, всегда служит поводом для следующего диагностического поиска:
1. Острая воспалительная демиелинизирующая полиневропатия (варианты Гийена — Барре и Миллера Фишера).
2. Идиопатическая краниальная полиневропатия.
3. Хроническая воспалительная демиелинизирующая полиневропатия.
4. Синдром Мелькерссона — Россолимо — Розенталя.
5. Рассеянный склероз.
6. Hyperostosis cranialis interna: аутосомно-доминантное наследственное заболевание, которое проявляется утолщением внутренней костной пластинки черепа с остеосклерозом и туннельными краниальными невропатиями с вариабельными нарушениеми обоняния, вкуса, зрения, кохлеовестибулярной дисфункцией.
7. Саркоидоз (синдром Хеерфорда) — инфильтрация околоушных желез, иридоциклит, поражение лимфоузлов, кожи, органов дыхания, печени, селезенки, костей, лихорадка (увеопаротидный синдром) базальный процесс (туберкулезный, лейкемический, криптококковый, паранеопластический и др.), всегда вовлекаются другие черепные нервы; парезы часто двусторонние, характеризуются быстрым началом.
8. Инфекционное поражение краниальных нервов (мононуклеоз, герпетическая инфекция, боррелиоз, ВИЧ-инфекция).
9. Системные заболевания (узелковый периартериит, гранулематоз Вегенера, болезнь Кавасаки и др.) приводят к мононейропатиям и полинейропатиям, а также к поражению других краниальных нервов.
12. Ан-a-липопротеинемия (болезнь Tанжера 9q31) — кроме дипареза лицевой мускулатуры, наблюдаются слабость, снижение мышечной силы и сухожильных рефлексов, парестезии, чрезмерная потливость, глазодвигательные нарушения и избирательная потеря болевой и температурной чувствительности. Отложения эфиров холестерина в корнеальной оболочке, миндалинах, печени, селезенке, слизистой прямой кишки обусловливают сплено- и гепатомегалию, лимфаденопатию, миндалины увеличены, оранжевого или желтого цвета. В крови высокий уровень триглицеридов; гипохолестеринемия.
13. Болезнь мотонейрона.
Рецидивирующая слабость мимических мышц
1. Идиопатическая нейропатия лицевого нерва (в том числе семейная).
2. Синдром Мелькерссона — Россолимо — Розенталя.
Терапевтическая тактика НЛН зависит от этиологии и периода заболевания: 1) острый (до 10 дней, чаще 3–72 часа); 2) ранний восстановительный (10–30 дней); 3) поздний восстановительный (1 мес.); 4) период остаточных явлений (более 6 мес.) — синкинезии, слабость лицевой мускулатуры, контрактуры, блефароспазм, симптом крокодиловых слез (синдром Фрея).
Основная цель лечебных мероприятий в острый период направлена на купирование отека, улучшение микроциркуляции, ремиелинизацию.
С целью профилактики развития кератита необходимо закапывание увлажняющих глазных капель, ношение защитных очков в дневное время и наложение повязки на глаз на ночь. Эти мероприятия проводят до тех пор, пока не станет возможным произвольное закрытие глаза и не восстановится мигательный рефлекс.
Лечение идиопатического паралича Белла. При наличии одного из клинически неблагоприятных прогностических факторов показана глюкокортикоидная терапия (преднизолон 1 мг/кг/сут в течение 7–10 дней).
В других случаях используют нестероидные ПВС в течение 2 недель.
Низкомолекулярные декстраны и дегидратирующие препараты (лазикс, L-лизина эсцинат) в остром периоде вводятся парентерально и сочетаются с вазоактивными (трентал, актовегин), нейрометаболическими препаратами (альфа-липоевая кислота (эспалипон, берлитион, тиогамма), нуклео-ЦМФ и витаминами В1, В2, В12.
Антибиотикотерапия назначается при отогенных поражениях ЛН, болезни Лайма (цефуроксим или амоксициллин 50 мг/кг/сут).
Ацикловир 80 мг/кг/сут в течение 5 дней назначают при заболевании герпетической этиологии, синдроме Рамзая Ханта.
Эффективность физиотерапевтических методов лечения, электростимуляции и рефлексотерапии не доказана. Традиционно с первого дня заболевания используется электрическое поле УВЧ, обладающее выраженным противовоспалительным, обезболивающим и дегидратирующим действием, курс лечения 8–10 процедур или фонофорез с гидрокортизоном. Принципы кинезиотерапевтической реабилитации при парезах мимической мускулатуры включают лечение положением, лечебную гимнастику и массаж. Массаж показан с 3-го дня от начала прозопареза. Существуют сведения о том, что упражнения с использованием биологической обратной связи приводят к улучшению функционального исхода и снижению частоты синкинезий.
Назначение антихолинэстеразных препаратов, в том числе и при использовании электрофореза, приводит в 60–75 % случаев к развитию вторичных контрактур мимической мускулатуры и спазмопарезам.
В случае формирования ранней или поздней вторичной контрактуры мимических мышц показана отмена медикаментозных и физиотерапевтических стимулирующих методик. Используются миорелаксанты (мидокалма или сирдалуда) в комбинации с транквилизаторами или карбамазепином в дозе 10 мг/кг/сут, магне В6. Применяются препараты ботулотоксина (ботокс или диспорт). Из тепловых процедур назначаются грязевые или парафиновые аппликации на пораженную половину лица температурой 38–40 °С, длительностью 20 мин.
Методом выбора кинезиологической терапии является постизометрическая релаксация мышц (ПИРМ). Сущность этой техники заключается в чередовании кратковременной изометрической работы в первые 5–7 с и пассивного растяжения мышц в последующие 6–10 с.
Консультация детского нейрохирурга показана с целью декомпрессии нерва или при его травматическом повреждении. В случаях сохранения выраженных асимметрий и двигательных дефектов (лагофтальм, свисающая нижняя губа и т.д.) показано направление больного на консультацию к нейрохирургу или пластическому хирургу с целью ревизии лицевого нерва или пластических операций.
1. Евтушенко С.К., Морозова Т.М., Прохорова Л.М. Рецидивирующая семейная невропатия лицевого нерва у девочки 9 лет // Междунар. неврол. журнал. — 2010. — № 3(33). — С. 58-60.
2. Морозова О.Г., Здыбский В.И., Ярошевский А.А. Опыт лечения невропатии лицевого нерва с применением препарата актовегин драже // Междунар. неврол. журнал. — 2008. — № 2(18). — С. 123-127.
3. Пітик М.І. Невропатія лицьового нерва: особливості патогенезу, діагностики й лікування в дітей та підлітків // Междунар. неврол. журнал. — 2009. — № 1(23). — С. 85-90.
4. Сучасна діагностика і лікування в неврології та психіатрії / За ред. Т.С. Міщенко та В.С. Підкоритова // Довідник лікаря «Невролог • Психіатр» — К.: ТОВ «Доктор Медіа», 2008. — С. 128-131.
5. Tanaka M., Mochizuki M., Sugiyama N., Hamano S. Bell’s palsy in children: analysis of clinical findings and course // No To Hattatsu. — 2004 Nov. — 36 (6). — 461-5.
6. Gilden D.H. Clinical practice. Bell’s Palsy // N. Engl. J. Med. — 2004 Sep. — 23. — 351(13). — 1323-31.
7. Holland N.J., Weiner G.M. Recent developments in Bell’s palsy // BMJ. — 2004 Sep. 4. — 329(7465). — 553-7.
8. Cockerham K.P., Hidayat A.A. et al. Melkersson-Rosenthal syndrome: new clinicopathologic findings in 4 cases // Arch. Ophthal. — 2000. — 118. — 227-232.
9. Linder T., Bossart W., Bodmer D. Bell’s palsy and Herpes simplex virus: fact or mystery? // Otol. Neurotol. — 2005 Jan. — 26(1). — 109-13.
10. Tiemstra J.D., Khatkhate N. Bell’s palsy: diagnosis and management // Am. Fam. Physician. — 2007, Oct. 1. — 76(7). — 997-1002.
11. Salinas R.A., Alvarez G., Ferreira J. Corticosteroids for Bell’s palsy (idiopathic facial paralysis) // Cochrane Database Syst. Rev. — 2004. — 4. — CD001942.
12. Ikeda M., Abiko Y., Kukimoto N., Omori H., Nakazato H., Ikeda K. Clinical factors that influence the prognosis of facial nerve paralysis and the magnitudes of influence // Laryngoscope. — 2005. — 115. — 855-860.
13. Allen D., Dunn L. Acyclovir or valaciclovir for Bell’s palsy (idiopathic facial paralysis) // Cochrane Database of Systematic Reviews. — 2004, Issue 3. Art. No.: CD001869.
14. Aramimed M., Valls-Sole J., Cruccu G., Ongerboer de Visseret B.W. Disorders of the Cranial Nerves // Neuromuscular Function and Disease: Basic, Clinical, and Electrodiagnostic Aspects / Ed. by W.F. Brown, C.F. Bolton, M.J. Aminoff. — Philadelphia: W.B. Saunders Company, 2002. — Vol. 1. — Р. 761.
15. Vargish L., Schumann S.A. For Bell’s palsy, start steroids early; no need for an antiviral // J. Fam. Practice. — 2008. — 57. — 22-25.
16. Seok J.I., Lee D.K., Kim K.J. The usefulness of clinical findings in localizing lesions in Bell’s palsy: comparison with MRI // J. Neurol. Neurosurg. Psychiatry. — 2008. — 79. — 418-420.
17. Bagger-Sjoback D., Remahl S., Ericsson M. Long-term outcome of facial palsy in neuroborreliosis // Otol. Neurotol. — 2005. — 26. — 790-795.
18. De Ru J.A., Braunius W.W., Van Benthem P.P., Busschers W.B., Hordijk G.J. Grading facial nerve function: why a new grading system, the MoReSS, should be proposed // Otol. Neurotol. — 2006. — 27. — 1030-1036.
19. Hato N., Yamada H., Kohno H., Matsumoto S., Honda N., Gyo K., Fukuda S., Furuta Y., Ohtani F., Aizawa H., Aoyagi M., Inamura H., Nakashima T., Nakata S., Murakami S., Kiguchi J., Yamano K., Takeda T., Hamada M., Yamakawa K. Valacyclovir and prednisolone treatment for Bell’s palsy: a multicenter, randomized, placebo-controlled study // Otol. Neurotol. — 2007. — 28. — 408-413.
20. Ushino M., Kondo K., Takeuchi N., Tojima H., Yamaguchi T., Kaga K. Prediction of the prognosis of Bell’s palsy using multivariate analyses // Otol. Neurotol. — 2007. — 29. — 69-72.