клетки каких органов могут стать мишенями на начальном этапе проникновения sars cov 2
Профессор назвал главные мишени коронавируса в организме
Исследователи из Массачусетского института и Гарварда вместе с зарубежными коллегами выяснили, что легкие, кишечник и полость носа являются основными мишенями для SARS-CoV-19. Это происходит из-за присутствия в органах большого количества клеток, наиболее восприимчивых к коронавирусной инфекции.
По словам научного сотрудника Института медицинской инженерии и науки Массачусетского технологического института (IMES) Алекса Шалека, сейчас важно как можно быстрее донести полученную в ходе работы информацию до ученых и медиков, которые трудятся над разработкой и поиском препаратов, способных воздействовать на COVID-19.
Сообщается, что исследователи использовали данные о РНК, найденные в различных типах клеток. Благодаря этому удалось обнаружить клетки, которые экспрессируют два белка, помогающие SARS-CoV-19 внедряться в человеческий организм.
Специалисты выяснили, что в носовой полости для заражения вирус использует секреторные клетки, ответственные за производство слизи. В легких это пневмоциты типа II, выстилающие альвеолы. А в кишечнике это энтероциты, отвечающие за абсорбцию питательных веществ.
Иммунный ответ на коронавирус SARS-CoV‑2 у больных COVID‑19
Академик Российской академии наук, д.м. н., президент
ФБГУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
В статье представлен анализ результатов исследований иммунного ответа и памяти к SARS-CoV‑2, включая все ветви адаптивного иммунитета, иммуноглобулины, В-клетки памяти, CD8+- и CD4+-T-клетки у больных в динамике в течение 6–8 месяцев после начала заболевания.
Гуморальное звено
Факт первичного иммунного ответа слизистых на COVID‑19 необычен и требует объяснения. Обсуждаются две гипотезы.
Первая: вирусы контаминируют слизистые дыхательных путей и ЖКТ за 7–14 дней до появления системного ответа и клинических проявлений инфекции, поражая клетки микробиоты — используют их для репродукции вируса.
Вторая: кросс-реактивная продукция антител, предпосылкой которой являются Spike-реактивные CD4+-Т-клетки, обнаруженные у большинства пациентов с COVID‑19 и более чем у 34 % неинфицированных людей. Это подтверждает существование общих эпитопов эндемичных коронавирусов, вызывающих банальные ОРВИ и COVID‑19.
Важно, что изотипы иммуноглобулинов (либо IgG, либо IgA) конкурировали за нейтрализующую активность по отношению к SARS-CoV‑2 в зависимости от локализации. Сывороточные антитела IgG сильно коррелировали с величиной IgG-ответа и тяжестью заболевания. У пациентов, например, с IgA-назальным ответом определялась высокая активность нейтрализации вирусов. Инфекция у таких больных протекала бессимптомно.
Это, с одной стороны, предполагает возможность нейтрализации вируса с помощью IgA слизистых без системного ответа, что имеет отношение к исходам заболевания. А с другой стороны, из-за множества корреляций, наблюдаемых между типами антител и их активностью в разных анатомических участках, клиническая интерпретация гуморального ответа существенно затруднена.
Кроме того, эти данные имеют важное значение для нашего понимания защиты вакцинации, индуцирующей системный ответ на вакцинные гены или белки коронавируса по классическому пути и обеспечивающей иммунный ответ слизистых оболочек на 3–6‑й неделе после вакцинации. В идеале вакцина должна не только защитить реципиента от неизбежной болезни, но и предотвратить бессимптомное носительство, что закрыло бы проблему бессимптомных носителей в популяции.
Титры Spike IgА и RBD IgА сохранялись на стабильном уровне на протяжении всего периода наблюдения t1/2— 210 дней, но у отдельных пациентов уровень специфических IgА-антител достоверно снижался через 90 дней.
Нельзя дать однозначный ответ в отношении серонегативных случаев COVID‑19. По-видимому, кроме протективного эффекта иммунитета слизистых, ответ напрямую связан с уровнем вирусной нагрузки SARS-CoV‑2. С одной стороны, высокие вирусные нагрузки связаны с более ранним ответом антител, в то время как у пациентов с низкой вирусной нагрузкой не может быть сероконверсии. С другой стороны, кинетика иммунного ответа может быть показателем скорости элиминации вируса у больного.
Идентификация специфичных В-клеток памяти к Spike, RBD и NCP с использованием флюоресцентно окрашенных зондов на IgD– и (или) CD27+ c последующей дифференцировкой по изотипам поверхностных IgM, IgG или IgA показала следующее. Количество специфических В-клеток увеличивалось в течение 120 дней после начала заболевания с последующим выходом на плато, в то время как Spike-специфические В-клетки памяти у людей, не заболевших COVID‑19, практически не встречались. RBD-специфические В-клетки появлялись на 16‑й день, и их количество увеличивалось в течение последующих 4–5 месяцев. Интересно, что только 10–30 % Spike-специфических В-клеток памяти было специфично для домена RBD через 6 месяцев после выздоровления больных.
NCP-специфичные В-клетки памяти также стабильно увеличивались в те же сроки и определялись спустя 5–6 месяцев после заболевания. Представленность изотипов иммуноглобулинов Spike-специфических В-клеток имела следующую динамику. В ранней фазе (20–60 дней) после заболевания IgM+ и IgG+ на В-клетках были представлены одинаково. В период после 60 дней до 240‑х суток преобладали IgG+ Spike-специфические В-клетки. Частота IgА+ Spike-специфических клеток составляла примерно 5 %, и они равномерно распределялись в течение всего периода наблюдения в 8 месяцев. Корреляция между сывороточным IgA и IgA слизистых оболочек не проводилась.
Сходная картина динамики наблюдалась и в случае IgG+, IgM+ и IgА+ к эпитопам RBD и NCP коронавируса. В то же время долгосрочное присутствие циркулирующих В-клеток памяти, направленных как против основных SARS-CoV‑2‑нейтрализующих таргетов (Spike и RBD), так и против не нейтрализующего таргета (NCP), свидетельствует о клеточной памяти, сохраняющейся после естественного воздействия вируса. Это может быть использовано для планирования ревакцинации. Тот факт, что почти все RBD- специфические IgG+-В-клетки памяти экспрессировали CD27, свидетельствует о долгосрочной иммунной памяти.
Анализ полученных данных говорит о том, что снижение нейтрализующих и других антител к SARS-CoV‑2 после клинического выздоровления вовсе мунитета. Просто с развитием и сохра- нением памяти В-клеток, способных активизироваться при встрече с новыми штаммами коронавируса, уровень антител в сыворотке снижается, в то время как IgА-ответ слизистых сохраняется на постоянном уровне в течении всего периода наблюдения.
Клеточный ответ
Процент больных с обнаруживаемыми циркулирующими CD8+-Т-клетками памяти через месяц после возникновения симптомов составил 70 %. К 6–9 месяцам клетки обнаруживались у 50 % выздоровевших пациентов. Фенотипические маркеры показали, что большинство SARS-CoV‑2‑специфичных CD8+-Т-клеток представлены терминально дифференцированными клетками памяти.
Циркулирующие SARS-CoV‑2‑специфичные CD4+-Т-клетки памяти через месяц после начала заболевания обнаруживались у 93 % пациентов. Через 6–9 месяцев уровень этих клеток был стабильным, а сами они выявлялись у более чем у 90 % пациентов, перенесших COVID‑19. Причем это касалось как Spike-специфичных, так и мембраноспецифичных CD4+-Т-клеток памяти.
Интересно, что при сравнении параметров иммунного ответа у больных с тяжелым и легким течением инфекции гуморальные показатели были более высокими у тяжелых больных, в то время как CD8+-Т-клетки были стабильными, а CD4+ — более низкими в тяжелых случаях заболевания. Объяснений этому феномену нет, важно, что слабый ответ Т-клеток наблюдается в острой фазе заболевания. Кроме того, важна и методология исследования клеточного им-мунитета.
Нарушения клеточного ответа проиллюстрированы дефицитом интерферонов I и II типов у пациентов с тяжелыми и среднетяжелыми формами COVID‑19 по сравнению с легкими и бессимптомными случаями заболевания. Это может быть связано с подавлением воспаления интерлейкином‑12 (IL‑12) и развитием вторичного дефекта клеточного иммунитета.
Иммунное взаимодействие
Большой интерес представляет изучение взаимодействия гуморального и клеточного ответа на SARS-Cov‑2. В исследованиях RBD-IgG, Spike IgА, RBD-В-клеток памяти, CD8+- и CD4+-Т-клеток в динамике у одних и тех же пациентов установлено, что у большинства из них (64 %) положительные показатели отмечались через 1–2 месяц после начала заболевания. Через 5–8 месяцев число реконвалесцентов, позитивных на пять тестов, снизилось до 43 %. В то же время как минимум три из пяти тестов были положительными спустя 6–9 месяцев. Важно отметить, что IgG на Spike дает на порядок больше положительных ответов, чем на RBD-антиген. Попытки связать гуморально- клеточные взаимодействия не привели к успеху из-за неоднородности участников исследования и методик оценки иммунного ответа.
Неопределенный результат
В метаанализе 22 исследований (4969 пациентов) установлены неблагоприятные признаки тяжелых форм болезни и летальных исходов, такие как лимфопения и нейтрофилез. Поскольку CD4+-Т-клетки необходимы для сбалансированного и эффективного иммунного ответа, неудивительно, что низкий уровень лимфоцитов может отражать гипервоспалительные процессы и способствовать более тяжелому течению заболевания и повышенной смертности.
Нейтрофилы как неотъемлемая часть врожденной защиты контролируют баланс микробиоты и элиминацию продуктов клеточной деструкции за счет производства активных форм кислорода и высвобождения нейтрофильных внеклеточных ловушек в венозном кровотоке. Лимфопения (менее 500 клеток в 1 мкл) указывает на повышение риска тяжелой формы заболевания и смертельных исходов при COVID‑19 в 3 раза. Стойкий нейтрофилез со сдвигом влево свидетельствует об истощении костномозгового резерва, а при сдвиге вправо отражает нарушения выхода клеток в ткани. Этот легко контролируемый анализом крови параметр указывает на более чем семикратное увеличение для пациента риска заболеть тяжело и погибнуть от COVID‑19.
Попытки выявить закономерности иммунного ответа на SARS-CoV‑2 оказались пока безуспешными.
Во-первых, можно сделать вывод, что переболевшие коронавирусной инфекцией сохраняют иммунную память в последующие 6–9 месяцев. Дальнейшие динамические исследования покажут, в какие сроки наступает снижение иммунного ответа, требующее профилактической вакцинации и (или) ревакцинации.
Во-вторых, и это очень интересно, каждый изученный компонент иммунного ответа и иммунной памяти демонстрирует различную кинетику. Это связано с индивидуальным ответом на инфекцию, наличием преморбида и частого превращения моноинфекции в смешанные инфекции SARS-CoV‑2 с активизировавшейся микробиотой больного.
В-третьих, неоднородность ответа может быть центральным признаком, характеризующим иммунную память к SARSCoV‑2. Биологические специфические IgG имеют 21 день периода полураспада, уровень антител с течением времени отражает продукцию короткоживущих, а потом и долгоживущих плазматических клеток. С точки зрения исчезновения возбудителя в течение нескольких дней после появления клиники, процесс наработки антител должен быть снижен к 6 месяцам, но, если SARS-CoV‑2 Spike и RBD IgG сохраняются дольше 8 месяцев, это означает, что вирус персистирует в организме хозяина или его микробиоте. Нельзя исключать и связь с пролонгированным иммунным ответом естественной реиммунизации циркулирующими эпидемическими альфа-коронавирусами, поддерживающими иммунный ответ.
В-четвертых, выявление и анализ SARSCoV‑2‑специфических В-клеток памяти потенциально могут применяться в качестве маркера гуморального ответа при вакцинации. Сейчас исследования поствакцинального иммунного ответа проводятся с использованием иммунофлуоресцентного анализа с оценкой IgM- и IgG-антител в качестве маркеров эффективности вакцины (рис. 3). Методы ИФА-диагностики, к сожалению, не стандартизованы едиными белками S, RBD, NCP, качество которых зависит от очистки антигена. Поскольку количество В-клеток памяти стабильно с течением времени, они могут представлять собой более надежный маркер продолжительности гуморальных иммунных реакций, чем иммуноглобулины сыворотки крови.
Таким образом, из результатов исследований иммунного ответа у больных COVID‑19 невозможно сделать какие-либо выводы о защитном иммунитете при новой коронавирусной инфекции. Ведь изучение антител и клеток памяти при этом заболевании пока еще не завершено. А значит, обсуждаемые механизмы защитного иммунитета против SARS-CoV‑2 у людей окончательно не определены.
Источник: Газета «Педиатрия сегодня» №6, 2021
Комплексный механизм развития СOVID-19
Полный текст:
Аннотация
Ключевые слова
31 декабря 2019 года власти Китайской Народной Республики официально заявили об эпидемии новой, до сих пор неизвестной инфекции. Главным очагом вспышки данного заболевания явился город Ухань (провинция Хубэй). Было выявлено, что возбудителем является РНК-геномный вирус рода Betacoronavirus семейства Coronaviridae, который наименовали Severe acute respiratory syndromerelated coronavirus 2 (SARS-CoV-2) из-за его высокой гомологии (
80%) с SARS-CoV, который вызывал острый респираторный дистресс-синдром (ОРДС) и высокую смертность в 2002–2003 годах.
11 марта 2020 г. Всемирная организация здравоохранения объявила о пандемии CoronaVirus Disease-19 (COVID-19) — официальное название заболевания, вызванного SARS-CoV-2, которое оказало влияние на большое количество людей во всем мире, о чем сообщается примерно в 200 странах [1].
Считалось, что вспышка SARS-CoV-2 первоначально началась через зоонозную передачу, связанную с рынком морепродуктов в Ухани. Позже было признано, что передача вируса от человека к человеку сыграла важную роль в последующей вспышке [2].
Входные ворота возбудителя — эпителий верхних дыхательных путей и эпителиоциты желудка и кишечника. Начальным этапом заражения является проникновение SARS-CoV-2 в клетки-мишени, имеющие рецепторы ангиотензинпревращающего фермента II типа (ACE2 — аngiotensin-converting enzyme 2) [3].
Рецепторы ACE2 представлены на клетках дыхательного тракта, почек, пищевода, мочевого пузыря, подвздошной кишки, сердца, центральной нервной системы, эндотелия.
ACE2 может быть выделен двумя протеазами: ADAM17 (a disintegrin and metalloproteinase domain 17, домен дезинтегрина и металлопротеиназы 17) и TMPRSS2 (transmembrane serine protease 2, трансмембранная сериновая протеаза 2). ACE2, расщепленный TMPRSS2, позволяет проникать SARS-CoV-2 в клетки, тогда как расщепление рецептора с помощью ADAM17 обеспечивает защиту органов [4].
Взаимодействие с Толл-подобными рецепторами
Вирус попадает в организм через дыхательные пути и взаимодействует в первую очередь с Toll-like receptor (TLR, Толл-подобными рецепторами) (рис. Блок 1). ТLR являются основными специализированными клеточными структурами, которые способны распознавать различные инфекционные агенты — микробы, вирусы, некоторые простейшие (прежде всего продукты их жизнедеятельности — экзотоксины и распада — эндотоксины) и инициировать на генетическом уровне экспрессию биологически активных веществ — цитокинов, детерминирующих запуск и формирование механизмов неспецифической резистентности организма. Распознав инфекционную агрессию, TLR немедленно «бьют в набат», инициируя включение противоинфекционных защитно-приспособительных механизмов организма на клеточном уровне.
Трансмембранные TLR состоят из двух доменов — внеклеточного, обеспечивающего прямое взаимодействие с лигандами микроорганизмов или продуктами их жизнедеятельности и распада, и внутриклеточного (цитоплазматического), инициирующего трансляцию сигналов активированных TLR. После взаимодействия с лигандами TLR приобретают способность связывать внутриклеточные адаптерные белки, которые обеспечивают последующую передачу сигнала. Эти белки имеют фрагмент специфического связывания с активированными TLR.
Выявление вирусов, в том числе SARS-Cov-2 и других внутриклеточных микроорганизмов, является основной целью функционирования другого семейства TLR, которые локализованы в цитоплазме и на внутренних структурах клеток (в области аппарата Гольджи и др.). Это небольшое внутриклеточное семейство объединяет TLR3, TLR7 и TLR9.
Знаковым событием в изучении врожденного иммунитета явилось обнаружение TLR на эндотелиоцитах и эпителиальных клетках кожи и слизистых оболочек. Эпителий, распознав с помощью TLR инфекционный фактор, инициирует немедленную мобилизацию механизмов его ликвидации «собственными силами» или путем привлечения адаптивного иммунного ответа.
Эти события развиваются по следующему сценарию: эпителиальные клетки вначале с помощью TLR распознают и идентифицируют SARS-CoV-2; полученная информация передается к транскрипционному ядерному фактору NF-κB, который вызывает экспрессию соответствующих генов. Активированные эпителиальные клетки начинают синтезировать различные биологически активные молекулы, в том числе — хемокины. Данные цитокины, обладая хемоаттрактирующим действием, привлекают к месту внедрения инфекции макрофаги и полиморфноядерные лейкоциты: нейтрофилы, базофилы, эозинофилы, которые, в свою очередь, как и эпителиоциты, активируются, фагоцитируют инфекционный фактор и выделяют при этом свой набор провоспалительных медиаторов.
Таким образом, внутриклеточные инфекционные факторы — вирусы (SARS-Cov-2), ряд микробов (возбудителей сифилиса, туберкулеза, лепры и др.) распознаются TLR, локализованными на внутренних структурах клеток. На основании этого можно предположить, что вакцинация против туберкулеза защищает организм от патогенного воздействия SARS-Cov-2. Вакцина против туберкулеза через внутриклеточные TLR активирует в том числе и такие механизмы защиты, которые направлены на возбудителей, к которым принадлежит и SARS-CoV-2. Этот механизм у детей очень выражен, а с возрастом он исчезает. По-видимому, благодаря этому дети мало заболевают COVID-19.
SARS-CoV-2 проникает в клетку, используя рецептор ACE2 [5] и фермент TMPRSS2. Но самым необычным оказалось то, что ген ACE2, который кодирует рецептор, используемый SARS-CoV-2 для проникновения в клетки человека, стимулируется интерфероном — одной из основных защитных сил организма при обнаружении вируса. Интерферон фактически включает синтез рецептора ACE2 на более высоких уровнях, предоставляя вирусу новые «порталы» для проникновения. Таким образом, использование интерферона на стадии, когда вирус активно проникает в клетки человека, может еще более усугубить ситуацию [6].
Взаимодействие с рецепторами ангиотензинпревращающего фермента 2
Жизненный цикл вируса при взаимодействии его с хозяином состоит из следующих 5 этапов: прикрепление, проникновение, биосинтез, созревание и высвобождение. После связывания с рецепторами хозяина вирус проникает в клетки хозяина посредством эндоцитоза или слияния мембран. Как только вирусное содержимое высвобождается внутри клеток-хозяев, вирусная РНК поступает в ядро для репликации. Вирусная матричная РНК используется для биосинтеза вирусных белков. Затем создаются новые вирусные частицы, которые выпускаются из клетки [7].
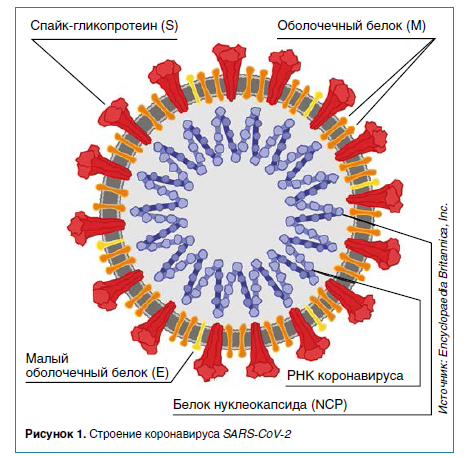
Коронавирусы состоят из четырех структурных белков; спайка, мембраны, оболочки и нуклеокапсида. Спайк состоит из двух функциональных субъединиц: S1 отвечает за связывание с рецептором клетки-хозяина, а S2 — за слияние вирусных и клеточных мембран.
В качестве функционального рецептора для SARS-CoV-2 идентифицирован ACE2 (рис. Блок 2). Структурный и функциональный анализ показал, что степень взаимодействия SARS-CoV-2 также связана с ACE2 [5].
Обнаружена высокая экспрессия ACE2 в легких, сердце, подвздошной кишке, почках, эндотелиоцитах и мочевом пузыре [8]. В легких ACE2 высоко экспрессирован на эпителиальных клетках бронхов. Продемонстрировано, что, когда спайковый белок SARS связывается с рецептором ACE2, комплекс подвергается протеолизу TMPRSS2, что приводит к расщеплению ACE2 и активации спайкового белка, способствуя проникновению вируса в клетку-мишень. Предполагается, что клетки, в которых одновременно присутствуют ACE2 и TMPRSS2, наиболее подвержены проникновению SARS-CoV [9].
Уникальной характеристикой SARS-CoV-2 среди коронавирусов является наличие участка расщепления фурином на сайте S1/S2, который полностью подвергается расщеплению во время биосинтеза в резком контрасте с шипом SARS-CoV, включенного в сборку без расщепления, что делает SARS-CoV-2 высокопатогенным [10]. Кроме того, SARS-CoV-2, по-видимому, обладает молекулярной мимикрией с белками хозяев — эволюционной стратегией, принятой вирусами для уклонения от иммунного надзора и использования систем клеток-хозяев.
Имеются данные, что SARS-CoV-2 развил уникальную вставку расщепления S1/S2, отсутствующую в любом из предыдущих секвенированных коронавирусов, что приводит к поразительной мимикрии идентичного фурин расщепляемого пептида на α-субъединице эпителиального натриевого канала человека (ENaC-α) [11]. Иначе говоря, в коронавирусе есть участок идентичный части человеческого белка. Эта фуриновая вставка, находящаяся на участке S1/S2, отвечает за вход вируса в клетку. Белок ENaC-α участвует в регуляции водно-солевого баланса эпителиальных клеток, и нарушение его функции может вызывать отечность, что и наблюдается в тканях при тяжелом течении COVID-19. Механизм возникновения отечности объясняется довольно просто: вирус использует человеческую протеазу TMPRSS2, чтобы проникнуть внутрь клетки, но при этом заодно мешает работать тому же самому человеческому белку, который тоже зависит от этой протеазы. Получается двойной удар: облегчается проникновение вируса в клетку и нарушается водно-солевой обмен в местах инфекции, что приводит к возникновению отеков.
Повреждающее действие на клетки дыхательных путей
Поскольку ACE2 высоко экспрессируется на апикальной стороне эпителиальных клеток легких в альвеолярном пространстве, этот вирус может проникать и разрушать их. SARS-CoV-2 очень быстро распространяется и мигрирует вниз по дыхательным путям [12]. Как SARS-CoV и вирус гриппа, так и SARS-CoV-2 преимущественно инфицирует пневмоциты II типа [13][14], приводя к апоптозу и гибели этих клеток, вследствие чего снижается синтез сурфактанта [15] (рис. Блок 2).
При дефиците сурфактанта происходит спадение (ателектазирование) одних альвеол и перерастяжение других с последующим их разрывом, т. е. развивается синдром утечки воздуха. Такая ситуация детерминируется гетерогенностью легких и, следовательно, разной степенью выраженности дефицита клеток — продуцентов поверхностно активных веществ легких, возникающем при синдроме полиорганной недостаточности (СПОН).
Кроме того, при дефиците сурфактанта нарушается санация альвеол и нижних дыхательных путей — перемещение слизи, мокроты в зону мукоцилиарного транспорта из-за уменьшения продольного градиента поверхностного давления.
Также под воздействием SARS-CoV-2 силы поверхностного натяжения могут вызывать не только спадение альвеол, но и «засасывание» в них жидкости из капилляров. Отсюда раннее развитие интерстициального отека при остром респираторном дистресс-синдроме (ОРДС). Силы молекулярного взаимодействия на разделе фаз жидкость/воздух (молекулы воды легче преодолевают межфазный раздел) могут способствовать задержке жидкости в альвеолах — развитию альвеолярного отека. Таким образом, дефицит сурфактанта является достаточным фактором, приводящим к включению всех известных патогенетических механизмов развития ОРДС.
Развитие фиброза легких
Пневмоциты II типа являются клетками-предшественниками пневмоцитов I типа [15]. Накоплению фибрина в сосудах легких способствует снижение содержания активаторов фибринолиза в легочном эндотелии. Фибрин может выходить в интерстиций и приводить к формированию склерозирующего альвеолита. Выходу фибрина в просвет альвеол благоприятствует нарастающее поражение пневмоцитов II типа. Экстравазаты фибрина в альвеолах вызывают образование гиалиновых мембран, которые являются одним из главных признаков ОРДС (рис. Блок 2).
Таким образом, патологическим результатом проникновения в дыхательную систему SARS-CoV-2 является диффузное повреждение альвеол с образованием гиалиновых мембран, богатых фибрином [16].
Гиперпродукция хемокинов
Эпителиальные клетки вначале с помощью TLR распознают и идентифицируют SARS-CoV-2. Полученная информация передается к транскрипционному ядерному фактору NF-κB, который вызывает экспрессию соответствующих генов (рис. Блок 1). Активированные таким образом эпителиальные клетки начинают синтезировать различные биологически активные молекулы, в том числе — хемокины, ростовые регуляторные онкогены α, β, γ (GRO-α, GRO-β, GRO-γ), интерлейкин-8 (IL-8, CXCL8), интерферон-γ, макрофагальные воспалительные протеины 1α, 1β (MIP-1α, MIP-1β), регулятор активации нормальной Т-клеточной экспрессии и секреции (RANTES, CCL5).
Данные цитокины, обладая хемоаттрактирующим действием, привлекают к месту внедрения инфекции макрофаги и полиморфноядерные лейкоциты: нейтрофилы, базофилы, эозинофилы, которые, в свою очередь, как и эпителиоциты, активируются, фагоцитируют инфекционный фактор и выделяют при этом свой набор провоспалительных медиаторов. Представленный сценарий противоинфекционной защиты является проявлением врожденного иммунитета.
Кроме того, эпителиоциты продуцируют гранулоцитарный (granulocyte colony-stimulating factor — G-CSF) и гранулоцитарно-макрофагальный колониестимулирующие факторы (granulocyte-macrophage colony-stimulating factor — GM-CSF). Данные колониестимулирующие факторы индуцируют дифференцировку клеток миелоидного происхождения: G-CSF активирует дифференцировку, пролиферацию нейтрофилов, а GM-CSF стимулирует пролиферацию и дифференцировку различных типов иммунных клеток-предшественников. В ткани легких GM-CSF вызывает пролиферацию и активацию легочных дендритных клеток и макрофагов. Мыши с дефицитом GM-CSF высокочувствительны к респираторным вирусам. Хемокин CXCL8 целенаправленно рекрутирует нейтрофилы в очаг поражения легких [17].
Гиперпродукция хемокина CXCL8 обусловливает привлечение большого числа нейтрофилов в пораженные ткани. Многие медиаторы, высвобождаемые самими нейтрофилами, являются нейтрофильными хемоаттрактантами, поэтому нейтрофилы могут рекрутировать другие нейтрофилы. В свою очередь, нейтрофилы, продуцируя провоспалительные цитокины и хемокины, привлекают моноциты.
Высокий уровень нейтрофилов в периферической крови ассоциирован с неблагоприятным прогнозом COVID-19 [18]. Нейтрофилы характеризуются быстрым темпом фагоцитоза, более высокой интенсивностью генерации активных форм кислорода (АФК). Гранулы нейтрофилов содержат достаточно широкий спектр ферментов, которые секретируются во внеклеточное пространство и могут вызывать деструкцию тканей [19]. Несмотря на присутствие нейтрофилов в тканях, инфицированных SARS-CoV-2, их роль в клиренсе коронавирусов остается неизвестной.
Активация NF-κB и гиперпродукция цитокинов
NF-κB был открыт в лаборатории нобелевского лауреата Д. Балтимора в 1986 г. как транскрипционный фактор, необходимый для специфической экспрессии генов в В-лимфоцитах. В дальнейшем была обнаружена его уникальная роль в патогенезе самых разных форм патологии. Воздействие на этот фактор постепенно приобретает облигатный характер при лечении многих заболеваний.
NF-κB совместно с I-κB образует IKK (ингибиторный киназный комплекс NF-κB).
Активация IKK необходима для высвобождения (приведение в активное состояние) NF-κB: IKK фосфорилирует ингибитор NF-κB — I-κB. Освобожденный вследствие деградации I-κB транскрипционный фактор NF-κB транслоцируется в ядро, где стимулирует экспрессию своего ингибитора I-κB. Затем эта вновь синтезированная (экспрессированная) молекула I-κB транслоцируется в ядро и препятствует дальнейшему взаимодействию NF-κB с регуляторными участками ДНК. Иначе говоря, существует петля отрицательной обратной связи, которая по механизму ауторегуляции ограничивает активность NF-κB.
Можно предположить, что SARS-CoV-2 нарушает взаимодействие NF-κB c I-κB. Он ингибирует экспрессию I-κB и таким образом не препятствует дальнейшему взаимодействию NF-κB с регуляторными участками ДНК. Это приводит к бесконтрольному образованию провоспалительных цитокинов.
Заболевание COVID-19 сопровождается чрезвычайно высоким уровнем продукции провоспалительных цитокинов (IFN-α, IFN-γ, IL-1β, IL-6, IL-12, IL-18, IL-33, TNF-α, GM-CSF и др.) и хемокинов (CCL2, CCL3, CCL5, CXCL8, CXCL9, CXCL10 и др.) [20], в связи с чем цитокиновая реакция, наблюдаемая у пациентов, инфицированных SARS-CoV-2, получила название «цитокиновая буря» (рис. Блок 1). Данные цитокины и хемокины рекрутируют эффекторные иммуноциты, обусловливая развитие местного воспалительного ответа. Характерной особенностью тяжелых форм является снижение продукции IL-10. «Цитокиновая буря» лежит в основе развития пневмонии и ОРДС и полиорганной недостаточности, которые в тяжелых случаях SARS-CoV-2 инфекции приводят к летальному исходу [21][22][23].
Тяжелое течение COVID-19 сопровождается значительно более высоким уровнем в сыворотке крови таких цитокинов, как IL-1β, IL-6, TNF-α, CXCL8. Установлено, что риск летального исхода заболевания ассоциирован именно с высоким уровнем IL-6 в сыворотке крови [24]. Предполагают, что вирус начинает вторую атаку, вызывая ухудшение состояния пациента примерно через 7–14 дней после начала заболевания. От появления первых симптомов COVID-19 до развития ОРДС в среднем проходит 8 суток [25].
Поражение легких и в первую очередь развитие пневмонии является основной причиной как тяжести течения, так и летальных исходов COVID-19 [23]. Возникающие в начале развития ОРДС нарушения перфузии легких приводят к повышению проницаемости альвеолярно-капиллярных мембран вследствие их гипоксической альтерации. Этот фактор, наряду с дефицитом сурфактанта, обуславливает развитие интерстициального отека легочной ткани, а затем — накопление жидкости в альвеолярном пространстве.
Активация свободнорадикальных процессов
Имеется четкая корреляционная связь между маркерами оксидативного стресса и тяжестью многих вирусных заболеваний, таких как гепатит C, однако для SARS-CoV клинических данных очень мало. Тем не менее результаты, полученные на доклиническом материале, свидетельствуют о том, что увеличивается генерация АФК и снижается антиоксидантная защита, что играет основную роль в патогенезе SARSCoV, а также в прогрессировании и тяжести данного респираторного заболевания. На экспериментальной модели на животных с тяжелым острым респираторным синдромом выявлены повышенные уровни АФК и снижение антиоксидантной защиты под влиянием SARS-CoV [29].
Окислительный стресс, NF-κB, TLR (TLR4) сигнальные пути, запускаемые вирусными патогенами, такими как SARS-CoV-2, могут дополнительно усиливать воспалительную реакцию хозяина, в конечном счете приводя к острому повреждению легких (рис. Блок 1). Передача сигналов TLR4-TRIFTRAF6 была идентифицирована как патогенный путь, который может опосредовать тяжесть острого повреждения легких. Окисленный фосфолипид, вырабатываемый макрофагами легких, способен вызывать большое образование цитокинов и повреждение легких с помощью TLR4-TRIF. Окисленные фосфолипиды были ранее идентифицированы в легких человека и животных, инфицированных вирусом SARS. В моделях in vivo потеря экспрессии TLR4 или TRIF защищала мышей от острого повреждения легких, вызванного вирусом птичьего гриппа 5N1. Кроме того, делеция ncf1, которая может регулировать генерацию АФК, уменьшает степень острого повреждения легкого. Таким образом, эти авторы предполагают, что окислительный стресс и врожденный иммунитет играют ключевую роль в тяжести острого повреждения легкого, вызываемого респираторными вирусами [32].
Развитие эндотелиальной дисфункции
SARS-CoV-2 нарушает функцию эндотелия [33][34] (рис. Блок 2). У пациентов с COVID-19 обычно наблюдаются артериальная гипертензия [35][36][37][38][39], тромбозы [40][41][42], повреждение почек [43][44], легочная эмболия [45][46], цереброваскулярные и неврологические расстройства [47][48], что, несомненно, указывает на то, что вирус направлен на повреждение эндотелия, одного из крупнейших органов в организме человека. Случаи болезни Кавасаки (системный васкулит) у детей с COVID-19 только подтверждают данную точку зрения [49].
Рецепторы ACE2 также экспрессируются эндотелиальными клетками [50]. Следует отметить, что все факторы, принимающие участие в проникновении SARS-CoV-2 в клетку, такие как сиаловая кислота, TMPRSS2, индуктор внеклеточной матричной металлопротеиназы (CD147) и катепсины B и L, также экспрессируются в эндотелиальных клетках [51].
Можно предположить, что SARS-CoV-2, попадая в эндотелиоцит, активирует NF-κB напрямую или через вызываемое им увеличенное количество АФК.
В конечном счете эндотелиальная клетка начинает продуцировать большое количество проагрегантов и вазоконстрикторов, что приводит к более высокой смертности [41, 52].
У пациентов с летальным исходом в результате инфекции SARS-CoV-2 на момент поступления были обнаружены значительно более высокие уровни D-димера и продуктов деградации фибрина, а также удлинение протромбинового времени по сравнению с выжившими пациентами [53]. На поздних сроках госпитализации у этой же группы пациентов наблюдалось значительное снижение содержания фибриногена и антитромбиновой активности, что характерно для диссеминированного внутрисосудистого свертывания (ДВС-синдром) [54].
Следует отметить, что ДВС-синдром, вызываемый системной инфекцией, характеризуется острым системным чрезмерным воспалительным ответом, тесно связанным с эндотелиальной дисфункцией [55].
Эндотелиальная дисфункция, возникающая под влиянием SARS-CoV-2, приводит к массивному тромбообразованию и закупорке мелких сосудов легких, почек, сердца, печени и других органов микротромбами, что вызывает нарушение микроциркуляции в данных органах и соответственно нарушение их функции. Микротромбоз легочных микрососудов приводит к нарушению перфузии легких. Действительно, легочный эндотелий представляет собой фундаментальный барьер между кровью и интерстицием и выполняет жизненно важные регуляторные функции; в частности, эндотелиальные клетки составляют одну треть клеточной популяции легкого, а повреждение легочного эндотелия еще больше усугубляет ОРДС.
У пациентов с COVID-19 с массивным микротромбозом и нарушением микроциркуляции возникает шоковое состояние с полиорганной недостаточностью, что в конечном счете может привести к летальному исходу.
Дисфункция эндотелия может быть самостоятельной причиной нарушения кровообращения в органе, поскольку нередко провоцирует ангиоспазм или тромбоз сосудов [56], что, в частности, наблюдается при некоторых формах ишемической болезни сердца. Тромбоз глубоких вен и/или тромбоэмболия легочной артерии ранее были описаны у пациентов с ОРВИ [57], а также сообщалось о случаях тромбоза, осложняющего ассоциированную с гриппом пневмонию [58].
При повреждении эндотелия у пациентов с COVID-19 его поверхность из антитромботической превращается в протромботическую. В случае обнажения проадгезивной поверхности субэндотелиального матрикса его компоненты — адгезивные белки (фактор фон Виллебранда, коллаген, фибронектин, тромбоспондин, фибриноген) немедленно включаются в процесс образования первичного (сосудистотромбоцитарного) тромба и, затем — гиперкоагуляции. Эндотелий способен продуцировать и выделять целый ряд веществ, таких как катехоламины, эндотелиин-1, ангиотензин-2, оказывающих сосудосуживающее действие. Ангиотензин II повышает проницаемость микрососудов, индуцирует транскрипцию тканевого фактора в эндотелиальных клетках и активирует тромбоциты. Кроме того, ангиотензин II может запускать высвобождение нескольких компонентов системы комплемента из эндотелиальных клеток, что дополнительно подтверждает ключевую роль эндотелия в патогенезе венозного и артериального тромбоза у пациентов с COVID-19 [59]. Таким образом, у пациентов с COVID-19 течение заболевания может осложниться инсультом, инфарктом или тромбозом артерий нижних конечностей с развитием полиорганной недостаточности.
Повреждение кишечника
Повреждение эпителия кишечника под воздействием SARS-CoV-2 может приводить к обширному отмиранию его слизистой. Повреждение кишечника обусловливает развитие синдрома кишечной аутоинтоксикации и синдрома мальабсорбции. Поврежденный кишечник становится источником «второй волны» поступающих в системный кровоток биологически активных веществ (в первую очередь цитокинов и АФК), которые потенцируют действие медиаторов «первой волны», обусловленной инициатором (SARS-CoV-2) развития СПОН (рис. Блок 2).
Повреждение естественного барьера кишечной стенки в условиях нестабильной гемодинамики приводит к перераспределению мезентериального кровотока и миграции (транслокации) внутрикишечных бактерий и их токсинов в брюшную полость с последующим развитием перитонита. Поступление токсинов и микробиоты по воротной вене в печень приводит к ее повреждению и дисфункции.
Одним из патогенетических факторов развития печеночной недостаточности считается индуцируемое эндотоксином нарушение портального кровотока. Кроме того, эндотоксинемия кишечного происхождения вызывает отсроченные повреждения «отдаленных» органов.
Развитие синдрома полиорганной недостаточности
В общих чертах схема развития сепсис-индуцированного СПОН при COVID-19 может быть представлена следующим образом. Проникший в организм SARS-CoV-2 распознается семейством TLR, которые запускают механизм образования цитокинов. Ключевыми цитокинами — медиаторами септической формы СПОН являются TNF-α, IL-1и IL-6, массивный выброс которых происходит из моноцитов, макрофагов и нейтрофилов. Цитокины опосредуют свое действие путем активации NF-κB (рис. Блок 1).
Последующие за активацией NF-κB и других транскрипционных факторов изменения генетической программы детерминируют стимуляцию синтеза вначале — «ранних» цитокинов, а затем (вторая волна) — «поздних» цитокинов и других медиаторов системной воспалительной реакции. Медиаторы вызывают многообразные метаболические и функциональные изменения в организме, манифестирующие развитие септической, а также и других — асептических форм СПОН. Одним из основных патогенетических компонентов этой формы патологии является нарушение микроциркуляции, которое вначале приводит к развитию системной капиллярно-трофической недостаточности, а затем в большой мере детерминирует формирование СПОН.
Прежде всего «удар волны» медиаторов воспаления принимают на себя легкие — «биохимический фильтр» крови на пути к головному мозгу, что приводит к их повреждению, или, согласно современной номенклатуре, развитию синдрома острого повреждения легких, который рассматривается в качестве «типового пейсмейкера» СПОН.
Комплекс факторов, составляющих патогенетическую основу многообразной клинической симптоматики СПОН, включает в себя острую дыхательную недостаточность (генерализованная гипоксия), нарушение микроциркуляции (капиллярно-трофическая недостаточность), эндотелиальную дисфункцию (нарушение регуляции просвета сосудов и системы гемостаза), энтеральную недостаточность (синдром кишечной аутоинтоксикации, синдром мальабсорбции), изменения метаболизма (синдром «гиперметаболизма», синдром «аутокатаболизма»), энцефалопатию (расстройства функции центральной нервной системы).
SARS-CoV-2 может вызывать локальное повреждение органа/ткани или оказывать генерализованное повреждающее воздействие на организм. При первом варианте возникает локальное адекватное классическое воспаление: SARS-CoV-2 и альтерированные клетки/ткани блокируются, инактивируются и выводятся из организма, что исключает возможность генерализации процесса. При втором — развивается неадекватное локальное воспаление с тяжелым повреждением тканей, недостаточной ограничительной функцией воспаления, чрезмерным образованием и массивным выходом медиаторов этого процесса в системный кровоток.
«Наводнение» крови различными биологически активными веществами происходит не только в условиях развития неадекватного воспаления, но и сопровождает любое более или менее выраженное генерализованное поражение организма.
Медиаторами гуморального компонента системного ответа в условиях развития СПОН являются: цитокины, компоненты системы комплемента, продукты метаболизма арахидоновой кислоты, фактор активации тромбоцитов, гистамин, клеточные адгезивные молекулы, токсические метаболиты кислорода, компоненты калликреин-кининовой системы и многие другие, общее число которых исчисляется сотнями.
Одной из характеристик СПОН служит фазность развития этого синдрома. Несмотря на отсутствие единой, согласованной точки зрения о патогенезе СПОН, с патофизиологической точки зрения представляется достаточно убедительной концепция «трехфазного ответа» под влиянием SARS-CoV-2.
Инициация СПОН связана с закономерным развитием системного защитно-приспособительного ответа организма, который состоит из двух компонентов: нейроэндокринного (стресс-реакция) и гуморального (по преимуществу «цитокинового» ответа). Данный системный ответ индуцирует включение адаптационных механизмов, направленных на мобилизацию, перераспределение, адекватное использование энергетических и пластических ресурсов с целью сдерживания масштаба альтерации, создания неблагоприятных условий для SARS-CoV-2.
Патогенетическую основу таких механизмов составляют системные изменения метаболизма. Поэтому следующий этап развития СПОН получил название «фаза метаболического ответа». Разумеется, на данном этапе происходят различные изменения функционального характера, которые, с одной стороны, направлены на обеспечение «метаболического ответа», а с другой — являются его следствием, т. е. по существу эти изменения не являются «центральным патогенетическим событием» этой фазы СПОН. Исключением из данного утверждения являются изменения (функционального и органического характера) желудочно-кишечного тракта, которые возникают в связи с «отказом» организма от «услуг» пищеварительной системы вследствие перехода на более доступные эндогенные резервы питания. Возникающее при этом повреждение желудочно-кишечного тракта детерминирует развитие синдрома мальабсорбции и синдрома кишечной аутоинтоксикации, которые обуславливают дальнейшее развитие и утяжеление СПОН (рис. Блок 2). Этот завершающий этап формирования данного синдрома получил название «фаза вторичной аутоагрессии», так как она детерминирована не столько этиологическими, сколько патогенетическими факторами СПОН. Такова в самом общем виде «трехфазная» концепция патогенеза СПОН, возникающая под влиянием SARS-CoV-2.
ВКЛАД АВТОРОВ
С.Б. Болевич внес основной вклад в разработку концепции идеи и написание текста статьи, окончательно утвердил публикуемую версию статьи и согласен принять на себя ответственность за все аспекты работы. С.С. Болевич внесла существенный вклад в редактирование текста статьи, а также осуществляла координирование обзора.
AUTHOR CONTRIBUTIONS
Sergey B. Bolevich: concept development, writing, critical revision of the manuscript for important intellectual content, approved the final version of the publication and agreed to take responsibility for all aspects of the work. Stefani S. Bolevich: critical revision of the manuscript for important intellectual content and supervision.
Список литературы
1. Zheng M., Gao Y., Wang G., et al. Functional exhaustion of antiviral lymphocytes in COVID-19 patients. Cell Mol Immunol. 2020 May; 17(5): 533–5. https://doi.org/10.1038/s41423-020-0402-2 PMID: 32203188
2. Li Q., Guan X., Wu P., et al. Early transmission dynamics in Wuhan, China, of Novel Coronavirus-infected pneumonia. N Engl J Med. 2020 Mar 26; 382(13): 1199–207. https://doi.org/10.1056/NEJMoa2001316 PMID: 31995857
3. Wan Y., Shang J., Graham R., et al. Receptor recognition by novel coronavirus from Wuhan: an Analysis based on decade-long structural studies of SARS. J Virol. 2020 Mar 17; 94(7): e00127–20. https://doi.org/10.1128/JVI.00127-20 PMID: 31996437
4. Xiao L., Sakagami H., Miwa N. ACE2: The key molecule for understanding the pathophysiology of severe and critical conditions of COVID-19: Demon or Angel? Viruses. 2020 Apr 28; 12(5): 491. https://doi.org/10.3390/v12050491 PMID: 32354022
5. Chen Y., Guo Y., Pan Y., et al. Structure analysis of the receptor binding of 2019-nCoV. Biochem Biophys Res Commun. 2020 Feb 17; 525(1): 135–40. https://doi.org/10.1016/j.bbrc.2020.02.071 PMID: 32081428
6. Ziegler C., Allon A.S., Nyquist S.K., et al. SARS-CoV-2 Receptor ACE2 is an interferon-stimulated gene in human airway epithelial cells and is enriched in specific cell subsets across tissues. Cell. 2020 May 28; 181(5): 1016–35.e19. https://doi.org/10.1016/j.cell.2020.04.035 PMID: 32413319
7. Yuki K., Fujiogi M., Koutsogiannaki S. COVID-19 pathophysiology: A review. Clin Immunol. 2020 Jun; 8. Zou X., Chen K., Zou J., et al. Single-cell RNA-seq data analysis on the receptor ACE2 expression reveals the potential risk of different human organs vulnerable to 2019-nCoV infection. Front Med. 2020 Apr; 14(2): 185–92. https://doi/org/10.1007/s11684-020-0754-0 PMID: 32170560
8. Zhou P., Yang X.L., Wang X.G., et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020 Mar; 579(7798): 270–3. https://doi/org/10.1038/s41586-020-2012-7 PMID: 32015507
9. Walls A.C., Park Y.J., Tortorici M.A., et al. Structure, function, and antigenicity of the SARS-CoV-2 Spike glycoprotein. Cell. 2020 Apr 16; 181(2): 281–92.e6. https://doi.org/10.1016/j.cell.2020.02.058 PMID: 32155444
10. Anand P., Puranik M., Aravamudan М., et al. SARS-CoV-2 strategically mimics proteolytic activation of human ENaC. Elife. 2020 May 26; 9: e58603. https://doi.org/10.7554/eLife.58603 PMID: 32452762
11. Wu Z., McGoogan J.M. Characteristics of and important lessons from the coronavirus disease 2019 (COVID-19) outbreak in China: summary of a report of 72314 cases from the Chinese center for disease control and prevention. JAMA. 2020 Apr 7; 323(13): 1239–42. https://doi.org/10.1001/jama.2020.2648 PMID: 32091533
12. Wu J., Wu X., Zeng W., et al. Chest CT Findings in patients with corona virus disease 2019 and its relationship with clinical features. Invest Radiol. 2020 May; 55(5): 257–61. https://doi.org/10.1097/RLI.0000000000000670 PMID: 32091414
13. Zhang S., Li H., Huang S., et al. High-resolution CT features of 17 cases of corona virus disease 2019 in Sichuan province, China. Eur Respir J. 2020 Apr 30; 55(4): 2000334. https://doi.org/10.1183/13993003.00334-2020 PMID: 32139463
14. Qian Z., Travanty E.A., Oko L., et al. Innate immune response of human alveolar type II cells infected with severe acute respiratory syndrome-coronavirus. Am J Respir Cell Mol Biol. 2013; 48(6): 742–8. https://doi/org/10.1165/rcmb.2012-0339OC PMID: 23418343
15. Xu Z., Shi L., Wang Y., et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respir Med. 2020 Apr; 8(4): 420–2. https://doi/org/10.1016/S2213-2600(20)30076-X PMID: 32085846
16. Newton A.H., Cardani A., Braciale T.J. The host immune response in respiratory virus infection: balancing virus clearance and immunopathology. Semin Immunopathol. 2016; 38(4): 471–82. https://doi/org/10.1007/s00281-016-0558-0 PMID: 26965109
17. Liu Y., Yang Y., Zhang C., et al. Clinical and biochemical indexes from 2019-nCoV infected patients linked to viral loads and lung injury. Sci China Life Sci. 2020 Mar; 63(3): 364–74. https://doi.org/10.1007/s11427-020-1643-8 PMID: 32048163
18. Genschmer K.R., Russell D.W., Lal C., et al. Activated PMN exosomes: pathogenic entities causing matrix destruction and disease in the lung. Cell. 2019 Jan 10; 176(1–2): 113–26.e15. https://doi.org/10.1016/j.cell.2018.12.002 PMID: 30633902
19. Huang C., Wang Y., Li X., et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020 Feb 15; 395(10223): 497–506. https://doi/org/10.1016/S0140-6736(20)30183-5 PMID: 31986264
20. He F., Deng Y., Li W. Coronavirus disease 2019: What we know? J Med Virol. 2020 Mar; 92(7): 719–25. https://doi/org/10.1002/jmv.25766 PMID: 32170865
21. Liu J., Zheng X., Tong Q., et al. Overlapping and discrete aspects of the pathology and pathogenesis of the emerging human pathogenic coronaviruses SARS-CoV, MERS-CoV, and 2019-nCoV. J Med Virol. 2020 May; 92(5): 491–4. https://doi.org/10.1002/jmv.25709 PMID: 32056249
22. Xu Z., Shi L., Wang Y., et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respir Med. 2020 Apr; 8(4): 420–2. https://doi.org/10.1016/S2213-2600(20)30076-X PMID: 32085846
23. Ruan Q., Yang K., Wang W., et al. Clinical predictors of mortality due to COVID-19 based on an analysis of data of 150 patients from Wuhan, China. Intensive Care Med. 2020 May; 46(5): 846–8. https://doi.org/10.1007/s00134-020-05991-x PMID: 32125452
24. Wang D., Hu B., Hu C., et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA. 2020 Mar 17; 323(11): 1061–9. https://doi.org/10.1001/jama.2020.1585 PMID: 32031570
25. Kuster G.M., Pfister O., Burkard T., et al. SARS-CoV2: should inhibitors of the renin-angiotensin system be withdrawn in patients with COVID-19? Eur Heart J. 2020 May 14; 41(19): 1801–3. https://doi.org/10.1093/eurheartj/ehaa235 PMID: 32196087
26. Bell T.J., Brand O.J., Morgan D.J., et al. Defective lung function following influenza virus is due to prolonged, reversible hyaluronan synthesis. Matrix Biol. 2019 Jul; 80: 14–28. https://doi.org/10.1016/j.matbio.2018.06.006 PMID: 2993304
27. Heldin P., Lin C.Y., Kolliopoulos C., et al. Regulation of hyaluronan biosynthesis and clinical impact of excessive hyaluronan production. Matrix Biol. 2019 May; 78–9: 100–17. https://doi.org/10.1016/j.matbio.2018.01.017 PMID: 29374576
28. van den Brand J.M.A., Haagmans B.L., van Riel D., et al. The pathology and pathogenesis of experimental severe acute respiratory syndrome and influenza in animal models. J Comp Pathol. 2014 Jul; 151(1): 83–112. https://doi.org/10.1016/j.jcpa.2014.01.004 PMID: 24581932
29. Lin C.W., Lin K.H., Hsieh T.H., et al. Severe acute respiratory syndrome coronavirus 3C-like protease-induced apoptosis. FEMS Immunol Med Microbiol. 2006 Apr; 46(3): 375–80. https://doi.org/10.1111/j.1574-695X.2006.00045.x PMID: 16553810
30. Khomich O.A., Kochetkov S.N., Bartosch B., et al. Redox biology of respiratory viral infections. Viruses. 2018 Jul 26; 10(8): 392. https://doi.org/10.3390/v10080392 PMID: 30049972
31. Imai Y., Kuba K., Neely G.G., et al. Identification of Oxidative stress and toll-like receptor 4 signaling as a key pathway of acute lung injury. Cell. 2008 Apr 18; 133(2): 235–49. https://doi.org/10.1016/j.cell.2008.02.043 PMID: 18423196
32. Gambardella J., Sardu C., Santulli G., et al. Hypertension, thrombosis, kidney failure, and diabetes: Is COVID-19 an endothelial disease? A comprehensive evaluation of clinical and basic evidence. J Clin Med. 2020 May 11; 9(5): 1417. https://doi.org/10.3390/jcm9051417 PMID: 32403217
33. Escher R., Breakey N., Lammle B. Severe COVID-19 infection associated with endothelial activation. Thromb Res. 2020 Jun; 190: 62. https://doi.org/ 10.1016/j.thromres.2020.04.014 PMID: 32305740
34. Schiffrin E.L., Flack J., Ito S., et al. Hypertension and COVID-19. Am J Hypertens. 2020 Apr 6; 33(5): 373–4. https://doi.org/10.1093/ajh/hpaa057 PMID: 32251498
35. Richardson S., Hirsch J.S., Narasimhan M. The Northwell COVID-19 research consortium. presenting characteristics, comorbidities, and outcomes among 5700 patients hospitalized with COVID-19 in the New York City Area. JAMA. 2020 May 26; 323(20): 2052–9. https://doi.org/10.1001/jama.2020.6775 PMID: 32320003
36. Chen T., Wu D., Chen H., et al. Clinical characteristics of 113 deceased patients with coronavirus disease 2019: Retrospective study. BMJ. 2020 Mar 26; 368: m1091. https://doi.org/10.1136/bmj.m1091 PMID: 32217556
37. Myers L.C., Parodi S.M., Escobar G.J., Liu V.X. Characteristics of hospitalized adults with COVID-19 in an integrated health care system in California. JAMA. 2020 Jun 2; 323(21): 2195–8. https://doi/org/10.1001/jama.2020.7202 PMID:32329797
38. Guan W.J., Liang W.H., Zhao Y., et al. Comorbidity and its impact on 1590 patients with Covid-19 in China: A Nationwide Analysis. Eur Respir J. 2020 May 14; 55(5): 2000547. https://doi.org/10.1183/13993003.00547-2020 PMID: 32217650
39. Zhou F., Yu T., Du R., et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: A retrospective cohort study. Lancet. 2020 Mar 28; 395(10229): 1054–62. https://doi.org./10.1016/S0140-6736(20)30566-3 PMID: 32171076
40. Bikdeli B., Madhavan M.V., Jimenez D., et al. Lip GYH. COVID-19 and thrombotic or thromboembolic disease: implications for prevention, antithrombotic therapy, and follow-up. J Am Coll Cardiol. 2020 Jun 16; 75(23): 2950–73. https://doi/org/10.1016/j.jacc.2020.04.031 PMID: 32311448
41. Klok F.A., Kruip M., van der Meer N.J.M., et al. Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb Res. 2020 Jul; 191: 145–7. https://doi/org 10.1016/j.thromres.2020.04.013 PMID: 32291094
42. Durvasula R., Wellington T., McNamara E., et al. COVID-19 and kidney failure in the acute care setting: our experience from Seattle. Am J Kidney Dis. 2020 Jul; 76(1): 4–6. https://doi.org/10.1053/j.ajkd.2020.04.001 PMID: 32276031
43. Ronco C., Reis T. Kidney involvement in COVID-19 and rationale for extracorporeal therapies. Nat Rev Nephrol. 2020 Jun; 16(6): 308–10. https://doi.org/10.1038/s41581-020-0284-7 PMID: 32273593
44. Rotzinger D.C., Beigelman-Aubry C., von Garnier C., Qanadli S.D. Pulmonary embolism in patients with COVID-19: Time to change the paradigm of computed tomography. Thromb Res. 2020 Jun; 190: 58–9. htpps://doi/org/10.1016/j.thromres.2020.04.011 PMID: 32302782
45. Poissy J., Goutay J., Caplan M., et al. Pulmonary embolism in COVID-19 patients: awareness of an increased prevalence. Circulation. 2020 Jul 14; 142(2): 184–6. https://doi/org/10.1161/CIRCULATIONAHA.120.047430 PMID: 32330083
46. Aggarwal G., Lippi G., Michael Henry B. Cerebrovascular disease is associated with an increased disease severity in patients with Coronavirus Disease 2019 (COVID-19): A pooled analysis of published literature. Int J Stroke. 2020 Jun; 15(4): 385–9. https://doi.org/10.1177/1747493020921664 PMID: 32310015
47. Mao L., Jin H., Wang M., et al. Neurologic Manifestations of hospitalized patients with coronavirus disease 2019 in Wuhan, China. JAMA Neurol. 2020 Jun 1; 77(6): 683–90. https://doi/org/10.1001/jamaneurol.2020.1127 PMID: 32275288
48. Riphagen S., Gomez R., Gonzalez-Martinez C., et al. Hyperinflammatory shock in children during COVID-19 pandemic. Lancet 2020, in press. 2020 May 23; 395(10237): 1607–8. https://doi/org/10.1016/S0140-6736(20)31094-1 PMID: 32386565
49. Lovren F., Pan Y., Quan A., et al. Angiotensin converting enzyme-2 confers endothelial protection and attenuates atherosclerosis. Am J Physiol Heart Circ Physiol. 2008 Oct; 295(4): H1377–84. https://doi.org/10.1152/ajpheart.00331.2008 PMID: 18660448
50. Vanarsdall A.L., Pritchard S.R., Wisner T.W. CD147 Promotes entry of pentamer-expressing human cytomegalovirus into epithelial and endothelial cells. mBio. 2018 May 8; 9(3): e00781–18. https://doi.org./10.1128/mBio.00781-18 PMID: 29739904
51. Zhang M.D., Xiao M., Zhang S., et al. Coagulopathy and antiphospholipid antibodies in patients with Covid-19. N Engl J Med. 2020 Apr 23; 382(17): e38. https://doi.org./10.1056/NEJMc2007575 PMID: 32268022
52. Tang N., Li D., Wang X., Sun Z. Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. J Thromb Haemost. 2020 Apr; 18(4): 844–7. https://doi.org/10.1111/jth.14768 PMID: 32073213
53. Lin L., Lu L., Cao W., Li T. Hypothesis for potential pathogenesis of SARS-CoV-2 infection-a review of immune changes in patients with viral pneumonia. Emerg Microbes Infect. 2020 Dec; 9(1): 727–32. htps://doi.org/10.1080/22221751.2020.1746199 PMID: 32196410
54. Iba T., Levy J.H., Warkentin T.E., et al. Scientific, Standardization committee on DIC, the S, Standardization Committee on P, Critical Care of the International Society on T and Haemostasis. Diagnosis and management of sepsis-induced coagulopathy and disseminated intravascular coagulation. J Thromb Haemost. 2019 Nov; 17(11): 1989–94. https://doi.org/10.1111/jth.14578 PMID:31410983
55. Abret N., Britton G.J., Gruber C., et al. The Sinai immunology review project. Immunology of COVID-19: Current state of the science. Immunity. 2020 Jun 16; 52(6): 910–41. https://doi.org/10.1016/j.immuni.2020.05.002 PMID: 32505227
56. de Wit E., van Doremalen N., Falzarano D., Munster V.J. SARS and MERS: Recent insights into emerging coronaviruses. Nat Rev Microbiol. 2016 Aug; 14(8): 523–34. https://doi.org/10.1038/nrmicro.2016.81 PMID: 27344959
57. Ishiguro T., Matsuo K., Fujii S., Takayanagi N. Acute thrombotic vascular events complicating influenza-associated pneumonia. Respir Med Case Rep. 2019 Jun 14; 28: 100884. https://doi.org/10.1016/j.rmcr.2019.100884 PMID: 31245274
58. Risitano A.M., Mastellos D.C., Huber-Lang M., et al. Complement as a target in COVID-19? Nat Rev Immunol. 2020 Jun; 20(6): 343–4. https://doi.org/10.1038/s41577-020-0320-7 PMID: 32327719
Об авторах
Болевич Сергей Бранкович, д-р мед. наук, профессор, заведующий кафедрой патологии человека
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991
Болевич Стефани Сергеевна, ассистент кафедры патофизиологии
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991

