какую роль в структуре белка играют водородные связи сохраняются ли эти связи
Какую роль в структуре белка играют водородные связи сохраняются ли эти связи
Водородные связи, поддерживающие альфа-спирали.
Рис. 1. Все альфа-спирали цепи A. Показаны в модели cartoons.
Водородные связи играют важнейшую роль в поддержании вторичной структуры белка. При образовании этого вида связи атом водорода обобществляется между двумя электроотрицательными атомами (например, кислородами в воде). Водород одной молекулы находится ближе к электроотрицательному атому другой молекулы, чем это может позволить Ван-дер-Ваальсово взаимодействие.
В белках водородные связи образуются между карбонильной группой одного аминокислотного остатка и аминогруппой другого. В альфа-спиралях водородные связи создают каркас, образуясь между i остатком и i+4 остатком.
На рисунке 3 показаны водородные связи, которые создают структуру спирали. Шариковой моделью (cpk 150) показаны атомы, участвующие в образовании этих водородных связей. Связь образуется между килородом карбонильной группы и водородом аминогруппы. Тонкой проволочной моделью (wireframe) показаны радикалы. Видно, что они не образуют остовных водородных связей.
Рис. 3. Альфа спираль, образованная остатками 67-84. Остовные водородные связи.
Также белки с похожей укладкой легко найти в базе данных PDB по запросу Flavodoxin.
Водородные связи, поддерживающие бета-листы.
Рис. 4. Бета-лист цепи A белка с идентификатором 3GL3. Номерами 1-7 обозначены тяжи, составляющие лист. Также обозначены первая и последняя аминокислота, входящие в состав листа (39 [ALA] и 149 [VAL] соответственно).
Структура бета-листа также поддерживается водородными связями. На рисунке 5 в шариковой модели (cpk 150) показаны атомы, между которыми образуется водородная связь (кислород карбонильной группы и водород аминогруппы).
Рис. 5. Бета-лист цепи А. Показаны 7 тяжей и водородные связи, которые держат их вместе.
Общее количество водородных связей, которые поддерживают вторичную структуру альфа-спиралей и бета-листов можно определить с помощью Jmol:
Водородные связи в бета-шпильках и бета-поворотах.
Стоит также отметить, что бета-поворот очень часто связывает антипараллельные бета-тяжи или бета-шпильки.
Водородные связи образуются не только для поддержания альфа-спиралей и бета-листов. Они могут образовываться в глобуле белка и между участками первичной структуру или связывать между собой разные участки, формирующие третичную структуру. Такие водородные связи также можно вычислить с помощью Jmol. В нашем случае их 40.
Рис. 7. Водородная связь между остатками [111] ALA и [113] PHE из цепи C. Показаны донор, акцептор и длина связи.
В какой структуре белка присутствуют водородные связи?
Вы будете перенаправлены на Автор24
Белок – это органическое вещество, которое имеет характерные черты строения и выполняет определенные функции в организме.
Структура белка
Белки содержатся внутри всех клеток живых организмов, выполняя строительную и энергетическую функции. Также к основным функциям белков относят катализ химических реакций и ферментативную регуляцию жизнедеятельности.
В организме белки могут иметь несколько типов структур, а именно:
Любая структура белка подвержена процессу денатурации, ренатурация (восстановление) характерна лишь для второй, третьей, четвертой структур.
Для того, чтобы понять, как именно структура белка влияет на его свойства необходимо обращать внимание на химическую организацию данной молекулы, а также процесс ее создания или распада.
Что касается вторичной структуры белка, то основную роль в ее формировании играют водородные связи. Именно они позволяют белковой структуре конформироваться таким образом, чтобы форма белковой молекулы становилась спиральной.
Спираль – это наиболее высокоорганизованный тип конформации отдельной белковой молекулы или полипептидной цепи.
Водородная связь в структуре белка и в других веществах
Такая спираль построена на пространственном расположении следующих атомов:
Наиболее устойчивым типом спирали является a – спираль. В такой структуре аминокислотные остатки направлены наружу от оси спирали, а группы С = 0 одного витка спирали связаны с группами Н—N следующего витка водородными связями. Водородные связи также образуются между сильно электроотрицательными атомами. Примерами могут служить атомы P или O. У них наблюдается небольшой локальный избыток положительного заряда. Этот тип водородных связей имеет в основном электростатическое происхождение и зависит от способности двух атомов к теснейшему сближению между собой.
Готовые работы на аналогичную тему
Водородная связь в белке играет очень важную роль. Возникая между атомом кислорода и карбонильной группой, а также атомом водорода и аминогруппой они принадлежат к полипептидной цепи. Водородная связь имеет частично двоесвязный характер и обеспечивает плоскость пептидного звена и делает атом кислорода несколько отрицательным.
Атом азота в свою очередь становится несколько положительным. Такая полярность создает благоприятные условия для образования водородной связи. Такие межмолекулярные связи имеют меньшую степень силы, но существенно влияют на скорость протекания химической реакции.
Для того, чтобы понять, как именно водородная связь удерживает молекулу белка, необходимо отметить ее особенности, роль, а также структурное начало в молекулах других веществ. Чаще всего водородная связь отмечается в молекулах: спиртов, карбоновых кислот, углеводах и пр.
Водородная связь также может быть представлена в молекулах спиртов R—ОН и карбоновых кислот RCOOH. При этом подобная водородная связь признается ассоциированной. В связи с этим спирты обладают достаточно высокой температурой кипения и растворимости по сравнению с теми же белками, в которых присутствует водородная связь.
Также понижение растворимости спиртов объясняется тем, что увеличение углеводородного радикала в молекуле спирта ведет к повышению трудности для карбоксильной группы в контексте удержания молекулы воды за счет образования водородных связей.
Также водородная связь может появляться при распаде молекул углевода по оси.
Огромную роль играют так называемые водородные связи, которые определяют специфические свойства белков или нуклеиновых кислот. Непрочность межмолекулярных связей приводит к колебанию свойств белковых молекул. Белки являются полимерами аминокислот. В свою очередь фибриллярные белки входят в структурный материал волос, ногтей, сухожилий и мышц. Водородные связи сворачивают белковую молекулу в спираль, но глобулярные белки также могут принимать вид листов. В дальнейшем такая структура белковой молекулы может образовывать многократные изгибы и сворачиваться в компактные, изолированные молекулы.
Белки волос и шерсти имеют вторичную структуру в виде a – спирали, многократно скрученной с друг другом в многожильные тяжи, нити которых видны глазом. Вторичная структура белка шерсти вытянута во всю длину, но не скручена в спираль. В молекуле миоглобина аминокислоты белковой цепи свернуты в восемь витков а-спирали, которые в свою очередь свернуты так, что в результате получается компактная молекула.
В белках водородные связи могут быть внутриклеточными и межцепочными. Внутрицепочные водородные связи стабилизируют спиральные и складчатые структуры. Наличие большого количества водородных связей позволяет стабилизировать полипептидную цепь и сделать возможным образование спирали. Один виток такой спирали включает около 3, 6 единиц аминокислотных остатков.
Следует отметить тот факт, что знание порядка расположения аминокислот в молекуле еще не дает полного представления о том, какую организацию имеет белковая молекула. Даже осторожное нагревание белков нередко утрачивают свои свойства и в природном состоянии происходит денатурация белка. Причем денатурация не всегда сопровождается расщеплением полипептидной цепи, чтобы ее расщепить требуются гораздо более жесткие условия. Следовательно, цепь образует какую – либо определенную структуру под воздействием слабых вторичных связей.
Такая вторичная связь обычно формируется при участии атома водорода, который находится между атомами азота и кислорода. Такая водородная связь, как правило, в двадцать раз слабее обычной валентной связи.
Как и чем можно объяснить образование водородных связей? Объяснение
Содержание:
Молекулы внутри вещества взаимодействуют друг с другом. Это осуществляется с помощью межмолекулярных взаимодействий, возникающих среди нейтральных молекул без образования ковалентных связей. К ним относятся водородные связи, которые также могут быть представителями внутримолекулярных взаимодействий.
Что такое водородные связи?
Водородная связь – связь, которая формируется между водородом и молекулами с сильнополярными связями (H-F, H-O, H-N). Она обеспечивает дополнительные межмолекулярные силы притяжения и увеличивает устойчивость вещества. Обозначается точками: Н ··· O.
Создание водородной связи отличается от других связей. Она формируется одновременно по обменному и донорно-акцепторному механизму. Роль донора играет электроотрицательный элемент, а акцептора – водород. Чем выше электроотрицательность, тем больше устойчивость вещества.
Водородная связь свойственна для многих веществ:
Образованием водородных связей можно объяснить изменение свойств веществ. Например, она повышает температуру кипения и плавления.
Биологическая роль водородных связей
Полимерные цепи с помощью водородных связей формируют объемные структуры, которым характерна высокая биологическая активность. Химические взаимодействия возникают из-за электростатических взаимоотношений разноименных зарядов частиц в веществе. Разрыв водородных связей в белках или нуклеиновых кислотах лишает нативных свойств.
Многие полимеры укреплены с помощью водородных связей. В нейлоне они играют главную роль при кристаллизации материала. Также они присутствуют в древесине, хлопке, льне, целлюлозе и других соединениях.
В какой структуре белка появляются водородные связи?
Водородные связи укрепляют белки и нуклеиновые кислоты во вторичной и третичной структурах. Они позволяют макромолекулам принимать определенную форму. Биологическое значение водородной связи заключается в образовании спиральных структур нуклеиновой кислоты ДНК, которая обеспечивается попарным расположением нуклеотидов.
В белках есть два варианта образования связей между:
Водородные связи формируются с помощью ван-дер-ваальсовых сил разноименных полюсов диполя. Первичная структура белков образуется с помощью пептидных связей. Пространственная структура основывается на водородных и ионных связях, ван-дер-ваальсовых силах, гидрофобных взаимодействиях. Водородные связи пептидных групп образуют вторичную структуру белков. Формирование третичной и четвертичной структур осуществляется водородными связями, образующимися между радикалами полярных аминокислот, ионными взаимодействиями, ван-дер-ваальсовыми силами, гидрофобными взаимодействиями.
§ 6. Водородная химическая связь (окончание)
Необратимая денатурация белка вам хорошо известна по процессу варки яиц или приготовления мяса, рыбы и других белковых продуктов. О том, какие факторы могут привести к разрушению природной структуры белковых молекул, красноречиво расскажут несложные опыты. Если к раствору белка куриного яйца прилить немного этилового спирта или соли тяжёлого металла (медного купороса, нитрата свинца (II)), то нетрудно будет заметить выпадение осадка вследствие денатурации белка. Аналогичным действием обладает никотин. Может быть, эти опыты помогут вам понять, как губительны такие вредные привычки, как курение и употребление спиртного.
Водородная связь играет важнейшую роль в организации структуры и функционирования таких природных биополимеров, как нуклеиновые кислоты.
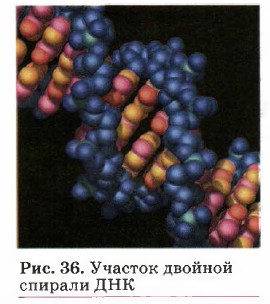
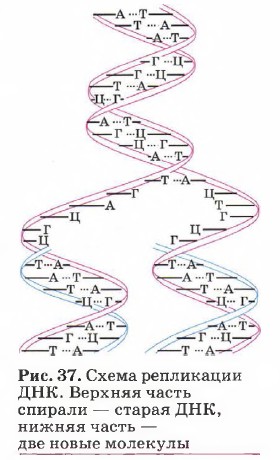
Так, двойная спираль (рис. 36) дезоксирибонуклеиновой кислоты — ДНК (из курса органической химии вспомните, из чего она состоит) — построена в полном соответствии с принципом комплементарности, или дополнительности. Он заключается в том, что напротив аденинового нуклеотида (А) одной полинукле- отидной цепи всегда располагается не любой, а только тиминовый нуклеотид (Т), а напротив гуанинового нуклеотида (Г) — обязательно цитозиновый нуклеотид (Ц) (рис. 37). Всё дело в том, что между этими нуклеотидами возникают водородные связи: между А и Т — две водородные связи, между Ц и Г — три.
Аналогичную роль играют водородные связи и в процессе передачи наследственной информации. Так, при самоудвоении ДНК (этот процесс, как вы помните, называют репликацией) водородные связи разрываются, полинуклеотидные цепи раскручиваются и расходятся. Каждая цепь служит матрицей для образования на ней комплементарной цепи за счёт возникновения новых водородных связей.
Таким образом, после репликации образуются две дочерние молекулы ДНК, в каждой из которых одна спираль была взята из родительской ДНК, а вторая (комплементарная) спираль синтезирована заново (см. рис. 37).
Не менее важны водородные связи и в процессе транскрипции, т. е. переписывания информации о составе синтезируемого впоследствии белка на полинуклеотидную цепь ДНК.
Аналогична роль водородных связей и в трансляции, т. е. передаче информации о последовательности аминокислот в белковой молекуле в рибосомы, где происходит её сборка.
1. Что такое водородная связь? Какую точку зрения — физиков или химиков — вы разделяете по вопросу её природы?
2. Каков механизм образования водородной связи? Какие виды водородной связи вы знаете?
3. Какими особыми свойствами обладают вещества с межмолекулярной водородной связью?
4. Какую роль играет межмолекулярная водородная связь в природе?
5. Какую роль играет внутримолекулярная водородная связь в организации нативной (природной) структуры биополимеров — белков и нуклеиновых кислот?
6. Какую роль играет внутримолекулярная водородная связь в хранении и передаче наследственной информации? При ответе используйте знания по курсу общей биологии, а также консультации учителей биологии и химии.
7. Подготовьте сообщение и презентацию о социальной роли водородных связей, проиллюстрировав примерами. Воспользуйтесь ресурсами Интернета.
8. Подготовьте сообщение об открытии структуры дезоксирибонуклеиновых кислот лауреатами Нобелевской премии Дж. Уотсоном и Ф. Криком, используя ресурсы Интернета.
9. Подготовьте сообщение о химической природе негативных последствий для организма человека курения и употребления алкоголя, используя различные источники информации и ЦОРы.
Фиброин
Свойства
Фиброин является гетеродимером, образованным двумя белковыми цепями. Его первичная структура состоит из повторяющейся аминокислотной последовательности (Gly-Ser-Gly-Ala-Gly-Ala) n.
В свою очередь, повторяющиеся аминокислотные последовательности образуют антипараллельные складчатые β-слои, связанные водородными связями. Эта структура обуславливает высокий предел прочности нитей паутин и шелка. Более прочный, чем кевлар, фиброин вдобавок ещё и высоко эластичен. Эти качества делают его материалом, применяемым в различных областях, включая биомедицину и текстильное производство.
Структуры
Структура белка
По вторичной структуре белка семейство кератинов разделяется на две группы:
Для первичной структуры α-кератинов характерно большое содержание цистеина и множество дисульфидных связей.
В отличие от α-кератинов поперечные дисульфидные связи между соседними полипептидными цепями у β-кератинов отсутствуют. В полипептидной цепи каждый второй элемент — глицин. Характерно повторение последовательности «GSGAGA».
Для α-кератинов основным структурным компонентом являются цилиндрические микрофибриллы диаметром 75 А, состоящие из спирализованных, скрученных попарно протофибрилл.