аспирационный синдром код по мкб 10 у детей
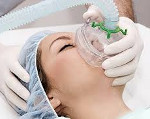
Синдром Мендельсона – острый аспирационный пневмонит, развивающийся вследствие попадания в дыхательные пути кислого желудочного содержимого. Чаще возникает как осложнение анестезиологического пособия. Клиника синдрома Мендельсона разворачивается в считанные часы и включает в себя одышку, лихорадку, дыхательную недостаточность, присоединение бактериальной пневмонии. Синдром диагностируется на основании клинических, аускультативных и рентгенологических данных. Первая помощь предполагает аспирацию содержимого из дыхательных путей, устранение бронхоспазма, перевод больного на ИВЛ, проведение лечебной бронхоскопии. В дальнейшем назначается противоотечная и антибактериальная терапия.
МКБ-10
Общие сведения
Причины
Единственно возможной причиной синдрома Мендельсона является аспирация содержимого желудка, повреждающее действие которого связано с высокой кислотностью химуса. Агрессивный субстрат приводит к сильнейшему химическому ожогу и отеку слизистой дыхательных путей, быстрому разрушению эпителия бронхиол и альвеол и пропотеванию транссудата в альвеолы. Это сопровождается развитием некардиогенного отека легких и респираторного дистресс-синдрома (гипоксемической формы дыхательной недостаточности).
В некоторых случаях вместе с желудочным соком в дыхательные пути могут попадать частички непереваренной пищи, вызывающие механическую закупорку бронхов среднего калибра (асфиктическая форма дыхательной недостаточности). В обоих случаях в конечном итоге развивается бронхиальная обструкция.
Для возникновения клиники синдрома Мендельсона достаточно попадания в респираторный пути даже небольшого объема (20-30 мл) желудочного сока с низким рН. Самые тяжелые повреждения отмечаются при аспирации большого количества кислого содержимого (>0,4 мл/кг), имеющего рН 5.
Факторами, предрасполагающими к аспирации или регургитации содержимого желудка и развитию синдрома Мендельсона, выступают нарушения сознания, обусловленные общим наркозом, алкогольным или наркотическим опьянением, действием седативных препаратов, ЧМТ, комой. Чаще всего синдром Мендельсона возникает как осложнение экстренных хирургических вмешательств (чаще брюшнополостных операций и кесарева сечения), когда не уделяется должного внимания подготовке ЖКТ. Дополнительными факторами риска служат повышение внутрибрюшного давления (у беременных в III триместре, больных ожирением, при парезах кишечника), заболевания ЖКТ (язвенная болезнь желудка и ДПК, эзофагит, гастрит, расширение пищевода, дивертикул пищевода, грыжа пищеводного отверстия диафрагмы).
Симптомы
Клиника синдрома Мендельсона разворачивается очень быстро, в течение нескольких часов. Патологические изменения проходят три фазы: острого ларинго- и бронхиолоспазма, частичного купирования бронхиолоспазма и нарастания острой дыхательной недостаточности.
В первые минуты после аспирации в результате рефлекторного сужения бронхиол возникает кашель, экспираторная одышка, цианоз кожных покровов, тахикардия, снижение АД. Первую фазу синдрома Мендельсона нередко ошибочно принимают за приступ бронхиальной астмы. В легких прослушиваются разнокалиберные влажные и свистящие хрипы; происходит повышение ЦВД, набухание вен шеи. Быстро развивается ОДН I—III ст.; уже на первом этапе возможен летальный исход от асфиксии.
Вторая фаза знаменуется самопроизвольным частичным расширением бронхиол и некоторым клиническим улучшением. Состояние больного временно стабилизируется: уменьшается одышка, снижается давление. Примерно через 48 часов наступает третья фаза синдрома Мендельсона. В этот период быстро нарастают явления бронхиолита и пневмонита, что вызывает новое ухудшение состояния больного и прогрессирование дыхательной недостаточности. Присоединяются бактериальные осложнения – развивается аспирационная пневмония (лихорадка, кашель с мокротой, лейкоцитоз). Летальный исход обычно наступает от отека легких.
Диагностика
Для клинической диагностики синдрома Мендельсона имеет значение характерная триада симптомов (тахипноэ, тахикардия, цианоз), а также невозможность устранить гипоксемию даже при подаче чистого кислорода (данный признак указывает на шунтирование венозной крови). При мониторинге газового состава крови отмечается снижение РаО2 до 35-45 мм рт. ст. Аускультативная картина характеризуется наличием множественных свистящих хрипов (в нижних отделах – крипитирующих хрипов).
При проведении бронхоскопии выявляется отек и гиперемия слизистой, наличие в просвете бронхов аспирированной жидкости, нередко с комочками пищи. На рентгенограммах легких видны очаги гиповентиляции, диффузное затемнение легочных полей («шоковое легкое»). С присоединением вторичной бактериальной пневмонии появляются очаги инфильтрации.
Лечение синдрома Мендельсона
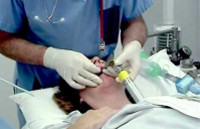
Неотложная помощь должна быть оказана больному сразу после установления факта аспирации желудочного содержимого. В первую очередь необходимо немедленно удалить аспират из полости рта и дыхательных путей с помощью электроотсоса. После этого производится интубация трахеи и перевод больного на ИВЛ в режиме гипервентиляции с ингаляцией 100% кислорода. В дальнейшем выполняется зондовое опорожнение желудка и санационная бронхоскопия: для бронхоальвеолярного лаважа используется стерильный физраствор. Лечение больного синдромом Мендельсона осуществляется в ОРИТ совместно анестезиологами-реаниматологами и пульмонологами.
С целью ликвидации бронхиолоспазма вводится атропин, эуфиллин, преднизолон или дексаметазон, орципреналин. Обязательно производится перкуссионный массаж грудной клетки. Для нейтрализации высокой кислотности осуществляются щелочные ингаляции раствора гидрокарбоната натрия. Проводится инфузия электролитных растворов, глюкозы, свежезамороженной плазмы, альбумина; стимуляция диуреза. Антибиотикотерапия показана для профилактики и лечения аспирационной пневмонии. Экстубация производится после восстановления спонтанного дыхания и самостоятельной способности поддержания адекватного газообмена.
Прогноз и профилактика
Летальные исходы при возникновении синдрома Мендельсона наблюдаются в 60% случаев, а в акушерской практике – более чем в 70% случаев. Чтобы предотвратить это грозное осложнение, перед экстренными операциями необходимо эвакуировать желудочное содержимое с помощью зонда (за исключением тех случаев, когда это противопоказано – например, при желудочном кровотечении). Перед плановыми операциями запрещается прием пищи и жидкости за 10-12 часов до вмешательства, при необходимости назначается прием антацидов, Н2-блокаторов и прокинетиков. Во избежание синдрома Мендельсона необходимо соблюдение правильного алгоритма анестезиологического пособия во время экстренных хирургических вмешательств.
Синдром аспирации мекония у новорожденных
14-16 октября, Алматы, «Атакент»
150 участников из 10 стран. Новинки рынка стоматологии. Цены от производителей
Общая информация
Краткое описание
Российская ассоциация специалистов перинатальной медицины (РАСПМ)
Год утверждения: 2017 (пересмотр каждые 3 года)
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Эпидемиология
Околоплодные воды могут быть окрашены меконием в 8-20% всех родов [1, 2, 8, 9]. Причем после полных 42 недель частота достигает 23-52% [10, 11]. От 2 до 9% новорожденных, у которых воды были окрашены меконием, в последствие отмечается клиническая картина САМ [2, 12, 13]. Около трети новорожденных с САМ требуют интубации трахеи и механической вентиляции легких [13]. Летальность при САМ в связи с тяжелыми повреждениями паренхимы легких и развитием легочной гипертензии может превышать 20%. Другие осложнения, включая СУВ, встречаются у 10-30% детей с САМ [14].
Диагностика
Диагностика
— курение, наркомания (особенно, кокаин) [2].
Комментарии: Необходимо проводить дифференциальный диагноз с врожденной пневмонией.
Дифференциальный диагноз
— Транзиторным тахипноэ новорождённых и другими состояниями, сопровождающимися развитием дыхательной недостаточности в раннем неонатальном периоде.
Лечение
Рекомендуется дифференцированный подход к оказанию помощи в родильном зале новорожденным с околоплодными водами, содержащими меконий [26]. Акушеры должны заранее предупредить врачей-неонатологов, если околоплодные воды окрашены меконием и имеются признаки дистресса плода. Санация ротоглотки после рождения головки плода не снижает вероятности развития респираторного дистресс-синдрома или клинически выраженного синдрома мекониальной аспирации, включая подгруппы, где имело место наличие густого мекония, отмечались признаки дистресса у плода или родоразрешение выполнялось абдоминальным путем [19].
Комментарии: В случае отсутствия лаважа желудка в родильном зале при наличии мекония в околоплодных водах не зарегистрировано вторичных осложнений, связанных с регургитацией и/или аспирацией мекониального желудочного содержимого [29]. В то же время лаваж желудка рассматривается как потенциально опасная манипуляция, поскольку введение рото- или назогастрального зонда в родильном зале нередко сопровождается развитием апноэ и/или брадикардией [30].
Синдром аспирации мекония у новорожденных. Клинические рекомендации.
Синдром аспирации мекония у новорожденных
Оглавление
Ключевые слова
синдром мекониальной аспирации
синдром аспирации мекония
персистирующая легочная гипертензия
синдром «утечки воздуха»
Список сокращений
ИВЛ – искусственная вентиляция легких
МАР – среднее давление в дыхательных путях
РКИ — рандомизированные контролируемые исследования
САМ – синдром аспирации мекония
СДР, РДС — синдром дыхательных расстройств
СРАР – continuous positive airway pressure / метод респираторной терапии – постоянное давление в дыхательных путях
УЗИ — ультразвуковое исследование
ЭТТ – эндотрахеальная трубка
f — частота аппаратных вдохов, в минуту
fO2 — содержание кислорода в воздушной смеси
Peep – пиковое давление в конце выдоха
Pip – пиковое давление на вдохе
раО2 – концентрация кислорода в крови
Термины и определения
Синдром аспирации мекония – тяжелое расстройство дыхания у новорожденных детей, вызванное попаданием мекония в нижние дыхательные пути.
Сурфактант (в переводе с английского – поверхностно-активное вещество) – смесь поверхностно-активных веществ, выстилающая альвеолы изнутри.
Синдром «утечки воздуха» – тяжелое состояние новорожденных, характеризующееся разрывом альвеол, выходом из них воздуха и его распространение по легким и в другие части организма.
Персистирующая легочная гипертензия – состояние, характеризующееся снижением кровотока в легких новорожденного и появление при этом право-левого сброса крови в результате возврата к констрикции артериол легких или персистирования.
Тахипноэ — учащённое поверхностное дыхание.
1. Краткая информация
1.1 Определение
Синдром аспирации мекония (САМ) – тяжелое расстройство дыхания у новорожденных детей, вызванное попаданием мекония в нижние дыхательные пути.
Синонимы САМ: синдром мекониальной аспирации новорожденных, неонатальная аспирация.
1.2 Этиология и патогенез
САМ чаще наблюдается у переношенных или доношенных новорожденных, которые подверглись внутриутробной антенатальной и/или интранатальной гипоксии и родились в асфиксии, приведшей к спазму сосудов брыжейки, усилению перистальтики кишечника, расслаблению анального сфинктера и пассажу мекония — выходу его в околоплодные воды. Обвитие пуповины вокруг шеи, сдавление ее стимулирует вагусную реакцию и пассаж мекония даже при отсутствии асфиксии.
1.3 Эпидемиология
1.4 Кодирование по МКБ 10
P24.0 – Неонатальная аспирация мекония
1.5 Классификация
Классификация САМ по вариантам течения
Первый вариант — с рождения имеется тяжелая дыхательная недостаточность, приступы вторичной асфиксии, одышки, притупления легочного тона, повышение ригидности грудной клетки, обильные разнокалиберные влажные хрипы в легких.
Классификация САМ по степени тяжести
В зависимости от количества, консистенции аспирированной жидкости, а также от сроков аспирации различают:
Легкая степень – отмечается тахипноэ, проходящее через 42-72 часа. Уровень рСО2 в артериальной крови в пределах нормы, рН крови без изменений. Редко отмечается незначительная гипоксимия, корригируемая ингаляцией кислорода.
Средняя степень – клиника схожа с легкой степенью, но нарастание дыхательной недостаточности происходит быстрее и пик приходится на 24 часа. В артериальной крови отмечается гипоксимия степень, которой не соответствует тяжести легочной патологии (сопоставление с Rg-граммой грудной клетки). Это может говорить о стойкой легочной гипертензии с шунтированием крови справа налево как на уровне открытого артериального протока так и на уровне предсердий (что подтверждается УЗИ сердца с Доплер-эффектом).
Тяжелая степень – дыхательная недостаточность отмечается сразу после рождения или в первые 24 часа жизни. В данном случае отмечается сочетание дыхательного и метаболического ацидоза, которые требуют немедленной коррекции.
При тяжелой степени достаточно часто развитие таких осложнений как напряженный пневмоторакс и практически всегда развитие стойкой легочной гипертензии. Стойкость легочной гипертензии связанна в первую очередь с утолщением стенок сосудов легочных артерий вследствие их чрезмерной гипертрофии и гиперплазии. Впервые о гипертрофии сообщили Siassi и соавт. в 1971 году. В частности, в их исследовании доказывалось, что хроническая гипоксия может вызывать утолщение стенок мелких легочных артерий вследствие гипертрофии гладкой мускулатуры, что в свою очередь приводит к стойкому сужению просвета сосуда. Помимо всего выше перечисленного сейчас установлено, что острая гипоксемия плода вызывает дальнейшее сужение легочных артерий, что в итоге приводит к стойкой легочной гипертензии.
2. Диагностика
2.1 Жалобы и анамнез
Анамнез заключается в выявлении факторов риска, таких как переношенность ребенка, эклампсия беременной, гипертензия беременной, сахарный диабет беременной.
2.2 Физикальное обследование
Рекомендовано на этапе постановки диагноза начать с оценки симптомов дыхательной недостаточности у новорожденного по шкале Даунса (Приложение Г) [1].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b)
Комментарии: Раннее (в течение 2 ч) наблюдается появление симптомов дыхательной недостаточности: тахипноэ, раздувание крыльев носа, втяжения уступчивых мест грудной клетки, цианоз. Увеличение передне-заднего размера грудной клетки.
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b)
Комментарии: При перкуссии выявляют участки притупления, чередующиеся с коробочным звуком. Выслушивается ослабленное или жёсткое дыхание с большим количеством проводных и крепитирующих хрипов. Удлинённый выдох. Тоны сердца приглушены, можно выслушать систолический шум. Из-за нарушения периферического кровотока кожные покровы приобретают мраморный цвет, могут появиться отёки.
2.3 Лабораторная диагностика
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3)
Комментарии: При САМ выявляют резко выраженную гипоксемию и смешанный ацидоз.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3)
Комментарии: Поскольку меконий может усилить рост бактерий и САМ трудно отличить от бактериальной пневмонии.
2.4 Инструментальная диагностика
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1a)
Комментарии: На рентгенограмме легких отмечают сочетание участков апневматоза (крупные, неправильной формы затемнения), отходящих от корней легких, с вкраплениями эмфизематозных областей. Легкие вначале выглядят эмфизематозными, диафрагма уплощена, переднезадний размер грудной клетки увеличен. Для обильной аспирации характерны рентгеновский симптом «снежной бури» и кардиомегалия, развивающийся в первые сутки пневмоторакс.
2.5 Дифференциальная диагностика
При диагностике РДС характерными признаками на рентгеновском снимке являются: диффузное снижение прозрачности легочных полей, ретикулогранулярный рисунок и полоски просветлений в области корня легкого (воздушная бронхограмма).
Диагностика раннего неонатального сепсиса, врожденной пневмонии. Характерны положительные маркеры воспаления, определяемые в динамике в первые 72 часа жизни. Рентгенологически при однородном процессе в легких ранний неонатальный сепсис/пневмония неотличимы от САМ. Однако, если процесс в легких очаговый (инфильтративные тени), то это признак характерен для инфекционного процесса и не характерен для САМ. При САМ на рентгенограмме органов грудной клетки инфильтративные тени перемежаются эмфизематозными изменениями, ателектазами, (возможны пневмомедиастинум и пневмоторакс).
Диагностика персистирующей легочной гипертензии новорожденных. На рентгеновском снимке органов грудной клетки отсутствуют характерные для САМ изменения. При эхокардиографическом исследовании выявляется право-левый сброс и признаки легочной гипертензии.
3. Лечение
3.1 Консервативное лечение
Сурфактантная терапия
При подтверждении САМ рекомендуется применение сурфактантной терапии [3].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3)
Комментарии: Способ сурфактант-терапии состоит в проведении лаважа трахеобронхиального дерева разведенным препаратом Порактант альфа**. Для этого препарат (75 мг во флаконе) разводят в 2,5 мл физиологического раствора, согласно инструкции фирмы производителя. Из этой эмульсии берут 0,5 мл и дополнительно разводят физиологическим раствором до 5,0 мл (осторожно перемешивая и не встряхивая) и проводят лаваж трахеобронхиального дерева дробно двумя-тремя порциями. Оставшиеся 2,0 мл (60 мг) эмульсии вводят попеременно по 1,0 мл в левый и в правый бронх болюсно через санационный катетер. Второй флакон препарата вводят микроструйно, так что общая доза составляла 50 мг / кг. Лечение синдрома аспирации мекония тяжелой степени путем проведения сурфактант-терапии в виде лаважа трахеобронхиального дерева разведенным Порактантом альфа** с последующим введением небольшой дозы препарата позволяет достоверно уменьшить время достижения нетоксической концентрации кислорода в подаваемой газовой смеси, время нахождения детей на искусственной вентиляции легких и в отделении реанимации и интенсивной терапии новорожденных. Известно, что меконий эффективно связывается с легочным сурфактантом за счет химических и физических механизмов взаимодействия и инактивирует его. При этом критерием инактивации является потеря сурфактантом свойства эффективно снижать поверхностное натяжение на границе раздела фаз воздух — вода. Меконий, сорбированный на частицах экзогенно введенного сурфактанта, удаляется при лаваже, а следующее за ним введение терапевтической дозы Порактанта альфа** 50 мг/кг выполняет роль заместительной терапии, приводя к повышению растяжимости легких, устранению ателектазов и улучшению вентиляционно-перфузионного отношения. Эффект терапии проявлялся улучшением аускультативной картины в легких и положительной динамикой на рентгенограммах грудной клетки.
Седация и миорелаксация
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2a)
Антибактериальная терапия
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b)
Комментарии: Антибактериальная терапия показана при аспирации мекония, так как он способствует росту бактерий. Начинают с цефалоспоринов и аминогликозидов. По результатам посевов из трахеи проводят смену антибактериальной терапии.
Респираторная терапия новорожденных с САМ
Помощь новорожденному с САМ в родильном зале
Уровень убедительности рекомендаций В (уровень достоверности доказательств–2b)
Комментарии: Широкое использование в предыдущие годы санации носо- и ротоглотки плода до рождения плечиков с профилактической целью не подтвердило своей эффективности, поэтому в настоящее время эта манипуляция не рекомендована для рутинного применения. Санация носо- и ротоглотки ребенка должна быть проведена после перемещения ребенка на реанимационный столик. При этом, несмотря на то, что околоплодные воды содержат меконий, если у ребенка сразу после рождения отмечается хороший мышечный тонус, активное самостоятельное дыхание или громкий крик, то санация трахеи не показана.
Если околоплодные воды содержат меконий и у ребенка отмечается сниженный мышечный тонус, неэффективное или ослабленное самостоятельное дыхание, сразу после рождения необходимо провести интубацию трахеи с последующей санацией через эндотрахеальную трубку. Следует обратить особое внимание на то, что санация проводится путем подключения шланга аспиратора через Т-образный коннектор или мекониальный аспиратор непосредственно к эндотрахеальной трубке. Санация производится до полной аспирации содержимого трахеи. Если эндотрахеальная трубка блокирована меконием, следует удалить эту трубку, повторно интубировать трахею ребенка и продолжить санацию. Использование с этой целью аспирационных катетеров, диаметр которых всегда меньше, чем диаметр эндотрахеальной трубки, не допускается. Если на фоне санации отмечается нарастание брадикардии менее 80уд/мин, санацию следует прекратить и начать искусственную вентиляцию легких (ИВЛ) до повышения частоты сердечных сокращений (ЧСС) более 100 уд/мин. Вопрос о необходимости повторной санации трахеи решается после восстановления сердечной деятельности ребенка в индивидуальном порядке.
Использование ИВЛ в условиях родильного зала
Рекомендуется начать ИВЛ сразу после извлечения ребенка из матери [2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2a)
Комментарии: Использование саморасправляющегося мешка у новорожденных:
Следует использовать саморасправляющийся мешок объемом не более 240 мл. Такой размер более чем достаточен для проведения вентиляции легких у новорожденных. После сжатия мешок расправляется самостоятельно за счет своих эластических свойств, независимо от источника газовой смеси, что делает использование этого устройства удобным и простым. Однако, для проведения ИВЛ воздушно-кислородной смесью, необходимо подключить мешок к источнику кислорода и установить скорость потока 8 л/мин. Такая скорость позволяет добиться концентрации в дыхательной смеси около 40%. Для создания более высокой концентрации кислорода (80-90%) к саморасправляющемуся мешку требуется подключить дополнительно кислородный резервуар. Следует помнить, что при проведении ИВЛ с помощью саморасправляющегося мешка трудно поддерживать одинаковое пиковое давление от вдоха к вдоху. Поэтому целесообразно использовать манометр, подключенный к мешку. Максимальное пиковое давление ограничено клапаном сброса избыточного давления, который срабатывает при превышении около 40 смН2O. Для создания большего давления на вдохе следует заблокировать пальцем клапан сброса давления. Иногда это может потребоваться при неэффективности первых принудительных вдохов в процессе масочной ИВЛ у крупных доношенных новорожденных. При использовании саморасправляющегося мешка невозможно создать положительное давление в конце выдоха, не подключив дополнительно клапан, создающий давление в конце выдоха. Использование саморасправляющегося мешка не позволяет обеспечить раздувание легких длительностью более одной секунды.
Использование аппарата ИВЛ с Т-коннектором:
В аппаратах ИВЛ с Т-коннектором газовая смесь поступает в маску или интубационную трубку через контур, подключенный к смесителю сжатого воздуха и кислорода и к манометру. Вентиляция обеспечивается благодаря окклюзии пальцем выходной трубки Т-коннектора, осуществляемой с определенной периодичностью. Аппарат позволяет создавать и регулировать необходимое давление, как на вдохе, так и при помощи изменения диаметра отверстия выходной трубки на выдохе (СРАР, PEEP). Время вдоха регулируется путем изменения длительности окклюзии пальцем выходной трубки Т-коннектора. Для функционирования устройства требуется подключение его к источнику газовой смеси. Скорость потока устанавливается 8 л/мин. По сравнению с саморасправляющимся и поточнорасправляющимся мешками устройства с Т-коннектором являются наиболее удобными для проведения ИВЛ у новорожденных детей в родильном зале.
ИВЛ как метод респираторной терапии новорожденных с САМ
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b)
Комментарии: Умеренную гипоксемию можно корригировать ингаляцией увлажненного кислорода через кислородную палатку. Эффект от применения СРАР у новорождённых с САМ непредсказуем и поэтому его не рекомендуют для рутинного использования.