когда и каким образом в клетке бактерий разрушается мрнк
Что необходимо знать о мРНК-вакцинах: 5 позиций
В результате беспрецедентной скорости в разработке новых вакцин, миру были представлены первые клинически одобренные мРНК-вакцины
В результате беспрецедентной скорости в разработке новых вакцин, миру были представлены первые клинически одобренные мРНК-вакцины для борьбы с пандемией Covid-19 – одна из них произведена Pfizer и BioNTech, другая – компанией Moderna. Испытания показали эффективность этих вакцин на уровне не менее чем 94%.
1. Технология мРНК вакцин не так молода, как кажется
Классический механизм работы вакцин (например, против полиомиелита и гриппа) заключается в презентации иммунной системе инактивированных частиц вируса. Другие вакцины (например, против гепатита B) используют отдельно взятый белок, являющийся частью инфекционного агента, чтобы вызвать схожий иммунный ответ.
мРНК-вакцины работают по другому принципу, «обманывая» иммунную систему таким образом, что РНК (в основном матричная мРНК) кодирует белок, который продуцируется в клетке путем трансляции и представляется иммунной системе; он действует как антиген. Иммунная система учится избирательно бороться с клетками, экспрессирующими такие антигены, такими как клетки-хозяева, инфицированные вирусами, или опухолевые клетки.
Хотя вакцины от Pfizer/BioNTech и Moderna – первые препараты, одобренные в клинической практике, сама технология мРНК-вакцин существует относительно давно. Первые испытания в онкологии с использованием схожих технологий берут свое начало еще в 2011 году.
2. мРНК-вакцины не изменяют ДНК
Существуют абсолютно необоснованные опасения, что мРНК-вакцины способны изменять ДНК. На самом же деле мРНК не входит в ядро клетки, а после своего введения биодеградирует в течение нескольких дней. Именно поэтому для формирования полноценного иммунного ответа необходимо 2 инъекции препарата.
3. мРНК-вакцины имеют высокую специфичность
Вирус SARS-CoV-2 имеет достаточно сложную структуру и его различные части стимулируют иммунную систему на образование нейтрализующих антител, которые не всегда способны эффективно элиминировать инфекцию. мРНК-вакцины стимулируют иммунный ответ к спайк-белку вируса, являющегося только частью вирусной мембраны.
4. Разработчики и эксперты не «срезали углы» во время клинических испытаний
Испытания вакцин начались с доклинической фазы, проводимой на животных, а затем постепенно переходили на 1-ую, 2-ую и 3-ю фазы. Например, 3-я фаза вакцины от Pfizer/BioNTech включает более 40 000 человек, исследования эффективности и безопасности будут продлжаться следующие 2 года.
Основные проблемы, связанные с использованием вакцины, обычно возникают в первые 2 месяца. Тем не менее, не исключены редкие побочные эффекты на больших выборках в миллионы людей, поэтому за вакцинированными необходимо пристальное наблюдение, особенно с учетом инновационной природы технологии.
5. Вакцина запускает воспалительные реакции
Частично вакцина работает путем индуцирования локальных иммунных реакций, поэтому воспалительные признаки в месте инъекции и небольшой дискомфорт в первые дни – вполне нормальное явление.
Как избавиться от РНК за несколько минут
Как избавиться от РНК за несколько минут
Модель «протекающего ведра». Уровень РНК в клетке (количество воды в ведре) зависит и от скорости ее распада (скорости вытекания воды из ведра), и от интенсивности транскрипции (потока воды в кране).
Автор
Редакторы
Статья на конкурс «био/мол/текст»: РНК — рибонуклеиновая кислота — это один из основных типов молекул в клетке. Различных видов РНК существует огромное количество, и их синтез идет постоянно. Но если бы РНК только накапливалась, то очень скоро она бы заполнила собой всю клетку. Поэтому параллельно с синтезом в клетке постоянно происходит противоположный процесс — распад РНК. Причем процесс этот сложный и тщательно регулируемый. Именно о нем и пойдет речь в статье.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
РНК — неотъемлемый участник большинства клеточных процессов. Прежде всего, РНК обеспечивают трансляцию: с матричных РНК (мРНК) считываются последовательности аминокислот в белке, транспортные РНК (тРНК) «поставляют» аминокислоты к месту синтеза, а саму реакцию осуществляют рибосомы, основной компонент которых, — рибосомные РНК (рРНК). Но роль РНК не ограничивается этими наиболее известными функциями. В последующие годы после открытия первых некодирующих РНК (тех, которые не кодируют белок, то есть всех не-мРНК) — рРНК и тРНК, — стало появляться множество новых данных об участии некодирующих РНК в самых разнообразных клеточных процессах. Оказалось, что РНК участвуют в таких важнейших клеточных процессах, как репликация (Y РНК), транскрипция (U1 РНК, 7SK РНК), сплайсинг (малые ядерные РНК U1, U2, U4, U5 и U6), процессинг (ряд малых ядрышковых РНК), клеточный транспорт (7SL РНК). Не так давно открытые микро-РНК и малые интерферирующие РНК участвуют в регуляции экспрессии генов и помогают в защите клетки от чужеродного генетического материала [2–5]. А некоторые молекулы РНК — рибозимы — даже могут осуществлять биохимические реакции, т.е. выступать в роли ферментов, что всегда считалось прерогативой белков. Так что, нет такой сферы клеточной деятельности, в которую не проникли молекулы РНК.
Как РНК образуются в клетке, изучено довольно хорошо. Но как эти молекулы разрушаются? И когда? Ведь некоторые РНК живут в клетке очень долго, другие же разрушаются за несколько минут. От чего это зависит?
Общие правила распада РНК
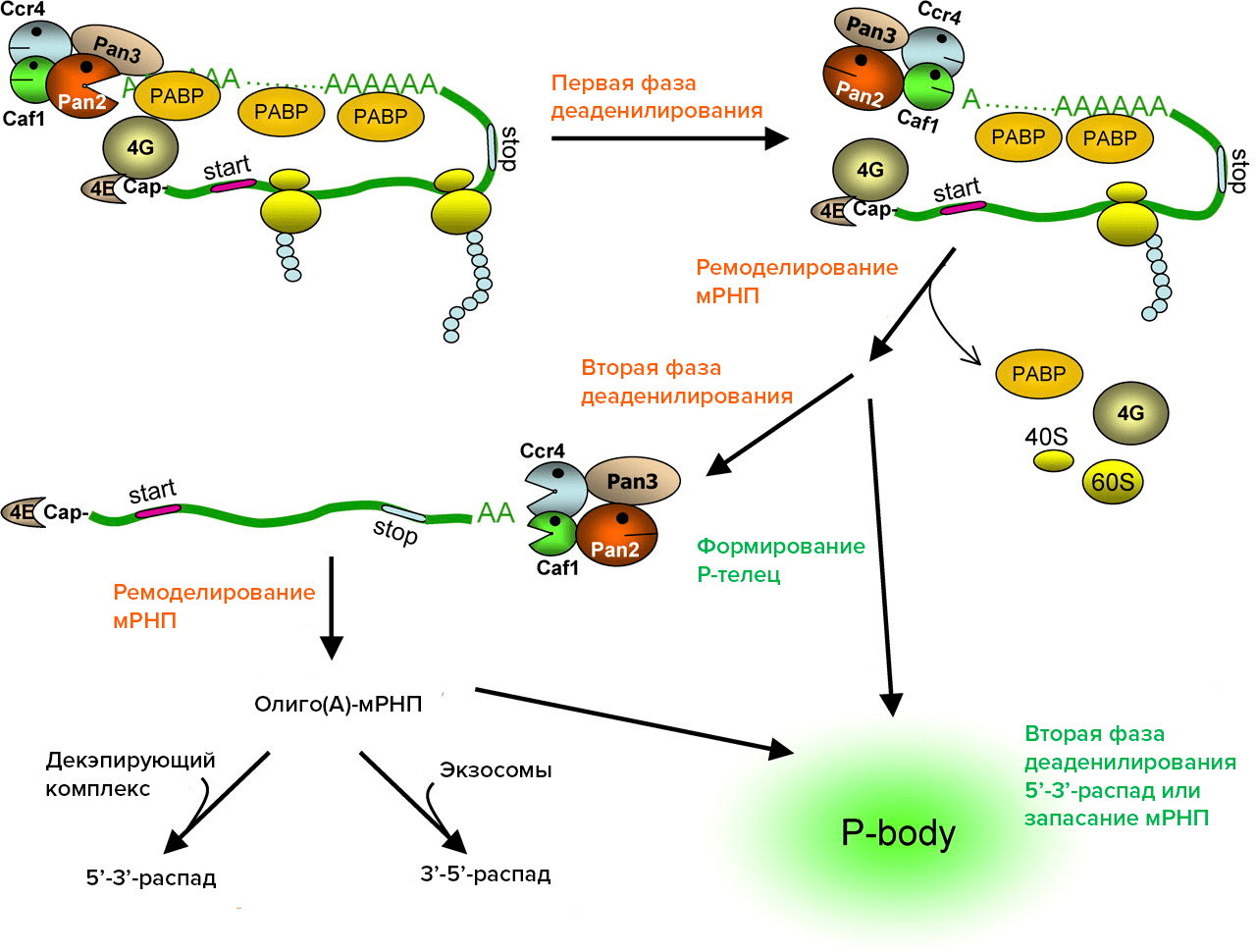
Рассмотрим сначала самый известный класс РНК — мРНК. У эукариот большинство мРНК имеет на 3’-конце «хвост» из многочисленных остатков аденина (обозначается как поли(А)). Присоединение поли(А)-хвоста к мРНК происходит в ядре с помощью определенного фермента. Для того, чтобы произошло полиаденилирование, необходимо, чтобы в составе мРНК был специальный сигнал — AAUAAA. В клетках млекопитающих поли(А)-хвост, достигающий длины 250 нуклеотидов, взаимодействует с поли(А)-связывающими белками (poly-A-binding protein, PABP). Поли(А)-хвост в комплексе с PABP очень важен: он участвует в транспорте мРНК из ядра в цитоплазму, в трансляции и защищает мРНК от распада, т.е. придает ей стабильность. Один белок PABP связывается с 12 аденозинами, но закрывает при этом 25–27 оснований. В цитоплазме плавают специальные ферменты — деаденилазы, — которые откусывают кусочки от поли(А)-хвостов. Если у мРНК поли(А)-хвост сократился до длины, недостаточной для связывания хотя бы одной молекулы PABP, то она подвергается быстрой деградации. Соответственно, первый шаг на пути деградации большинства мРНК — разрушение поли(А)-хвоста [6], [7].
Рисунок 1. Этапы распада мРНК в клетках млекопитающих. Деаденилирование осуществляется с помощью ферментов CCR4, Caf1, Pan2-3. После первой фазы деаденилирования поли(А)-хвост мРНК укорачивается до размеров небольшого олиго(А)-участка, мРНК перестает транслироваться (теряет PABP, факторы инициации трансляции, рибосомы). На второй фазе деаденилирования мРНК полностью теряет поли(А), после чего подвергается декэпированию и деградации с 5’-конца или с 3’-конца с помощью экзосомы или же отправляется в Р-тельце для временного хранения в нетранслируемом состоянии.
В цитоплазме почти все факторы, участвующие в распаде РНК (ферменты, разрушающие поли(А)-хвост, отрезающие кэп, различные экзонуклеазы), сконцентрированы в специальных гранулах — Р-тельцах. По сути, они представляют собой скопления белков и недораспавшихся РНК. Согласно последним данным, в Р-тельцах происходит не только разрушение мРНК, но также и их накопление, и временное хранение. Такая изоляция в Р-тельцах защищает клетку от случайной трансляции не успевших деградировать молекул. Таким образом, мРНК в цитоплазме может пребывать в двух состояниях: в транслируемом, и тогда она связана в комплексы с рибосомами, и нетранслируемом — в составе Р-телец [9], [10].
Существует большое количество механизмов распада РНК, характерных для определенных обстоятельств или специфических молекул РНК. Некоторые из них будут описаны ниже. Однако стоит подчеркнуть, что несмотря на отличия на начальных этапах процесса, в любом случае дело заканчивается разрушением РНК с помощью все тех же белков — экзонуклеаз или экзосом, а в случае мРНК еще и ферментов, удаляющих кэп, и избавляющих РНК от поли(А)-хвоста. Далее все эти белки я буду называть «факторами деградации».
Хвост нужен для деградации
В клетках прокариот разрушение и мРНК, и стабильных рРНК и тРНК происходит сходным образом. Принципиальное отличие от эукариот заключается в том, что у прокариот деградация РНК всегда начинается с внутреннего разреза молекулы эндонуклеазой, и только потом получившиеся фрагменты РНК деградируют до отдельных нуклеотидов с помощью экзонуклеаз. Что самое интересное, РНК прокариот перед деградацией приобретают поли(А)-хвосты, хотя раньше считалось, что полиаденилированные РНК есть только у эукариот. Прокариотам поли(А)-хвост нужен исключительно как платформа, с которой связываются экзонуклеазы перед началом деградации РНК. Учитывая этот факт, можно предположить, что и у эукариот поли(А)-хвост — это затравка для распада мРНК, которая в процессе эволюции приобрела дополнительные, теперь уже неотъемлемые, защитные и транспортные функции [6], [11].
У мРНК гистонов другие хвосты
Следует отдельно сказать об мРНК гистонов. Гистоны — белки, обеспечивающие компактную упаковку ДНК в хромосомы. Важно, что в клетке они транслируются только во время S-фазы клеточного цикла, когда происходит репликация ДНК: гистоны нужны для упаковки вновь синтезированной ДНК. После этого их мРНК необходимо разрушить. Регуляция синтеза гистонов и распада их мРНК очень важна, т.к. любые нарушения упаковки ДНК в хромосомы могут иметь катастрофические последствия для клетки. Поэтому для деградации мРНК гистонов существует независимый от всех других РНК механизм, который включается исключительно во время S-фазы.
В клетках эукариот мРНК гистонов уникальны, потому что они не имеют интронов (участков РНК, которые вырезаются из нее в процессе сплайсинга — одного из важнейших этапов созревания мРНК у эукариот) и поли(А)-хвоста. Отсутствие поли(А)-хвоста, видимо, тоже связано со спецификой созревания этих мРНК: у них нет сигнала полиаденилирования, и их 3’-конец образуется просто благодаря эндонуклеотическому разрезу. Но как же происходит распад, если у мРНК гистонов отсутствует платформа в виде поли(А)-хвоста для привлечения необходимых ферментов? Эта задача решается очень просто: вместо поли(А)-хвоста на конце мРНК синтезируется поли(U)-хвост, причем происходит это уже не в ядре, как у остальных мРНК, а в цитоплазме. Зрелый 3’-конец мРНК гистонов состоит из так называемой стебельно-петлевой структуры и АСС-хвостика. Эта структура выполняет роль стабилизатора — как поли(А)-хвост для других мРНК. С ней взаимодействует белок, который привлекает ферменты, синтезирующие поли(U)-хвост на конце мРНК. А дальше распад мРНК гистонов проходит уже без особенностей. То есть, у мРНК гистонов поли(U)-хвосты выполняют ту же функцию при распаде РНК, что и поли(А)-хвосты у прокариот [6].
Контроль качества
Зачем же все-таки нужно уничтожать РНК? Прежде всего, с помощью механизмов распада клетка избавляется от «испорченных» РНК. Ошибка в одной мРНК в конечном счете приводит к синтезу многих неправильных белковых молекул, а те, в свою очередь, тоже не могут выполнять свою работу. Нарушения в некодирующих РНК (рРНК, тРНК и др.) не менее опасны: часто такие молекулы просто перестают нормально функционировать. Поэтому в клетке происходит постоянный контроль качества РНК от этапа синтеза молекул до их созревания и дальнейшей работы.
Куда деть непригодные матричные РНК?
Далеко не все из вновь синтезированных в ядре мРНК функционально пригодны. Многие из них с самого начала содержат ошибки. От таких «неправильных» мРНК необходимо избавляться. Первоочередная задача — определить, где произошла ошибка. Удобнее всего это делать во время синтеза белка: первый раунд трансляции, когда с данной мРНК впервые синтезируется белок, как бы служит проверкой мРНК на качество.
Один из вариантов мутаций, которые могут возникать при синтезе мРНК — появление терминирующего кодона в неположенном месте. Это происходит, если при синтезе мРНК полимераза вместо нужного нуклеотида вставила другой, в результате чего вместо значащего триплета появляется стоп-кодон. С таким кодоном связываются факторы терминации, и синтез белка заканчивается раньше времени. Чтобы избежать накопления таких «обрубленных» белков, существует NMD (nonsense-mediated decay) — деградация, обусловленная появлением преждевременного стоп-кодона.
Основная роль в этом механизме принадлежит маркерным белкам, которые расположены на мРНК выше, чем нормальный терминирующий кодон. Именно взаимодействие этих маркеров с аппаратом терминации трансляции и приводит к запуску процесса распада мРНК. В этом механизме ключевую роль играет первый раунд трансляции: если после него мРНК не разрушилась, то она приобретает «иммунитет» к NMD, потому что маркерные белки при первом прохождении рибосомы удаляются (рис. 2) [12], [13].
Рисунок 2. Система nonsense-mediated decay (NMD). В норме рибосома при синтезе белка сдвигает маркерные белки, и распада мРНК не происходит (слева). Если же мРНК содержит нонсенс-мутацию, то к тому моменту, когда рибосома дойдет до ложного стоп-кодона, и с ним свяжутся факторы терминации трансляции, маркерные белки будут все еще связаны с мРНК (справа).
Иногда из-за ошибок синтеза мРНК она, наоборот, теряет стоп-кодон, а не получает лишний. В этом случае вместо того, чтобы остановиться в нужном месте, рибосома продолжает синтез за пределы транслируемой области, и белок получается удлиненным. На этот случай у некоторых мРНК существует специальный механизм деградации — REMD (ribosome extension-mediated decay). Принцип этого механизма похож на предыдущий. С нетранслируемой областью мРНК связан комплекс белков. Если к концу синтеза он остается на своем месте, мРНК продолжает функционировать как матрица в последующих раундах трансляции. Сдвигание же этого комплекса (из-за прохождения рибосомы) сигнализирует о том, что от мРНК надо избавиться [14].
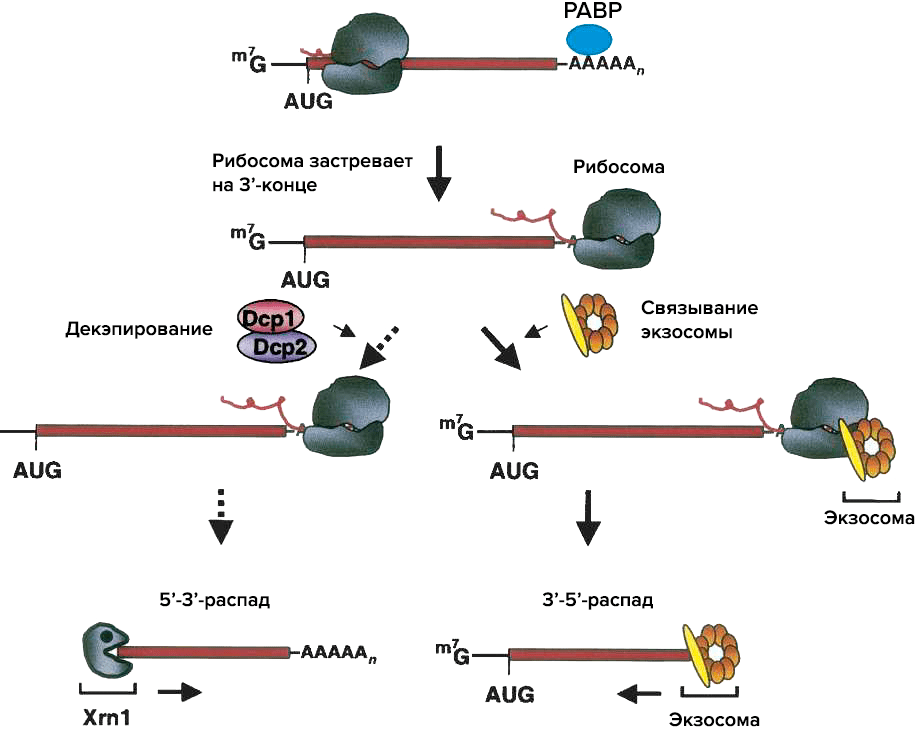
мРНК может потерять стоп-кодон и по другой причине — если ее синтез был прерван. Такая обрубленная мРНК все равно может участвовать в трансляции, но долго прожить ей не удается благодаря механизму NSD (nonstop decay). Поскольку нормальной терминации на недосинтезированной мРНК произойти не может, то, дойдя до ее конца, рибосома просто останавливается. К такой «повисшей» на краю мРНК рибосоме тут же подскакивают определенные белки, связываются с ней и привлекают факторы деградации (рис. 3) [15].
Рисунок 3. Схема non-stop decay (NSD)
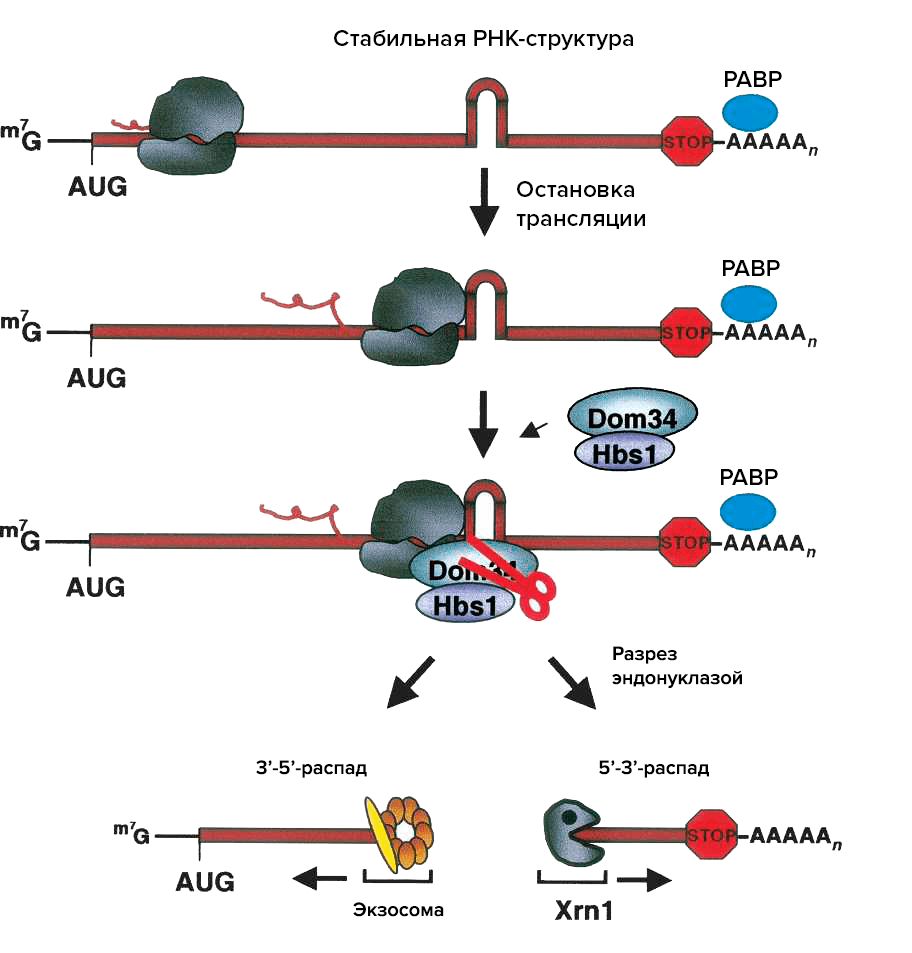
В некоторых случаях на пути рибосомы при ее проходе по мРНК встают непреодолимые препятствия, опять же из-за нарушений в мРНК или рРНК (см. ниже). Такую рибосому узнают определенные белки, они в свою очередь привлекают эндонуклеазу, которая разрезает мРНК в месте остановки. Далее оставшиеся два куска мРНК подвергаются распаду с помощью экзонуклеаз. Этот механизм деградации называется NGD (no-go decay) (рис. 4) [15].
Рисунок 4. Схема no-go decay (NGD)
Долгоживущие РНК все-таки не вечны
Рано или поздно каждая РНК в клетке распадается. Даже некодирующие рРНК и тРНК, которые обычно живут долго, со временем все-таки отбраковываются по мере появления в них ошибок, то есть по мере «изнашивания».
От общего количества РНК в клетке наибольшую долю составляют рибосомные — 18S и 25S. Учитывая, что обе эти РНК входят в состав рибосом, логично было бы предположить, что нарушения в этих РНК выявляются в процессе синтеза белка. Это верно только для 18S рРНК — именно она занимается узнаванием кодонов мРНК при трансляции. Если во время синтеза белка рибосома останавливается, то 18S рРНК быстро разрушается, т.е. фактически используется такой же механизм выявления ошибки, что и при NGD. В обоих случаях сигналом к запуску распада выступает «застрявшая» во время синтеза рибосома. Очень может быть, что при этом ферменты разрушают и мРНК, и 18S рРНК без выяснения того, из-за которой из них произошла остановка синтеза. В данном случае надежнее сразу избавиться от обоих участников процесса. Однако это никак не касается 25S рРНК, в которой непосредственно находится ферментативный центр рибосомы. Распад 25S рРНК не зависит не только от трансляции, но и практически от всех белков, участвующих в различных типах распада РНК, кроме одной из экзосомных экзонуклеаз. Предполагается, что сигналом для распада 25S рРНК является невозможность связывания рибосомных белков с дефектной молекулой. Видимо, прежде всего, в деградации 25S рРНК участвуют ферменты распада белков. После диссоциации рибосомных белков от 25S рРНК и их распада сама теперь уже «оголенная» рРНК становится доступной для экзонуклеаз [16–19].
Время жизни тРНК измеряется часами и днями. В течение этого времени они постоянно участвуют в синтезе белка, проходя примерно через 40 циклов трансляции в минуту. Нуклеотиды в составе тРНК специфическим образом модифицированы. Мишенью для быстрого распада прежде всего становятся тРНК, по какой-либо причине потерявшие свои модификации. Такие тРНК менее компактны из-за нарушения структуры и являются легкой добычей для факторов деградации [20]. На 3’-хвосте гипомодифицированных тРНК синтезируется дополнительный тринуклеотид ССА, что является сигналом быстрого распада [21].
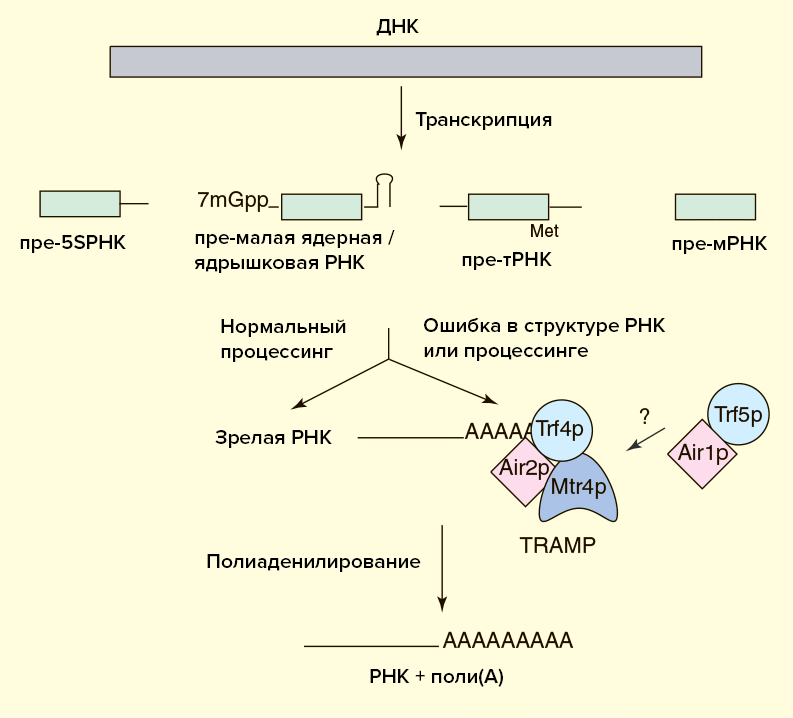
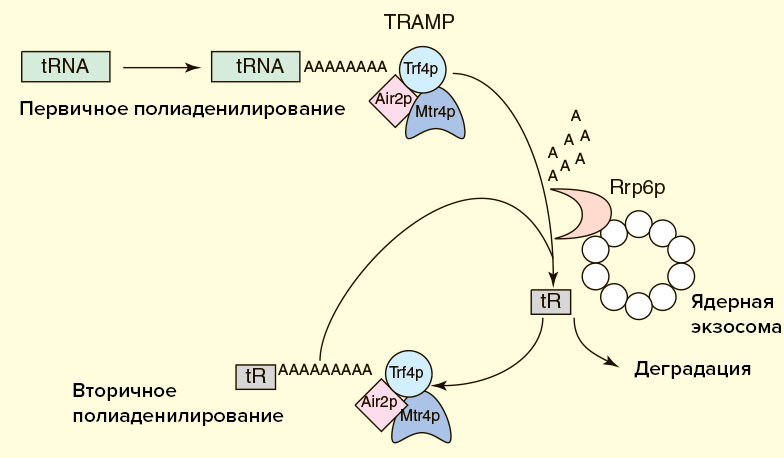
Известно, что TRAMP может стимулировать экзосомную деградацию и неполиаденилированной РНК, но в этом случае процесс идет медленнее. Зачем же нужен поли(А)-хвост? Дело в том, что некодирующие РНК вовсе не представляют собой одноцепочечную нить, а свернуты в сложные вторичные и третичные структуры. Иногда экзосома в процессе укорочения РНК «застревает» на высокоструктурированных участках. В этом случае TRAMP осуществляет дополнительные раунды полиаденилирования и деградации до тех пор, пока РНК не будет полностью разрушена. Видимо, для быстрой эффективной работы экзосоме необходима затравка в виде одноцепочечного участка РНК, роль которого как раз и играет поли(А)-хвост (рис. 5) [22].
Рисунок 5а. Схема деградации некодирующих РНК в ядре
Рисунок 5б. Схема деградации полиаденилированной тРНК экзосомой
Некоторым РНК нельзя позволять долго жить
Распад РНК — это не только способ контролировать качество работающих в клетке молекул, это также и мощный механизм регуляции. Известно, что в клетке есть РНК, которые распадаются очень быстро, за считанные минуты. Время жизни РНК напрямую связано с ее функцией. Быстрее всего распадаются мРНК, кодирующие регуляторные факторы. Количество этих молекул повышается в определенный момент клеточного цикла или в ответ на определенные стимулы, после чего они быстро распадаются. Такая система позволяет клетке оперативно реагировать на различные внутренние и внешние сигналы. Если этот процесс по каким-либо причинам нарушается, и РНК накапливаются в избыточном количестве, это может привести к сбою в работе всей клетки. Поэтому многие из генов таких мРНК являются протоонкогенами. Такие гены, как c-myc, c-fos, TNFα относятся к их числу.
Как оказалось, такие короткоживущие мРНК содержат специальные сигналы быстрого распада. Самый распространенный тип подобного сигнала — AU-богатый элемент (т.е., последовательность, богатая аденином и урацилом). AU-богатые элементы представляют собой последовательности в Если вставить такой элемент в состав долгоживущей РНК, то она начнет быстро распадаться. Например, AU-богатый элемент c-fos укорачивает время жизни мРНК β-глобина с более, чем 24 часов до 37 минут! С AU-богатыми элементами связываются клеточные факторы, которые и контролируют их функции, и привлекают ферменты деградации. Иногда они вовсе не стимулируют быстрый распад мРНК, а, наоборот, стабилизируют ее. Одни и те же белки могут связываться с разными AU-богатыми элементами и вызывать при этом различный эффект [23], [24].
Интересно, что многим короткоживущим мРНК одних AU-богатых элементов не хватает. Они содержат и другие последовательности, которые независимо от AU-богатых элементов ускоряют их разрушение. Так что, если по каким-то причинам один из двух механизмов деградации данной мРНК не сработал, то второй уж точно обеспечит ее распад. По-видимому, эта система двойной регуляции времени жизни возникла в эволюции особо важных, но при этом потенциально опасных в случае излишнего накопления мРНК. Кроме того, наличие двух элементов быстрой деградации дает большую гибкость при клеточном ответе на внешние и внутренние сигналы [25].
Чтобы не распасться, нужно стабилизироваться
А что, если мы зададимся не вопросом, почему какие-то РНК быстро распадаются, а почему другие живут долго? Может быть, РНК-долгожители не деградируют, потому что содержат сигналы, защищающие их от быстрого разрушения? Действительно, совсем недавно выяснилось, что многие долгоживущие мРНК имеют в своем составе определенные мотивы, с которыми взаимодействуют белки-стабилизаторы. Пока известно восемь таких элементов и изучена их связь с белком со сложным названием HNRPA2B1. Этот белок обеспечивает удлинение времени жизни соответствующей мРНК. Вероятно, существуют и другие подобные белки, которые еще только предстоит обнаружить. Кроме того, пока остается открытым вопрос, как именно работает механизм защиты РНК от деградации [26].
Разрушение? Нет, защита
РНК-интерференция — это механизм подавления экспрессии генов, который может вести к распаду соответствующей мРНК. В системе РНК-интерференции принимают участие два типа молекул РНК — микроРНК и малые интерферирующие РНК. Эти молекулы имеют очень малые размеры — около 22 нуклеотидов.
Эти маленькие РНК соединяются с комплементарными им последовательностями мРНК-мишеней, после чего происходит или разрезание мРНК-мишени и дальнейшее разрушение ее фрагментов, или просто блокировка трансляции с этой мРНК. Какие же РНК становятся жертвами РНК-интерференции? Микро-РНК чаще всего связываются с клеточными мРНК, распад которых необходим для регуляции экспрессии соответствующих генов. Малые интерферирующие РНК призваны защищать клетку от чужеродных РНК, попадающих в клетку из вирусов, а также от внутренних врагов — ретротранспозонов [27].
Что же такое распад РНК для клетки?
Подытожим, зачем нужен распад РНК.
Во-первых, это контроль качества РНК. Своевременный распад нефункциональной РНК препятствует накоплению ненужных и потенциально опасных для клетки молекул (как непосредственно РНК, так и белков). Неоценимую помощь в этом процессе оказывают разнообразные механизмы регистрации ошибок, заточенные под распознавание определенных типов нарушений РНК.
Во-вторых, это регуляция экспрессии генов. Экспрессия гена — это преобразование информации, хранящейся в генах, в функциональный продукт — РНК или белок. Но ведь количество той или иной РНК или белка в клетке в каждый момент времени определяется и уровнем синтеза этой молекулы, и уровнем распада. Поэтому быстрая деградация РНК — это очень важный механизм регуляции экспрессии, который позволяет клетке быстро отвечать на внутренние и внешние сигналы.
В-третьих, это защита от чужеродных и вредных молекул. Часто генетический материал вирусов оказывается в клетке именно в форме РНК, кроме того, некоторые транспозоны могут транскрибироваться, что также приводит к накоплению нежелательных молекул. Распознавание этих РНК и избавление от них клетки — необходимый защитный процесс, который также обеспечивается механизмами, основанными на распаде РНК.
Большие дела небольших молекул: как малые РНК дирижируют генами бактерий
Большие дела небольших молекул: как малые РНК дирижируют генами бактерий
рисунок автора статьи и Копаевой Е.А.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: В последние годы РНК — а особенно ее «неклассические» разновидности — приковывает внимание биологов всего мира. Выяснилось, что регуляция с помощью некодирующих РНК широко распространена — начиная от вирусов и бактерий и заканчивая человеком. Изучение разнообразия малых бактериальных РНК-регуляторов ясно показало их важную роль как в промежуточном метаболизме, так и в адаптивных реакциях. В этой статье описаны разновидности малых РНК бактерий и механизмы регуляции, осуществляемые с их помощью. Особый акцент сделан на роли этих молекул в жизнедеятельности бактериальных агентов, вызывающих особо опасные инфекции.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
РНК: больше, чем просто копия ДНК
Со школьной скамьи большинству читателей этого сайта известны основные механизмы работы живой клетки. В курсе биологии, начиная с законов Менделя и заканчивая ультрасовременными проектами по секвенированию геномов, красной нитью проходит идея магистральной генетической программы развития организма, известная профессиональным биологам как центральная догма молекулярной биологии. Она гласит, что молекула ДНК выступает носителем и хранителем генетической информации, которая через посредника — матричную РНК (мРНК), и при участии рибосомальной (рРНК) и транспортной РНК (тРНК), — реализуется в виде белков. Последние определяют видовой и индивидуальный фенотип.
Несложно заметить, что РНК при таком подходе отводится второстепенная роль: проводя юридическую аналогию, можно сказать, что РНК (матричная, в частности) — что-то вроде копии важного документа, не имеющей самостоятельной законной силы. На общем фоне выделяются некоторые вирусы (например, ВИЧ, вирусы простуды и гриппа, а также вызывающие кишечные инфекции энтеровирусы) — самые настоящие генетические «еретики», хранящие генетическую информацию в форме РНК (а не ДНК, как положено). Но вирусы — форма жизни сама по себе весьма экстравагантная и, благодаря крайней степени паразитизма, часто очень несуразная. В частности, они лишены клеточного строения, неизменно присутствующего у всех остальных организмов. По этой причине можно относиться к ним просто как к органическому веществу, хотя и сложно устроенному — нуклеопротеиду, способному к самовоспроизведению при попадании в клетку.
Такое положение дел и отведение РНК роли второстепенного участника молекулярного спектакля сохранялось в научной среде вплоть до 80-х годов прошлого века. Пристальнее присмотреться к РНК заставили работы Т. Чека, показавшего, что РНК может выступать в роли катализатора химических реакций. Прежде считалось, что ускорение химических процессов в клетке — прерогатива ферментов, имеющих исключительно белковую природу. Открытие каталитической активности у РНК имело далеко идущие следствия — вкупе с более ранними теоретическими работами К. Вёзе [1] и М. Эйгена, оно позволило нарисовать возможную картину пребиотической эволюции на нашей планете. Дело в том, что с момента открытия у ДНК функции носителя генетической информации дилемма о том, что появилось в ходе эволюции раньше — ДНК или белок, необходимый для воспроизводства ДНК, — казалась почти столь же философской (то есть, беспредметной), как и вопрос о первенстве появления курицы или яйца. После открытия Т. Чека решение обрело вполне реальные очертания — была найдена молекула, обладающая свойствами как носителя информации, так и биокатализатора (пусть и в зачаточном виде). Со временем эти исследования переросли в целое направление в биологии, изучающее возникновение жизни через призму так называемого «мира РНК» [2, 3].
Так стало очевидно, что древний мир РНК мог иметь отношение к зарождению и расцвету первичной жизни. Тем не менее, из этого вовсе не следует автоматически, что РНК у современных организмов — не архаизм, адаптированный под нужды внутриклеточных молекулярных систем, а действительно важный участник молекулярного ансамбля клетки. Лишь развитие молекулярных методов — в частности, секвенирования нуклеиновых кислот [4, 5], — показало, что РНК истинно незаменимы в клетке, причем не только в виде канонической троицы «мРНК, рРНК, тРНК». Уже первые обширные данные по секвенированию ДНК указали на показавшийся поначалу труднообъяснимым факт — большая часть ее оказалась некодирующей — то есть, не несущей информацию о молекулах белка или «стандартных» РНК. Конечно, частично это можно приписать «генетическому мусору» — «выключенным» или утративших свою функцию фрагментам генома. Но сохранять такое количество «приданого» для биологических систем, старающихся тратить энергию экономно, кажется нелогичным.
И действительно, более детальные и тонкие методы исследования позволили обнаружить целый класс РНК-регуляторов экспрессии генов, частично заполняющих межгенное пространство. Еще до прочтения полных последовательностей геномов эукариот у круглого червя С. elegans были выделены микроРНК — молекулы небольшой длины (около 20 нуклеотидов), которые могут специфично связываться с участками мРНК по принципу комплементарности [6]. Несложно догадаться, что в таких случаях с мРНК уже не прочесть информацию о кодируемых белках: рибосома просто не может «пробежаться» по такому, внезапно ставшему двухцепочечным, участку. Этот механизм подавления экспрессии гена, называемый РНК-интерференцией, уже был разобран на «биомолекуле» достаточно подробно [7, 8, 9]. На сегодняшний день открыты тысячи молекул микроРНК и других некодирующих РНК (piRNA, snoRNA, nanoRNA и др.). У эукариот (в том числе, и у человека) они расположены в межгенных участках. Установлена важная их роль в клеточной дифференцировке, канцерогенезе, иммунном ответе и других процессах и патологиях [7].
Малые РНК — «троянский конь» для бактериальных белков
Несмотря на то, что некодирующие белок РНК у бактерий были открыты гораздо раньше первых аналогичных регуляторов у эукариот, их роль в метаболизме бактериальной клетки долгое время была завуалирована для научной общественности. Это объяснимо — традиционно бактериальная клетка считалась более примитивной и менее таинственной для исследователя структурой, сложность которой не идет ни в какое сравнение с нагромождением структур в клетке эукариотической. Более того, в геномах бактерий содержание некодирующей информации составляет лишь несколько процентов от общей длины ДНК, достигая максимум 40% у некоторых микобактерий. Но, учитывая, что микроРНК обнаружены даже у вирусов, у бактерий они должны играть важную регуляторную роль и подавно.
Оказалось, у прокариот существует довольно много малых РНК-регуляторов [10]. Условно все они могут быть разделены на две группы:
В первой группе выделяют малые РНК, для которых связывание с белком возможно, но необязательно. Известный пример — РНКаза Р (RNAse P), действующая как рибозим на «созревающую» тРНК. Однако если РНКаза Р может функционировать без белкового компонента, то для других малых РНК в этой группе связывание с белком обязательно (а сами они являются, по сути, кофакторами). Например, tmРНК активирует сложный белковый комплекс, выступая в роли «отмычки» для «застрявшей» рибосомы — в случае, если матричная РНК, с которой ведется считывание, подошла к концу, а стоп-кодон так и не повстречался.
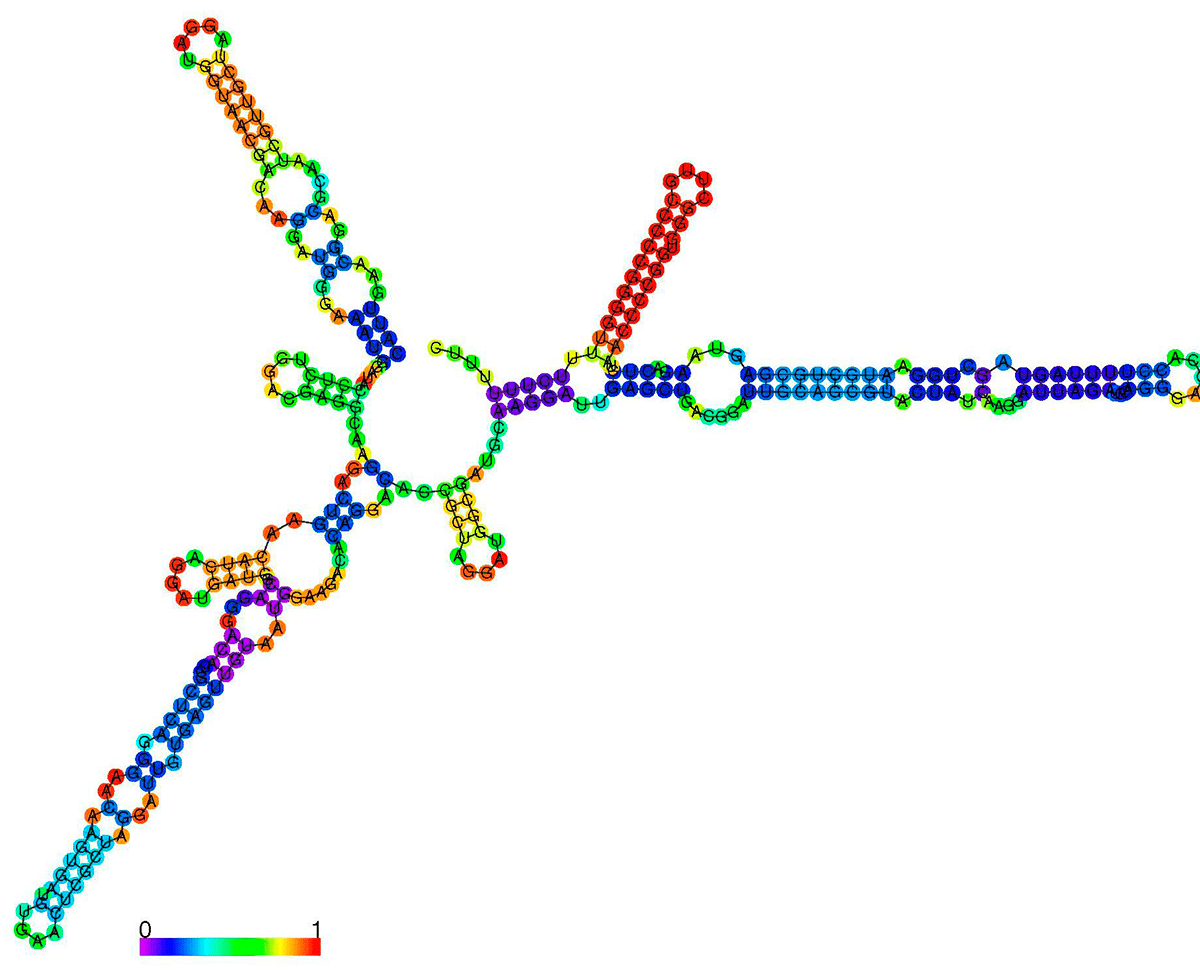
Рисунок 1. Биоинформатически предсказанная вторичная структура малой РНК CsrB из Vibrio cholerae M66-2. Малые РНК — одноцепочечные молекулы, но, как и для других РНК, сворачивание (фолдинг) в стабильную пространственную структуру сопровождается формированием участков, где молекула гибридизуется сама на себя. Многочисленные изгибы на структуре в виде разомкнутых колец называются шпильками. В некоторых случаях комбинация шпилек позволяет РНК играть роль «губки», нековалентно связывая определенные белки. Но чаще молекулы такого типа интерферируют с ДНК или РНК; при этом пространственная структура малой РНК нарушается, и образуются новые участки гибридизации уже с молекулой-мишенью. Тепловая карта отражает вероятность того, что соответствующая пара нуклеотидов действительно будет связана внутримолекулярной водородной связью; для неспаренных участков — вероятность образовать водородные связи с какими-либо участками внутри молекулы. Изображение получено с помощью программы RNAfold.
Малые РНК бактерий интерферируют. и весьма успешно!
Механизм, по которому действуют регуляторы второй группы, в общем-то, схож с таковым у регуляторных РНК эукариот — это та же РНК-интерференция путем гибридизации с мРНК, только сами цепочки малых РНК зачастую подлиннее — до нескольких сотен нуклеотидов (см. рис. 1). В результате, из-за малой РНК рибосомы не могут считать информацию с мРНК. Хотя зачастую, похоже, не доходит и до этого: образовавшиеся комплексы «малая РНК — мРНК» становятся мишенью РНКаз (типа РНКазы Р) [10].
Компактность и плотность упаковки прокариотического генома дает о себе знать: если у эукариот большинство регуляторных РНК записаны в отдельных (чаще всего не кодирующих белок) локусах, то многие малые РНК бактерий могут кодироваться в том же участке ДНК, что и подавляемый ген, но на противолежащей цепи! Такие РНК называются цис-кодируемыми (антисмысловыми), а малые РНК, лежащие на некотором удалении от подавляемого участка ДНК — транс-кодируемыми. По-видимому, расположение цис-РНК можно считать торжеством эргономичности: они могут считываться с противолежащей цепи ДНК в момент ее расплетения одновременно с транскриптом-мишенью, что позволяет тонко управлять количеством синтезируемого белка.
Малые РНК в транс-положении эволюционируют независимо от целевой мРНК, и последовательность регулятора сильнее меняется в результате мутаций. Возможно, такой расклад бактериальной клетке только «на руку», поскольку малая РНК приобретает активность в отношении ранее несвойственных ей мишеней, что сокращает время и энергетические затраты на создание других регуляторов. С другой стороны, давление отбора не позволяет транс-малой РНК мутировать слишком сильно, поскольку она потеряет активность. Тем не менее, для гибридизации с матричной РНК большинству транс-малых РНК необходим помощник — белок Hfq. По-видимому, в противном случае неполная комплементарность малой РНК может создавать проблемы для связывания с мишенью.
По-видимому, потенциально реализуемый механизм регуляции по принципу «одна малая РНК — множество мишеней» помогает интегрировать метаболические сети бактерии, что крайне необходимо в условиях короткой одноклеточной жизни. Можно продолжить спекуляцию на тему и предположить, что с помощью транс-кодируемых малых РНК осуществляется пересылка экспрессионных «предписаний» из функционально связанных, но физически удаленных локусов. Необходимостью в подобного рода генетической «перекличке» логично объясняется большое количество малых РНК, обнаруженных у патогенных бактерий. Например, несколько сотен малых РНК найдено у рекордсмена по этому показателю — холерного вибриона (Vibrio cholerae). Это микроорганизм, который умеет выживать и в окружающей водной среде (как пресной, так и соленой), и на водных моллюсках, и в рыбе, и в кишечнике человека — тут без комплексной адаптации с помощью регуляторных молекул никак не обойтись!
CRISPR на страже бактериального здоровья
Нашлось применение малым РНК и в решении другой насущной для бактерий задаче. Даже самые злостные патогенные кокки и палочки могут оказаться бессильны перед лицом опасности, исходящей от особых вирусов — бактериофагов, способных молниеносно истребить бактериальную популяцию. У многоклеточных организмов для защиты от вирусов существует специализированная система — иммунная, средствами клеток и выделяемых ими веществ охраняющая организм от незваных гостей (в том числе, вирусной природы). Бактериальная клетка — одиночка, но она не так уязвима, как может показаться на первый взгляд. Хранителями рецептов для поддержания противовирусного иммунитета бактерий выступают локусы CRISPR — кластерные регулярно-прерывистые короткие палиндромные повторы (clustered regularly interspaced short palindromic repeats) (рис. 2; [11]). В геномах прокариот каждая CRISPR-кассета представлена лидерной последовательностью длиной несколько сотен нуклеотидов, за которой следует серия из 2–24 (иногда до 400) повторов, разделенных спейсерными участками, схожими между собой по длине, но уникальными по нуклеотидной последовательности. Длина каждого спейсера и повтора не превышает сотню пар нуклеотидов [12].
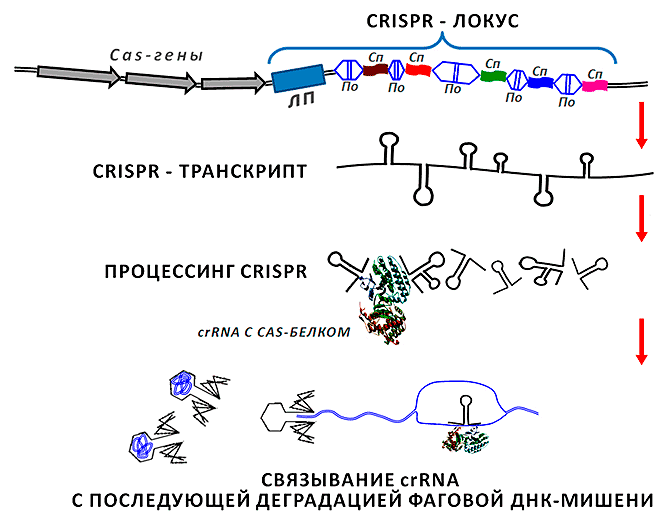
Рисунок 2. CRISPR-локус и процессинг соответствующей ему малой РНК до функционального транскрипта. В геноме CRISPR-кассета представлена перемежающимися между собой спейсерами (на рисунке обозначены как Сп), частично гомологичными участкам фаговой ДНК, и повторами (По) длиной 24–48 п.н., демонстрирующими диадную симметрию. В противоположность повторам, спейсеры внутри одного локуса одинаковы по длине (у разных бактерий это может быть 20–70 нуклеотидов), но отличаются по нуклеотидной последовательности. Участки «—спейсер—повтор—» могут быть достаточно протяженными и состоять из нескольких сотен звеньев. Вся структура фланкируется с одной стороны лидерной последовательностью (ЛП, несколько сотен пар оснований). Неподалеку находятся Cas-гены (CRISPR—associated), организованные в оперон. Белки, считываемые с них, выполняют ряд вспомогательных функций, обеспечивая процессинг транскрипта, считанного с CRISPR-локуса, его успешную гибридизацию с фаговой ДНК-мишенью, встраивание новых элементов в локус и т.д. Образующаяся в результате многоэтапного процессинга СrRNA гибридизуется с участком ДНК (нижняя часть рисунка), впрыскиваемой фагом в бактерию. Это заставляет «замолчать» транскрипционную машину вируса и останавливает его размножение в прокариотической клетке.
Из гипотезы формирования спейсеров неясно, зачем между ними нужны повторы, внутри одного локуса незначительно отличающиеся по длине, но практически идентичные по последовательности? Здесь открывается широкий простор для фантазии. Быть может, без повторов было бы проблематично осуществить разбиение генетических данных на смысловые фрагменты, подобные секторам на жестком диске компьютера, и тогда доступ транскрипционной машины к строго определенным участкам CRISPR-локуса стал бы затруднительным? А быть может, повторы упрощают рекомбинационные процессы при встраивании новых элементов фаговой ДНК? Или же они — «знаки препинания», без которых не обойтись при процессинге CRISPR? Как бы то ни было, биологическая причина, объясняющая поведение бактериальной клетки на манер гоголевского Плюшкина, в свое время будет найдена.
CRISPR, будучи «летописью» взаимоотношений бактерии с фагом, может использоваться в филогенетических исследованиях. Так, недавно осуществленное типирование по CRISPR позволило окинуть взглядом эволюцию отдельных штаммов чумного микроба (Yersinia pestis). Исследование их CRISPR-«родословных» пролило свет на события полутысячелетней давности, когда штаммы проникли в Монголию с территории, в настоящее время относящейся к Китаю [13]. Но не для всех бактерий, и, в частности, патогенов, данный метод применим. Несмотря на недавние сведения о предсказанных CRISPR-обрабатывающих белках у возбудителей туляремии (Francisella tularensis) и холеры, сами CRISPR, если и присутствуют в их геноме, то немногочисленны. Возможно, фаги, учитывая их положительный вклад в приобретение вирулентности патогенными представителями бактериального царства, не так уж вредны и опасны, чтобы обороняться от них с помощью CRISPR? Или же вирусы, атакующие эти бактерии, слишком многообразны, и стратегия «интерферирующего» РНК-иммунитета в отношении них бесплодна?
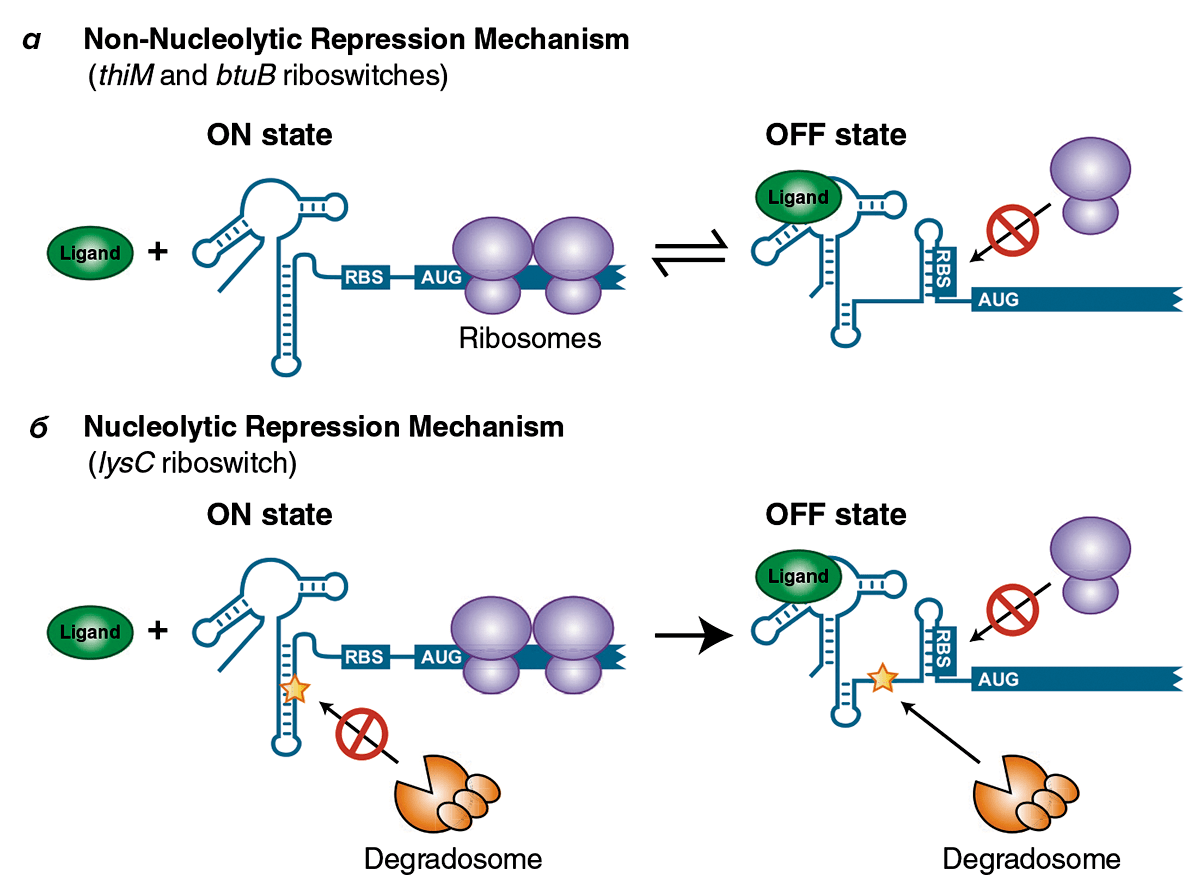
Рисунок 3. Некоторые механизмы работы рибосвитчей. Рибосвитчи (рибопереключатели) встроены в матричную РНК, но отличаются большой свободой конформационного поведения, зависящего от специфичных лигандов, что дает основание считать рибосвитчи самостоятельными единицами малых РНК. Изменение конформации экспрессионной платформы влияет на сайт посадки рибосомы на мРНК (RBS), и, как следствие, определяет доступность всей мРНК для считывания. Рибосвитчи в известной степени аналогичны операторной области в классической модели lac-оперона — но только аптамерные участки обычно регулируются низкомолекулярными веществами и осуществляют переключение работы гена на уровне мРНК, а не ДНК. а — В отсутствие лигандов рибосвитчи btuB (кобаламинового транспортера) и thiM (тиаминпирофосфат-зависимый), осуществляющие ненуклеолитическую репрессию мРНК, «включаются» (ON) и позволяют рибосоме заняться своим делом. Связывание лиганда с рибосвитчем (OFF-положение) приводит формированию шпильки, делающей этот участок недоступным для рибосомы. б — Лизиновый рибосвитч lysC при отсутствии лиганда также включен (ON). Выключение рибосвитча блокирует рибосоме доступ к мРНК. Но в отличие от описанных выше рибосвитчей, в лизиновом при выключении «оголяется» участок, разрезаемый специальным РНКазным комплексом (degradosome), и вся мРНК утилизируется, распадаясь на мелкие фрагменты. Репрессия рибосвитчем в данном случае называется нуклеолитической (nucleolytic) и необратима, поскольку, в отличие от примера (а), обратное переключение (снова в ON) уже невозможно. Важно отметить, что таким образом может достигаться утилизация группы «ненужных» мРНК: рибосвитч похож на деталь детского конструктора, и схожие по структуре переключатели могут иметься у целой группы функционально связанных матричных молекул.
Рибосвитч — датчик для бактерии
Итак, есть белок-ассоциирующие малые РНК, есть малые РНК, интерферирующие с собственными мРНК бактерий, а также РНК, захваченные бактериями из вирусов и подавляющие фаговую ДНК. Разве можно вообразить какой-нибудь еще механизм регуляции с помощью малых РНК? Оказывается, да. Если проанализировать описанное выше, то обнаружится, что во всех случаях антисмысловой регуляции наблюдается интерференция малой РНК и мишени как результат гибридизации двух отдельных молекул. А почему бы не расположить малую РНК в составе самого транскрипта? Тогда можно, изменяя конформацию такого «засланного казачка» внутри мРНК, менять доступность всей матрицы для считывания при трансляции или же, что энергетически еще более целесообразно, регулировать биосинтез мРНК, т.е. транскрипцию!
Такие структуры широко представлены в бактериальных клетках и известны как рибосвитчи (riboswitch). Они располагаются перед началом кодирующей части гена, на 5′-конце мРНК. Условно в составе рибосвитчей можно выделить два структурных мотива: аптамерный участок, ответственный за связывание с лигандом (эффектором), и экспрессионную платформу, обеспечивающую регуляцию экспрессии гена посредством перехода мРНК в альтернативные пространственные структуры [14]. Например, такой переключатель («выключающего» типа) используется для функционирования лизинового оперона: при избытке лизина он существует в виде «запутанной» пространственной структуры, блокирующей считывание с оперона, а при его нехватке рибосвитч «расплетается», и синтезируются белки, необходимые для биосинтеза лизина [10] (рис. 3).
Описанная принципиальная схема устройства рибосвитча — не канон, существуют варианты. Любопытный «включающий» тандемный рибосвитч обнаружен у холерного вибриона: экспрессионной платформе предшествуют сразу два аптамерных участка. Очевидно, это обеспечивает бóльшую чувствительность и более плавный ответ на появление в клетке еще одной аминокислоты — глицина. Возможно, косвенно причастен к высокой выживаемости бактерии схожий по принципу действия, но «двойной» рибосвитч в геноме возбудителя сибирской язвы (Bacillus anthracis). Он реагирует на входящее в состав минимальной среды жизненно важное для этого микроба соединение — тиаминпирофосфат [15].
Помимо переключения метаболических путей в зависимости от доступного для бактериальной клетки «меню», рибосвитчи могут быть датчиками гомеостаза бактерии. Так, они были замечены в регуляции доступности гена для считывания при нарушении функционирования трансляционной системы внутри клетки (например, такие сигналы как появление «незаряженных» тРНК и «неисправных» (stalled) рибосом), либо при изменении факторов внешней среды (например, повышении температуры) [14].
Не нужно белков, дайте нам РНК!
Так что же означает присутствие такого разнообразия малых РНК-регуляторов внутри бактерии? Свидетельствует ли это об отказе от концепции, когда главными «управленцами» являются белки, или мы наблюдаем очередной модный тренд? Видимо, ни то, и ни другое. Конечно, некоторые малые РНК являются глобальными регуляторами метаболических путей — как упомянутая CsrB, участвующая, вкупе с CsrС, в регуляции запасания органического углерода. Но, принимая во внимание принцип дублирования функций в биологических системах, малые РНК бактерий можно сравнить скорее с «антикризисным менеджером», чем с генеральным директором. Так, в условиях, когда для выживания микроорганизма нужно быстро перенастроить внутриклеточный метаболизм, их регуляторная роль может оказаться решающей и более эффективной, чем у белков с аналогичными функциями. Таким образом, РНК-регуляторы отвечают, скорее, за экспресс-реагирование, менее стойкое и надежное, чем в случае с белками: не следует забывать, что малая РНК поддерживает свою 3D-структуру и удерживается на ингибируемой матрице слабыми водородными связями.
Косвенным подтверждением этих тезисов могут стать уже упоминавшиеся малые РНК холерного вибриона. Для этой бактерии попадание в организм человека — не желанная цель, а, видимо, чрезвычайная ситуация. Выработка токсинов и активация других, связанных с вирулентностью, путей в данном случае — всего лишь защитная реакция на агрессивное противодействие среды и клеток организма «чужакам». «Спасателями» здесь выступают малые РНК — например Qrr, помогающие вибриону в стрессовых условиях модифицировать стратегию выживания, изменяя коллективное поведение. Косвенно подтвердить эту гипотезу может также открытие малой РНК VrrA, активно синтезирующейся при нахождении вибрионов в организме и подавляющей наработку мембранных белков Omp [16]. «Спрятанные» мембранные белки в начальной фазе инфицирования, возможно, помогают избежать мощного иммунного ответа со стороны организма человека (рис. 4).
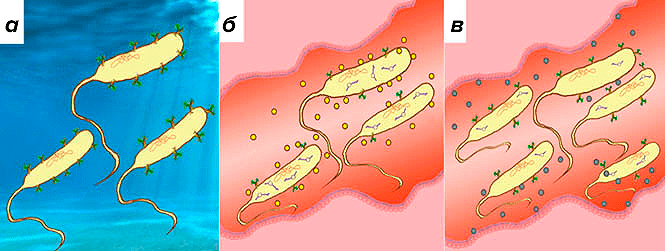
Рисунок 4. Малые РНК в реализации патогенных свойств холерного вибриона. а — Холерный вибрион хорошо чувствует себя и прекрасно размножается в водной среде. Организм человека, вероятно, не является основной экологической нишей для этого микроба. б — Попадая по водному или пищевому пути передачи инфекции в агрессивную среду — тонкий кишечник человека, — вибрионы по организованности поведения начинают напоминать псевдоорганизм, основная задача которого — сдержать иммунный ответ и создать себе благоприятную среду для колонизации. Большое значение в координации действий внутри популяции бактерий и их взаимодействия с организмом отводится мембранным везикулам. До конца неизученные факторы среды в кишечнике являются сигналами для экспрессии в вибрионах малых РНК (например, VrrA). В результате запускается механизм образования везикул, являющихся неиммунногенными при низком числе клеток вибриона в кишечнике. Дополнительно к описанному эффекту малые РНК помогают «спрятать» потенциально провокационные для иммунной системы человека мембранные белки Omp. При косвенном участии малых РНК Qrr1—4 запускается интенсивная выработка холерного токсина (не показано на рисунке), что дополняет спектр адаптивных реакций холерного вибриона. в — Уже через несколько часов количество бактериальных клеток возрастает, а пул малых РНК VrrA уменьшается, что, вероятно, приводит к экспонированию мембранных белков. Количество «пустых» везикул также постепенно уменьшается, и на этом этапе они заменяются на иммунногенные, доставляемые в энтероциты. Видимо, это часть «плана» по реализации комплексного сигнала, смысл которого — спровоцировать эвакуацию вибрионов из организма человека. NB: соотношение размеров бактериальных клеток и энтероцитов не соблюдено.
рисунок автора статьи и Копаевой Е.А.
Видимо, роль малых РНК у всех бактериальных патогенов велика, но в особенности это верно для тех, у которых паразитизм — факультативная экологическая ниша, либо у которых патогенность — эволюционно молодое приспособление. В этом смысле показательным может стать чумной микроб, произошедший от псевдотуберкулезной палочки несколько тысяч лет назад. Установлено высокое сходство геномов псевдотуберкулезной и чумной бактерий, и, в то же время, различия в нуклеотидных последовательностях у более чем половины общих для них малых РНК-регуляторов. Резонно полагать, что малые РНК послужили формированию физиологических механизмов, приведших к появлению высоковирулентного чумного микроба, вызвавшего печально известные эпидемии «черной смерти». Но во многих других случаях малые РНК — все же «актеры второго плана», ведь разнообразие функциональных белковых молекул из 20 типов аминокислот трудно сравнить с аналогичным у РНК, имеющих в своем арсенале лишь четыре типа нуклеотидов.
Интересно проследить, как изменятся наши представления о малых РНК-регуляторах, когда будут получены новые данные на платформах RNAseq, в том числе, по свободноживущим и некультивируемым формам. Недавние работы с использованием «глубокого секвенирования» уже дали неожиданные результаты, указав на наличие микроРНК-подобных молекул у мутантных стрептококков [17]. Конечно, такие данные нуждаются в тщательной перепроверке, но, как бы то ни было, можно с уверенностью утверждать, что изучение малых РНК у бактерий преподнесет немало сюрпризов.
Благодарности
Оригинальные идеи и композиционное оформление при создании заглавного рисунка, а также рисунка 4 принадлежат выпускнице ИархиИ ЮФУ Копаевой Е.А. Наличие в статье рисунка 2 — заслуга доцента каф. зоологии ЮФУ Г.Б. Бахтадзе. Он же осуществил научную корректуру и доработку заглавного рисунка и рисунка 4. Автор выражает им огромную признательность за терпение и творческий подход к делу. Отдельная благодарность коллеге, с.н.с. лаб. биохимии микробов Ростовского противочумного института Сорокину В.М. за обсуждение текста статьи и высказанные ценные замечания.