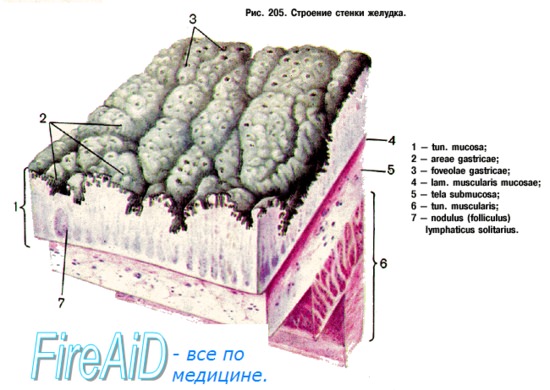
какую роль выполняет слизь в желудке
Какую роль выполняет слизь в желудке
Органическим компонентом желудочного сока является слизь.
Нерастворимая слизь (муцин) является продуктом секреторной активности добавочных клеток и клеток поверхностного эпителия. Муцин выделяется через апикальную мембрану мукоцита, образует слой слизи толщиной 0,5—1,5 мм, он обволакивает слизистую оболочку желудка и препятствует повреждающему воздействию соляной кислоты и пепсинов на клетки слизистой оболочки и раздражающих веществ, поступивших с пищей. Этими же клетками одновременно с муцином продуцируется и бикарбонат. Образующийся при взаимодействии муцина и бикарбоната мукозобикарбонатный барьер предохраняет слизистую оболочку от аутолиза под воздействием соляной кислоты и пепсинов.
Слой слизи является преградой для обратной диффизии ионов водорода из полости желудка; он нейтрализует соляную кислоту благодаря буферным свойствам из-за наличия гидрокарбонатов, а также адсорбирует ферменты. Под влиянием длительного воздействия желчных кислот (при забрасывании их из двенадцатиперстной кишки), салицилатов, масляной и пропионовой кислот, алкоголя происходит нарушение слизистого барьера. Это приводит к обратной диффизии ионов водорода из полости желудка, контакту слизистой оболочки с пепсинами и ее повреждению в результате аутолиза. Так формируются пептические язвы желудка. Возникновению язвенного процесса способствуют продукты жизнедеятельности микроорганизма Helicobacter pylori, которые усиливают секрецию соляной кислоты.
Какую роль выполняет слизь в желудке
Полость рта. Слюнные железы. Секрет всех слюнных желез, смешанный в полости рта, образует слюну, или ротовую жидкость, содержащую, кроме чистого секрета слюнных желез, постоянную микрофлору, слущенные эпителиальные клетки, лейкоциты, эритроциты и другие компоненты.
У человека имеется три пары больших слюнных желез: околоушная, подъязычная и подчелюстная, а также большое количество мелких желез, рассеянных в слизистой оболочке рта, губ, щек. Мелкие железы постоянно выделяют секрет, увлажняющий слизистую и предохраняющий ее от высыхания, а крупные железы выделяют секрет периодически и принимают участие в пищеварении. Слюнные железы, наряду с секрецией слюны, обладают эндокринной функцией, выделяя гормоны и гормоноподобные вещества. К ним относятся: а) паротин, регулирующий фосфорно-кальциевый обмен в костях и тканях зуба; б) эритропоэтин; в) фактор роста и регенерации эпителия слизистой желудочно-кишечного тракта; г) инсулиноподобные факторы роста и другие.
В течение суток у взрослого человека образуется от 0,5 до 2,0 л слюны, pH которой составляет от 5,8 до 8,0. Смешанная слюна содержит 99,5% воды и, соответственно, 0,5-0,6% сухого вещества, включающего органические и неорганические компоненты. Неорганические компоненты включают ионы натрия, калия, кальция, магния, железа, фтора, а также фосфаты, хлориды, сульфаты, бикарбонаты. Органические вещества слюны чрезвычайно гетерогенны по химической природе и биологической активности. Это прежде всего ферменты. В слюне содержится около 50 различных ферментов, относящихся к гидролазам, оксиредуктазам, трансферазам, липазам, изомеразам. Оптимум действия ферментов слюны – слабощелочная реакция.
Типовые нарушения функции слюнных желез и связанное с ними изменение водно-электролитного баланса организма. К типовым нарушениям функции слюнных желез относятся гипосиалия и гиперсиалия.
Гиперсиалия характеризуется резким увеличением слюноотделения в среднем от 1,5 л до 3-4,5 л в зависимости от степени тяжести патологии. При нейропаралитической гиперсиалии суточный объем слюноотделения может достигать 10-12 л, что лежит в основе изотонической дегидратации.
Причины гиперсиалии весьма разнообразны, включают инициирующее воздействие следующих этиологических факторов:
1) раздражение верхнего и нижнего слюноотделительных центров (ядра лицевого и языкоглоточного нервов) при бульбарных параличах, ишемии, гипоксии, кровоизлияниях, опухолевых поражениях структур продолговатого мозга;
2) активация структур переднего гипоталамуса, включающего высшие вегетативные центры холинергических нервных влияний на различные органы и ткани, в том числе и на слюнные железы;
3) перерезка разветвлений лицевого нерва (барабанной струны) при неудачных оперативных вмешательствах, что приводит к развитию денервационного синдрома и нейропаралитической гиперсиалии;
4) рефлекторная стимуляция бульбарных центров слюноотделения при воспалительных деструктивных процессах в слизистой желудочно-кишечного тракта, при гельминтозах;
5) избыточное освобождение медиаторов альтерации, в частности ацетилхолина, гистамина, лейкотриенов; при стоматитах инфекционной или инфекционно-аллергической природы, прорезывании зубов у детей, адаптации к протезам;
6) системное и локальное действия в полости рта токсинов экзогенной или эндогенной природы, когда слюнные железы элиминируют из кровотока ксенобиотики или аутокины и экспрессируют их вместе с большим количеством слюны;
7) при язвенной болезни 12-перстной кишки в случаях усиления центрогенных холинергических влияний на секреторную активность желудочно-кишечного тракта;
8) действие лекарственных препаратов с выраженными свойствами холиномиметиков или симпатолитиков.
При гиперсиалии значительное количество слюны попадает в просвет желудочно-кишечного тракта, нарушая оптимум действия протеолитических ферментов желудка (пепсинов), возникает перераспределение объемов внутрисосудистой и внесосудистой жидкости.
Роль желудка в регуляции водно-электролитного баланса и пищеварения. Клетки желудочных желез ежесуточно секретируют 2-3 л желудочного сока, состоящего на 99,0-99,5% из воды и 0,5-1,0% плотного остатка. Последний представлен неорганическими соединениями (хлориды, сульфаты, фосфаты, бикарбонат натрия, ионы калия, кальция, магния) и органическими веществами (ферменты, мукоиды). В желудочном соке в небольшом количестве содержатся азотсодержащие вещества небелковой природы: мочевина, мочевая и молочная кислоты.
Различают базальную (голодную) и стимулированную пищеварительную секрецию. Натощак у взрослого человека выделяется около 10% того количества, которое выделяется при максимальной стимуляции.
В процессе желудочной секреции выделяют три фазы: 1) сложно-рефлекторную (цефалическую); 2) желудочную; 3) кишечную.
Важнейшими компонентами желудочного сока являются соляная кислота, пепсиногены и слизь. Секреция соляной кислоты – ярко выраженный цАМФ-зависимый процесс, активация которого связана с усилением гликоген- и гликолитической активации кислотообразующей функции париетальных клеток. При этом возникают процессы фосфорилирования-дефосфорилирования субстратов в митохондриальной окислительной цепочке, транспортирующей ионы водорода из матричного пространства. И наконец, важным структурным компонентом париетальных клеток является (Н-К)-АТФ-аза секреторной мембраны, перекачивающая протоны из клеток в просвет железы за счет энергии АТФ. Вода поступает в париетальные клетки путем осмоса.
В желудочном соке выделяют несколько видов пепсиногенов (A, В, С, D и другие), активируемых при участии соляной кислоты, а также имеются непротеолитические ферменты (липаза, лизоцим, муколизин, карбоксигидразы, уреазы).
Важнейшим протективным фактором желудка от воздействия соляной кислоты и пепсинов является слизеобразование. Желудочная слизь (или муцин) состоит из нерастворимой (видимой) и растворимой фракций. Видимая слизь – высокогидротированный гель, содержащий нейтральные мукополисахариды, сиеломуцины, гликопротеиды, протеогликаны, протеины. Растворенный муцин является продуктом секреции желудочных мукозных клеток и переваривания видимой слизи.
Желудочная слизь обладает большой буферной емкостью за счет наличия бикарбонатов и фосфатов. При взаимодействии муцина и бикарбоната формируется мукозно-бикарбонатный барьер, предохраняющий слизистую от аутолиза.
Роль тонкого и толстого кишечника в обеспечении пищеварения и водно-электролитного баланса. В течение суток у человека вырабатывается около 2,5 л кишечного сока, выделяемого различными железами и имеющего сложный состав.
В проксимальном участке 12-перстной кишки находятся бруннеровы железы, сходные по структуре с пилорическими. Сок бруннеровых желез – бесцветная жидкость слабощелочной реакции (рН 7-8), главным его компонентом является муцин, обладающий слабой протеолитической, амилолитической и липолитической активностью.
В слизистой оболочке 12-перстной и всей тонкой кишки заложены кишечные крипты, или либеркюновы железы, окружающие каждую ворсинку. Секреторной способностью обладают многие эпителиоциты крипт тонкой кишки. Однако важнейшие кишечные ферменты сосредоточены не в криптах, а на поверхности ворсинок, будучи трансмобилизованными из клеток или адсорбированными из просвета кишечника.
Бокаловидные клетки слизистой тонкого кишечника обеспечивают выделение слизи через разрывы апикальной плазматической мембраны, их секрет обладает протеолитической активностью.
Энтероциты с ацидофильными гранулами содержат гидролитические ферменты, а аргентофинные клетки обладают эндокринной функцией. Клеточная секреция включает два самостоятельных процесса – отделение жидкой и плотной частей сока. Плотная часть кишечного сока содержит отторгнутые эпителиальные клетки, а также основную массу кишечных ферментов и биологически активные вещества.
Жидкая часть включает в себя органические и неорганические вещества. Органические вещества – это слизь, белки, аминокислоты, мочевина и другие. В числе неорганических веществ кишечного сока имеются хлориды, бикарбонаты, фосфаты, соли натрия, калия, кальция. рН кишечного сока в норме составляет 7,2-7,6, а при усилении секреции достигает 8,6.
В тонком кишечнике осуществляется полостное и пристеночное пищеварение, завершается гидролиз пептидов при участии аминопептидазы щелочной каймы энтероцитов
Пристеночный гидролиз жиров обеспечивается кишечной моноглицеридлипазой, а нуклеиновых кислот – при участии нуклеаз, эстераз и щелочных фосфатаз. Углеводы гидролизуются глюкозидазами (мальтазой и трегалазой), галактизидазой (лактазой), глюкоамилазой. Высокая субстратная специфичность кишечных дисахаридаз при их дефиците обусловливает непереносимость соответствующих дисахаридов, развитие синдромов мальабсорбции и диареи.
Толстая кишка в функциональном отношении может быть представлена тремя отделами:
1) проксимальным (слепая, восходящая ободочная, проксимальная часть поперечно-ободочной);
2) дистальным (дистальная часть поперечно-ободочной, нисходящая ободочная, сигмовидная);
Основными функциями толстой кишки являются секреторная, всасывательная, резервирующая и экскреторная.
Из тонкой кишки химус через илеоцекальный канал порциями переходит в толстую кишку, что составляет до 4 л химуса.
Часть пищи, в том числе клетчатка и пектин, подвергается гидролизу в основном в проксимальной части толстой кишки за счет ферментов химуса и сока толстой кишки (катепсина, пептидазы, липазы, амилазы, нуклеазы, щелочной фосфатазы); рН кишечного сока составляет 8,5-9,0. В толстом кишечнике происходит всасывание жидкости и соли.
Натрий всасывается в плазму через эпителиальную клетку против градиента концентрации при участии активного энергозависимого транспорта. Часть натрия пассивно всасывается по осмотическому градиенту через межклеточное пространство.
Всасывание хлоридов происходит против химического градиента концентрации, но в соответствии с электрическим, усвоение хлоридов происходит в результате анионного обмена с бикарбонатами. Количество бикарбонатов в фекальных массах варьирует в широких пределах.
В толстом кишечнике происходит всасывание воды до 4-6 л в сутки. Это пассивный процесс, регулируемый осмотическим и гидростатическим давлением. У здорового человека всасывание воды и солей в 3-4 раза меньше максимально возможной. Всасывание указанных ингредиентов зависит от скорости продвижения пищевой массы в тонком и толстом кишечнике.
Внешнесекреторная функция поджелудочной железы. Поджелудочная железа натощак выделяет небольшое количество секрета, продукция которого резко возрастает при поступлении пищевого содержимого из желудка в 12-перстную кишку и достигает в среднем до 1,5-2,5 л в сутки.
Щелочная среда панкреатического сока (рН 7,5-8,8) обусловлена наличием в нем гидрокарбонатов, обеспечивающих ощелачивание желудочного содержимого.
Секреция сока поджелудочной железы происходит в три фазы: сложнорефлекторную, желудочную и гуморальную.
Основную массу белков панкреатического сока составляют ферменты (трипсин, химотрипсин, карбоксипептидаза, калликреин и другие), продуцируемые в основном в виде проферментов и активирующиеся в 12-перстной кишке.
Желчеобразование и желчевыделение. Секреция желчи у человека в сутки составляет до 1,0 л. Желчеобразование осуществляется непрерывно, но интенсивность его изменяется в зависимости от характера нервных и гуморальных влияний. Составными частями желчи являются вода, желчные кислоты, билирубин, холестерин, неорганические соли, жирные кислоты, фосфолипиды и другие компоненты. Для пузырной желчи характерна нейтральная или кислая среда (рН 6,0-7,0), а для печеночной – щелочная (рН 7,5-8,0).
С помощью желчи усиливается полостное пищеварение белков, углеводов, особенно нейтральных жиров и липидов, активируется всасывание кальция. Важная роль в регуляции водно-солевого гомеостаза отводится легким и коже: с выделенным воздухом теряется 300-400 мл воды в сутки, а с потом – 600-700 мл.
Наиболее выраженные нарушения водно-солевого обмена, связанные с патологией системы органов пищеварения, возникают в условиях гипо- или гиперсаливации, неукратимой рвоты, гиперсекреторных состояний желудка, кишечной непроходимости, диарейного синдрома. Многие из указанных форм патологии носят приобретенный характер, а в ряде случаев – врожденный или наследственный.
Слизистый след раковых заболеваний
Слизистый след раковых заболеваний
Автор
Редактор
Статья на конкурс «био/мол/текст»: Муцины — главные гликопротеины слизи, покрывающей дыхательные, пищеварительные и мочеполовые пути. Слизистый слой защищает от инфекций, обезвоживания, физических и химических повреждений, а также играет роль смазки и способствует прохождению веществ по тракту. Но интересно другое: оказывается, по изменению уровня продукции муцинов в эпителиальных клетках различных органов — легких, простаты, поджелудочной железы и других — можно судить о развитии скрытых до поры до времени онкологических процессов. Особенно это актуально при затруднениях в диагностике рака и в определении источника опухолевых клеток при метастазировании.
Обратите внимание!
Эта работа опубликована в номинации «лучшее новостное сообщение» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
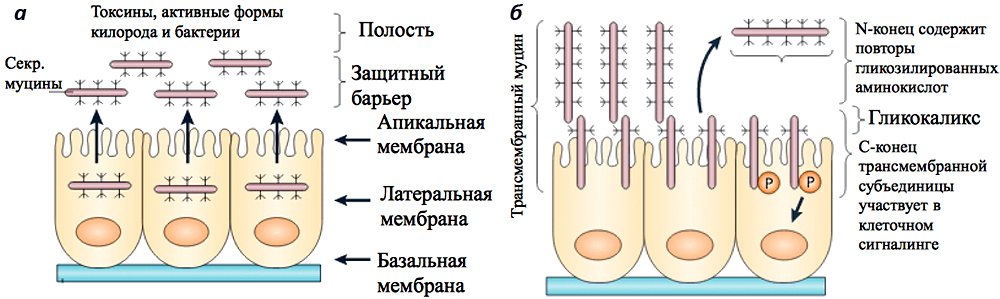
Муцины (от лат. mucus — слизь), или мукопротеины — семейство высокомолекулярных гликопротеинов, содержащих кислые полисахариды. Это семейство очень гетерогенно: молекулярный вес его представителей варьирует в пределах от 0,2 до 10 миллионов дальтон [1]. В своей структуре муцины содержат тандемные повторы из таких аминокислот, как пролин, треонин и серин; именно по двум последним идет гликозилирование [2]. У человека выделяют до 21 вида мукопротеинов, обозначаемых как MUC1, MUC2 и так далее (табл. 1), которые по месту своего расположения в слизи делятся на мембранные и секретируемые формы (рис. 1) [3].
Рисунок 1. Секретируемые и мембранные формы муцинов в защитном барьере эпителия. а — Секретируемые муцины формируют поверхностный защитный гель над эпителиальными клетками. MUC2 — самый распространенный муцин слизистой оболочки желудочно-кишечного тракта. б — Трансмембранные муцины экспонируются на поверхности клеток эпителия, где они представляют собой часть гликокаликса. Участки с тандемными повторами аминокислот на N-конце жестко закреплены над гликокаликсом, и при их отрыве у MUC1 и MUC4 открываются субъединицы муцинов, способные передать в клетку стрессовый сигнал. Рисунок из [2].
| Мембранно-связанные муцины: | Секретируемые муцины: |
|---|---|
| MUC1 — желудок, грудная клетка, желчный пузырь, шейка матки, поджелудочная железа, дыхательные пути, двенадцатиперстная кишка, толстая кишка, почки, глаза, B-клетки, T-клетки, дендритные клетки, эпителий среднего уха | MUC2 — тонкая и толстая кишки, дыхательные пути, глаза, эпителий среднего уха |
| MUC3A/В — тонкая и толстая кишки, желчный пузырь, эпителий среднего уха | MUC5B — дыхательные пути, слюнные железы, шейка матки, желчный пузырь, семенная жидкость, эпителий среднего уха |
| MUC4 — дыхательные пути, желудок, толстая кишка, шейка матки, глаза, эпителий среднего уха | MUC5AC — дыхательные пути, желудок, шейка матки, глаза, эпителий среднего уха |
| MUC12 — желудок, тонкая и толстая кишки, поджелудочная железа, легкие, почки, простата, матка | MUC6 — желудок, двенадцатиперстная кишка, желчный пузырь, поджелудочная железа, семенная жидкость, шейка матки, эпителий среднего уха |
| MUC13 — желудок, тонкая и толстая кишки (включая аппендикс), трахея, почки, эпителий среднего уха | MUC7 — слюнные железы, дыхательные пути, эпителий среднего уха |
| MUC16 — перитонеальный мезотелий, репродуктивные пути, дыхательные пути, глаза, эпителий среднего уха | MUC19 — сублингвальные и субмандибулярные слюнные железы, дыхательные пути, глаза, эпителий среднего уха |
| MUC17 — тонкая и толстая кишки, желудок, эпителий среднего уха | MUC20 — почки, плацента, толстая кишка, легкие, простата, печень, эпителий среднего уха (в некоторых источниках этот муцин относят к мембранно-связанным [1]) |
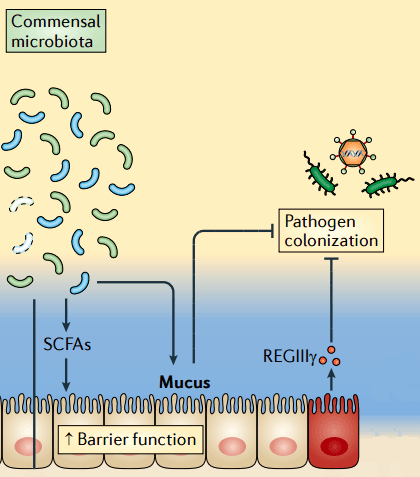
В слизистой оболочке муцины выполняют важную защитную функцию. Они помогают организму очищаться от ненужных субстанций, держать дистанцию от патогенных организмов и даже регулировать поведение микробиоты. В кишечнике, например, мукопротеины участвуют в диалоге между бактериями и эпителиальными клетками слизистой. Микробиота через эпителиальные клетки влияет на продукцию муцинов (рис. 2), а те, в свою очередь, могут участвовать в передаче воспалительных сигналов [4, 5]. К гликанам муцинов прикрепляются бактериофаги, которые тоже вносят свою лепту в регуляцию численности бактерий [6]. Углеводные цепи мукопротеинов прекрасно связывают воду, образуя плотный слой и удерживая таким образом антимикробные белки от смывания в просвет кишечника [7]. Конечно, в слизистой желудочно-кишечного тракта (и не только его) мукопротеины не являются основным защитным механизмом. Помимо муцинов в защите участвуют антимикробные пептиды, секретируемые антитела, гликокаликс и другие структуры.
Рисунок 2. Влияние микробиоты на секрецию слизи. Бактерии — комменсалы толстой кишки в ходе катаболизма неперевариваемых в тонкой кишке углеводов образуют короткоцепочечные жирные кислоты (SCFA, short-chain fatty acids), такие как ацетат, пропионат и бутират, которые повышают продукцию муцинов и защитную функцию эпителия. Рисунок из [5].
При длительном стрессовом воздействии на клетку возможна ее раковая трансформация. Под действием стресса клетка может потерять полярность, в результате чего ее апикальные трансмембранные молекулы, среди которых присутствуют и муцины, начнут экспонироваться на базолатеральных поверхностях. В этих местах муцины — нежелательные гости, так как их неспецифическое связывание с другими молекулами и рецепторами может привести к нарушению межклеточных и базальных контактов. MUC4, например, содержит EGF-подобный домен, способный связываться с тирозинкиназным рецептором соседней клетки и приводить к нарушению плотных контактов [2]. Лишенная связи с окружением, деполяризованная клетка имеет все шансы превратиться в раковую, если уже не является ею.
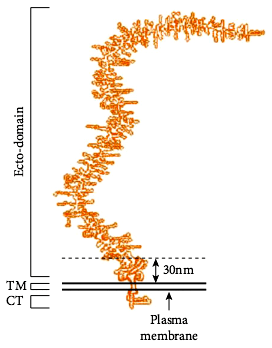
Рисунок 3. Структура мукопротеина MUC1. СТ — цитоплазматический домен, ТМ — трансмембранный домен. Рисунок из [12].
В диагностике некоторых видов злокачественных опухолей изучают профиль производимых клетками муцинов. Дело в том, что экспрессия генов разных типов мукопротеинов во время развития организма имеет специфические пространственно- временные рамки. Однако при онкологических заболеваниях часто наблюдают нерегулируемую экспрессию некоторых из этих генов. Например, MUC1 (рис. 3) в определенном количестве является маркером рака мочевого пузыря [8]. При патологии концентрация MUC1 значительно увеличивается, изменяется и структура мукопротеина. Путем воздействия на клеточный метаболизм через тирозинкиназные и другие рецепторы MUC1 усиливает продукцию факторов клеточного роста [8].
Однако оценка сывороточного уровня MUC1 — не слишком чувствительный, хотя и высокоспецифичный метод диагностики рака мочевого пузыря, для скрининга не подходящий, но для слежения за прогрессией пригодный. Установлено также, что благоприятный исход заболевания связан с гиперпродукцией рецептора к эпидермальному фактору роста HER3 на фоне повышенного содержания MUC1. Только с помощью совокупного анализа этих маркеров можно строить какие-то прогнозы [9].
Дальнейшие исследования, связанные с этим муцином, будут посвящены изучению влияния взаимодействий MUC1 с различными факторами и рецепторами на течение болезни. Кроме того, уже идентифицирован генный локус, ответственный за синтез молекулы MUC1. Этот локус рассматривают в качестве возможной мишени для проведения генной терапии в целях уменьшения риска развития первичной опухоли и ее метастазирования*.
* — Подробно о генетической терапии рассказано в статье «Генная терапия против рака» [10].
Другое исследование выявило, что аномальная экспрессия гена, кодирующего MUC4, является маркером рака поджелудочной железы. Ген этого муцина заметно экспрессировался именно в раковых клетках, но не в тканях нормальной или даже воспаленной железы (при хроническом панкреатите). В качестве основного диагностического метода ученые использовали ПЦР с обратной транскрипцией. Этим же способом они оценили и уровень синтеза мРНК MUC4 в моноцитарной фракции периферической крови пациентов: ведь именно по крови в случае успеха было бы легче всего проводить скрининг в клиниках. Такой анализ оказался достоверным способом выявления панкреатической аденокарциномы на ранних стадиях. У здоровых людей и при опухолях других органов экспрессию гена MUC4 не фиксировали [11].
Открытие того факта, что трансмембранные муцины ассоциированы с клеточной трансформацией и могут способствовать развитию опухоли, положило начало новому направлению в изучении противораковых агентов — пока в доклинических исследованиях.
Увеличение продукции муцинов можно наблюдать при самых разных болезнях, затрагивающих слизистые. Однако в некоторых случаях профиль экспрессии генов разных муцинов, возможно, удастся связать с конкретной патологией. Да и среди многочисленных структурных трансформаций муцинов, характерных для рака, можно выделить те, которые станут наиболее специфичными маркерами для рутинного выявления той или иной опухоли.
Какую роль выполняет слизь в желудке
Желудок выполняет ряд пищеварительных и не пищеварительных функций, нарушение которых в условиях патологии может привести к расстройствам не только желудочного и кишечного пищеварения, но и к развитию анемий, к гормональному дисбалансу, нарушению кислотно-основного состояния, электролитного баланса и другим сдвигам. Основными функциями желудка являются секреторная, моторная, эвакуаторная, резервуарная, экскреторная, всасывательная и инкреторная [1, 2, 4, 5, 7, 8, 9].
Основными анатомическими отделами желудка, отличающимися своими структурными и функциональными особенностями, являются: кардиальный отдел, дно и тело желудка, пилорический отдел. Касаясь секреторной функции желудка, следует отметить способность слизистой секретировать соляную кислоту, бикарбонаты, пепсиногены, гастрин, слизь, однако в различных отделах желудка имеются особенности секреции [7, 8, 9].
Внутренняя поверхность желудка покрыта однослойным высокопризматическим эпителием, непрерывно выделяющим мукоидный секрет, или так называемую видимую слизь, а также бикарбонаты. Барьер видимой слизи составляет 0,5-1,5 мм и обеспечивает защиту подлежащих слоев слизистой от агрессивного действия кислотно-пептического фактора [1, 2, 4, 5, 7, 8, 9].
Кардиальный отдел представляет собой узкое (шириной в 1-4 см) кольцо ниже отверстия пищевода и содержит железы, вырабатывающие мукоидный секрет, здесь же обнаружены париетальные клетки, продуцирующие HCl и внутренний фактор Кастла. Основное количество париетальных или обкладочных клеток, секретирующих НCl и внутренний фактор Кастла, представлено в дне и теле желудка, составляющих 75 % всего желудка. Кроме того, в теле и дне желудка имеются главные зимогенные клетки, вырабатывающие пепсиногены, мукозные клетки, а также аргентофинные клетки. Железы пилорического отдела, составляющего 15-20 % желудка, содержат клетки, вырабатывающие слизь. Особенностью этого отдела является наличие в нем G-клеток, продуцирующих гастрин [7, 8, 9].
В различных отделах желудка выделяют так называемые промежуточные клетки, выделяющие мукоидный секрет и бикарбонаты. Эти клетки обладают высокой митотической активностью и являются камбием для всего эпителия желудка. Главные и часть париетальных клеток не обладают митотической активностью, их восполнение обеспечивается за счет пролиферации и созревания камбиальных клеток. По всей территории желудка в глубоких слоях слизистой располагаются аргентофинные клетки, продуцирующие 5-окситриптамин (предшественник серотонина) и другие биологически активные вещества. Тучные клетки соединительной ткани продуцируют гистамин, серотонин, гепарин, фактор активации тромбоцитов (ФАТ), фактор хемотаксиса эозинофилов (ФХЭ), фактор хемотаксиса моноцитов (ФХМ) и другие цитокины [4, 5, 6].
Иннервация желудка обеспечивается экстрамуральными нервами (блуждающим, чревным, диафрагмальным) и интрамуральной нервной системой [7, 8, 9].
Парасимпатическая иннервация осуществляется блуждающими нервами, содержащими преганглионарные волокна и оканчивающимися в миэнтеральном сплетении на клетках Догеля I типа – втором нейроне парасимпатической иннервации.
Симпатическая иннервация осуществляется волокнами, идущими в составе ваго-симпатических стволов блуждающих нервов и волокон чревных нервов, достигающих желудка совместно с брыжеечными нервами [7, 8, 9].
Метасимпатическая система регуляции основных функций желудка представлена подслизистым сплетением (мейснерово), слизистым, межмышечным (ауэрбахово) и субсерозным.
В свою очередь, активность метасимпатической системы желудка находится под преимущественным регулирующим влиянием n.vagus.
Характеристика фаз желудочной секреции
Различают базальную (голодную) и стимулированную (пищеварительную) секрецию. Секреция желудочного сока натощак составляет у взрослого человека 10 % того количества, которое образуется при максимальной стимуляции. Перерезка блуждающего нерва или удаление антрального отдела, содержащего G-клетки, приводит к прекращению базальной секреции, из чего следует, что она стимулируется гастрином и зависит от тонуса блуждающего нерва [1, 2, 4, 5, 7, 8, 9].
В процессе желудочной секреции выделяют три фазы:
1) сложнорефлекторную (цефалическую);
Клетки желудочных желез ежесуточно секретируют 2-3 литра желудочного сока. По своему составу желудочный сок на 99-99,5 % состоит из воды и 1-0,5 % составляет плотный остаток, представленный неорганическими (хлориды, сульфаты, фосфаты, бикарбонат натрия, ионы калия, кальция, магния) и органическими (ферменты, мукоиды) веществами. В небольшом количестве в желудочном соке находятся азотсодержащие вещества небелковой природы (мочевина, мочевая кислота, молочная кислота) [5, 7, 8, 9].
Афферентная стимуляция цефалической фазы желудочной секреции осуществляется при участии различных анализаторов – вкусового, обонятельного, зрительного, слухового.
Эфферентное звено регуляции первой фазы желудочной секреции обеспечивается холинэргическими нервными волокнами, ацетилхолином, освобождаемым интрамуральными нервными сплетениями. Латентный период первой фазы составляет 5-10 минут. В цефалическую фазу выделяется около 45 % желудочного сока, богатого ферментами.
Основными эфферентными регуляторами сложнорефлекторной фазы являются: холинергические нервные влияния, ацетилхолин, а также гастрин, высвобождающийся при активации n. vagus [5, 7, 8, 9].
Стимуляторами желудочной фазы секреции являются механические факторы (растяжение желудка поступающей в него пищей) и химические раздражения слизистой желудка, приводящие к активации холинергических влияний и усилению продукции ацетилхолина и гастрина.
Различают гастрин 17 и гастрин 34. Гастрин 17 обладает наибольшей активностью, гастрин 34 имеет более продолжительный период существования, но в шесть раз меньшую активность. Гастрин 17 в большей мере оказывает местный стимулирующий эффект на секреторную активность желудка при участии антрофундального кровотока. Гастрин 34, всасываясь в системный кровоток, регулирует оксигенацию и трофику слизистой желудочно-кишечного тракта. Гастрин 34 синтезируется клетками 12-перстной кишки и поджелудочной железы и при триптическом гидролизе расщепляется с образованием гастрина 17, 14, 13. Гастрин 14 и гастрин 13 обнаруживаются в небольших количествах, и биологическая значимость их неясна. Стимулируют инкрецию гастрина ацетилхолин, механическое растяжение антрального отдела, продукты протеолиза, катехоламины через a-адренорецепторы, ионы кальция, магния, алкоголь, кофеин [1, 2, 4, 5, 7, 8, 9].
Третья фаза желудочной секреции – кишечная – продолжается 1-3 часа развивается при переходе пищи из желудка в кишечник. Кишечная фаза поддерживается механическим растяжением тонкого кишечника и химическим раздражением хеморецепторов слизистой 12-перстной кишки продуктами гидролиза пищи и сопровождается освобождением различных биологически активных соединений – гастрина, энтерогастрона, соматостатина, секретина, холецистокинина, гастроингибирующего пептида, мотилина, нейротензина и другие [1, 2, 4, 5, 7, 8, 9].
К числу медиаторов, играющих роль первых посредников в индукции секреции желудочного сока, относятся ацетилхолин, гистамин и гастрин.
Как известно, важнейшими компонентами желудочного сока являются НСl, пепсиногены и слизь.
НСl вырабатывается париетальными клетками, расположенными в перешейке, шейке и верхнем отделе тела железы. Эти клетки характеризуются исключительным богатством митохондрий вдоль секреторных внутриклеточных канальцев. В состоянии покоя париетальных клеток секреторные канальцы выражены слабо, вместо них имеются особые пузырчатые образования – тубуловезикулы. В периоды секреторной активности в процессе пищеварения количество секреторных канальцев увеличивается, их мембрана сливается с плазматической мембраной, увеличивая тем самым ее площадь. Кислотопродуцирующие клетки желудка активно используют собственный гликоген для нужд секреторного процесса. Секреция НСl – ярко выраженный цАМФ-зависимый процесс, активация которого протекает на фоне усиления гликогенолитической и гликолитической активности. Кислотообразующая функция обкладочных клеток характеризуется наличием в них процессов фосфорилирования-дефосфорилирования, существованием митохондриальной окислительной цепи, транспортирующей ионы водорода из матриксного пространства, а также (Н-К)-АТФазы секреторной мембраны, перекачивающей протоны из клетки в просвет железы за счет энергии АТФ. Вода поступает в канальцы клетки путем осмоса [5, 7, 8, 9].
В полости желудка НСl стимулирует секреторную активность желез желудка, способствует превращению пепсиногена в пепсин, создает оптимальное рН для действия протеолитических ферментов желудочного сока, вызывает денатурацию и набухание белков. Кроме того, HCl стимулирует продукцию секретина в двенадцатиперстной кишке, обеспечивает антибактериальное действие вместе с лизоцимом и сиаломуцинами, а также стимулирует моторную функцию желудка и регулирует работу пилорического сфинктера [7, 8, 9].
При ахлоргидрии содержание микроорганизмов в 1 мл желудочного сока возрастает до 100000 (в норме в 1 мл содержится 100 микробных клеток).
Основным ферментативным процессом в полости желудка является начальный гидролиз белков до альбумоз и пептонов с образованием небольшого количества аминокислот. В желудочном соке выделено 7 видов пепсинов, продуцируемых главными клетками.
Основными пепсинами желудочного сока являются:
Пепсин А – группа ферментов, гидролизирующих белки при рН = 1,5- 2,0. Около 1 % пепсина переходит в кровяное русло, фильтруется в почках и выделяется с мочой (уропепсин).
Гастриксин, пепсин С, желудочный катепсин. Соотношение между пепсином А и гастриксином в желудочном соке от 1:1 до 1:5. Оптимум действия фермента при рН = 3,2-3,5.
Пепсин В, парапепсин, желатиназа – разжижает желатину, расщепляет белки соединительной ткани. Оптимум действия фермента при рН до 5,6.
Ренин, пепсин Д, химозин – расщепляет казеин молока в присутствии ионов Са, с образованием параказеина и сывороточного белка.
Пепсины не продуцируются железами антрального отдела желудка, гастриксин же присутствует во всех отделах желудка.
Желудочный сок содержит ряд непротеолитических ферментов – желудочную липазу, лизоцим, муколизин, карбоангидразу, уреазу. Лизоцим вырабатывается клетками поверхностного эпителия и придает бактерицидные свойства желудочному соку.
Желудочный сок обладает небольшой амилолитической и липолитической активностью. Не исключено, что амилаза и липаза рекретируются фундальными и пилорическими железами из крови. В желудочном соке обнаружены и другие непротеолитические ферменты: трансаминазы, аминопептидазы, щелочная фосфатаза, рибонуклеазы и другие [5, 7, 8, 9].
Важнейшим протективным фактором желудка от воздействия НСl и пепсинов является слизеобразование.
Желудочная слизь, или муцин, вырабатывается клетками поверхностного цилиндрического эпителия, добавочными клетками шеек желез дна и тела, мукоидными клетками кардиальных и пилорических желез.
Желудочная слизь состоит из нерастворимой видимой и растворимой слизи. Видимая слизь – высокогидратированный гель, содержит нейтральные мукополисахариды, сиаломуцины, гликопротеиды, протеогликаны, протеины. Растворенный муцин образуется из секрета желудочных желез и продуктов переваривания видимой слизи [5, 7, 8, 9].
Адсорбционная и антипептическая способность слизи, обусловленная наличием сиаловых кислот, обеспечивает защиту слизистой от самопереваривания. Гликопротеиды, входящие в состав видимого муцина, совершенно резистентны к протеолизу. Слизь обладает значительной буферной емкостью и способностью нейтрализовать кислоту за счет наличия бикарбонатов и фосфатов, которые секретируются вместе со слизью и адсорбируются на ней. Образующийся при взаимодействии муцина и бикарбоната мукозо-бикарбонатный барьер предохраняет слизистую от аутолиза, создает такую среду, в которой большинство макромолекул нерастворимы. Такой барьер непроницаем для бактериальных олигопептидов.
Кислые мукополисахариды – протеогликаны обеспечивают липотропную активность слизи, предотвращая ожирение печени. Биологическое действие фукомуцинов (нейтральных муцинов), составляющих основную массу видимой и растворимой слизи, связано с наличием в их составе групповых антигенов крови, фактора роста и антианемического фактора Кастла.
Сиаломуцины участвуют в синтезе НCl, они способны нейтрализовать вирусы и препятствовать вирусной гемаглютинации.
Выделение слизи стимулируют умеренные концентрации катехоламинов, гистамин, гастрин, серотонин, механическое раздражение слизистой. Усиливают образование слизи простациклин, а также простагландины (РgE1, PgE2), улучшающие кровоснабжение слизистой оболочки. Простагландины F2b стабилизируют мембраны лизосом эпителия, препятствуя его десквамации, и являются мембранопротекторами. АКТГ, глюкокортикоиды подавляют слизеобразование [3, 5, 6, 9].
Характер и механизмы нервных и гормональных влияний на желудочную секрецию
Ацетилхолин стимулирует деятельность главных, обкладочных и мукозных клеток через М-холинорецепторы, а также за счет стимуляции освобождения гастрина G-клетками. Кроме того, ацетилхолин подавляет активность D-клеток и продукцию соматостатина-ингибитора желудочной секреции. В ткани желудка под действием ацетилхолина и гастрина из ECL-клеток и тучных клеток выделяется гистамин, который через Н2 – рецепторы активирует аденилатциклазу с последующей стимуляцией (Н-К)-АТФ-азы. Этот фермент обеспечивает электронейтральный обмен ионов калия на ионы водорода. В равной степени гистамин стимулирует секрецию бикарбонатов и слизи. Стимулирующим влиянием на процесс желудочной секреции обладают простагландины F 2α, высвобождающиеся под влиянием ацетилхолина [1, 2, 4, 5, 7, 8, 9].
Эффекты катехоламинов на секреторную способность желудка, по данным ряда авторов, весьма противоречивы: через β1-адренорецепторы подавляется продукция НСI; через β2-адренорецепторы подавляется продукция пепсиногена. Действуя через α-адренорецепторы, катехоламины вызывают ограничение кровотока в слизистой желудка, активацию G-клеток и усиление продукции гастрина. Последнее приводит к повышению секреторной способности желудка.
В настоящее время очевидно значение ряда гормональных и гуморальных факторов, оказывающих модулирующее влияние на секреторную функцию желудка. Гормональными факторами, стимулирующими желудочную секрецию, являются АКТГ, глюкокортикоиды, СТГ, пролактин, инсулин, глюкагон, паратгормон. К гормональным и гуморальным ингибиторам желудочной секреции относятся вазопрессин, окситоцин, тиреокальцитонин, эндогенные опиоидные пептиды, ВИП, ГИП и другие факторы [1, 2, 4, 5, 7, 8, 9].
Важную роль в регуляции желудочной секреции играют биологически активные вещества и тканевые гормоны, причем гистамин, простагландины групп В, F оказывают стимулирующее воздействие на желудочную секрецию, в то время как простагландины типа Е, А и простациклин подавляют секрецию кислоты и пепсина [5, 7, 8, 9].
Что касается серотонина – важного медиатора воспалительных реакций – он оказывает неоднозначное действие на желудочную секрецию: стимулирует действие главных клеток и подавляет активность обкладочных [1, 2, 4, 5].
Ниже представлены особенности влияния ряда гормонов и гуморальных модуляторов секреторной, моторной и эвакуаторной функции желудка.
Холецистокинин – продуцируется в G-клетках тонкой кишки под влиянием пептидов, аминокислот, жирных кислот. Холецистокинин стимулирует секрецию секрецию желудочного сока, панкреатических ферментов, инсулина, моторику желчного пузыря, кишечника и тормозит эвакуаторную активность желудка.
Мотилин – является дигестивным пептидом, продуцируется энтерохромафинными клетками тонкого кишечника (ЕС2-клетками), стимулирует секрецию пепсиногена главными клетками желудка, вызывает тоническое сокращение желудка и кишечника. Мотилин потенцирует действие ацетилхолина на пилорический отдел желудка и ускоряет эвакуацию химуса.
Секретин – продуцируется S-клетками проксимального отдела тонкого кишечника. Секретин стимулирует секрецию пепсиногена главными клетками желудка, тормозит продукцию соляной кислоты париетальными клетками. Секретин стимулирует освобождение бикарбонатов и воды поджелудочной железой, печенью, дуоденальными железами, усиливает секрецию желчи и кишечного сока, потенцирует действие холецистокинина на моторику желчного пузыря.
Важнейшим регулятором желудочной секреции является соматостатин, продуцируемый D-клетками желудочно-кишечного тракта, а также нервными клетками центральной и периферической нервной системы. Стимуляция инкреции соматостатина происходит под влиянием пептонов, кислого содержимого. Реципрокные отношения отмечены между продукцией соматостатина, гастрина, ацетилхолина.
Соматостатин ингибирует секрецию СТГ, ТТГ, пролактина, инсулина, глюкагона, а также ряда дигестивных пептидов – гастрина, холецистокинина. Снижение содержания соматостатина в слизистой оболочке антрального отдела выявлено у больных с рецидивирующей язвой двенадцатиперстной кишки [1, 2, 4, 5].
У пациентов со соматостатинпродуцирующими опухолями выявлено снижение секреторной активности желудка.
Ингибирующим влиянием на секреторную активность желудка обладают:
Гастроингибирующий пептид (ГИП) – тормозный полипептид, синтезируется в эндокриноцитах (К-клетках) тонкой кишки под влиянием липидов, снижает секрецию НСI, угнетает реабсорбцию натрия и воды в ЖКТ, стимулирует секрецию инсулина, ингибирует моторику желудка. ГИП активирует секреторную деятельность толстого кишечника. Усиление секреции ГИП выявлено при диабете 2-типа, демпинг-синдроме.
Нейротензин образуется в N-клетках слизистой оболочки подвздошной кишки, в гипоталамусе и базальных ганглиях, высвобождение нейротензина в кишечнике происходит под влиянием липидов. Нейротензин ингибирует двигательную и секреторную функцию желудка, стимулирует секрецию бикарбонатов поджелудочной железой и освобождение глюкагона.
Пептид YY синтезируется эндокриноцитами толстой и тонкой кишки, угнетает секреторную функцию желудка и поджелудочной железы, тормозный медиатор для верхних отделов пищеварительной трубки.
Энтероглюкагон – синтезируется в ЕСI-клетках слизистой оболочки кишечника, особенно подвздошной и толстой кишки; его секреция возрастает под влиянием триглицеридов и углеводов. Энтероглюкагон угнетает моторику желудка, снижает образование соляной кислоты париетальными клетками. Энтероглюкагон обладает трофическим влиянием на слизистую кишечника.
Нейропептиды могут оказывать как активирующее, так и тормозное влияние на секреторную и моторную функции желудка.
Вазоактивный интестинальный пептид (ВИП) – содержится в больших нейросекреторных гранулах типа Р. Он подавляет секрецию соляной кислоты и пепсиногена клетками желудка, активирует кровоток в стенке кишечника, секрецию кишечного сока и бикарбоната поджелудочной железой. ВИП стимулирует инкрецию инсулина, усиливает гликогенолиз в печени. ВИП обладает выраженным вазодилятаторным и гипотензивным эффектом.
Бомбезин – гастринстимулирующий полипептид – GRP, продуцируется в нервных волокнах желудочно-кишечного тракта и клетках ЦНС. Стимулирует продукцию соляной кислоты, пепсиногена, гастрина, панкреатического сока. Бомбезин способствует выделению энтероглюкагона, холецистокинина, субстанции Р, панкреатического полипептида, соматостатина.
Субстанция Р – относится к нейропептидам, выделяется нервными окончаниями интрамускулярного нервного сплетения ЖКТ, а также клетками головного и спинного мозга. Субстанция Р усиливает слюноотделение, оказывает стимулирующее действие на моторику пищеварительного тракта, участвует в передаче информации о боли с периферии в центральную нервную систему.
Энкефалины и эндорфины – эндогенные опиоидные пептиды, образуются в гипоталамических структурах, слизистой двенадцатиперстной кишки, поджелудочной железе, надпочечниках. Они оказывают тормозное влияние на секреторную и моторную функции желудка и кишечника путем блокады освобождения ацетилхолина и субстанции Р клетками этих отделов.
Нейропептид Y образуется клетками центральной и периферической нервной системы, угнетает секрецию ацетилхолина в нервных окончаниях желудочно-кишечного тракта, а следовательно, секреторную и моторную функцию ЖКТ.
Тиролиберин – образуется в гипоталамусе, аденогипофизе, клетках ЖКТ, почках, печени, плаценте, сетчатке глаза. Тиролиберин угнетает образование НСI в желудке и моторику желудка.