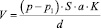какую функцию выполняет сурфактант выстилающий альвеолы изнутри
Какую функцию выполняет сурфактант выстилающий альвеолы изнутри
2.1. Дыхательные функции легких. Альвеолярное дыхание
Легкие играют важную роль не только в регуляции и обеспечении внешнего дыхания, но выполняют и ряд недыхательных функций. Недыхательные функции легких включают их участие в голосообразовании, регуляции теплоотдачи и кислотно-основного состояния организма, иммунных реакциях, в обеспечении тканевого фагоцитоза, регуляции метаболизма биологически активных прессорных и депрессорных субстанций, прокоагулянтных и антикоагулянтных факторов свертывания крови. В легких инактивируются пептиды, цикличесские нуклеотиды, простагландины, ксенобиотики, а также гистамин, серотонин.
Дыхательная функция легких определяется их участием в обеспечении альвеолярного дыхания, а также в регуляции внешнего дыхания за счет наличия мощных рефлексогенных зон.
Состояние легочной вентиляции определяется глубиной дыхания (дыхательным объемом) и частотой дыхательных движений.
Различают следующие объемы дыхания:
Дыхательный объем – объем вдоха и выдоха при спокойном дыхании.
Резервный объем вдоха и выдоха – количество воздуха, которое человек может дополнительно вдохнуть или выдохнуть при нормальном дыхании.
Остаточный объем – количество воздуха, оставшегося в легких, после максимального выдоха.
Жизненная емкость легких (ЖЁЛ) – наибольшее количество воздуха, которое можно максимально выдохнуть после максимального вдоха (сумма дыхательного объема и резервных объемов вдоха и выдоха)
Функциональная остаточная емкость – количество воздуха, оставшееся в легких после спокойного выдоха.
Жизненную ёмкость легких можно вычислить по формуле ЖЁЛ (л)= 2,5*рост (в м).
ЖЁЛ зависит от роста, возраста человека, рода занятий, особенно велико у пловцов и гребцов (до 8 л).
Легкие плода и новорожденных, не совершивших первый вдох, не содержат воздуха.
Различают анатомическое и функциональное мертвое пространство.
Анатомическое мертвое пространство – это объем невентилируемых воздухоносных путей – трахеи, бронхов и бронхиол.
Функциональное мертвое пространство – более емкое понятие, оно включает не только анатомическое мертвое пространство, а также вентилируемые, но неперфузируемые альвеолы.
Минутный объем дыхания равен произведению дыхательного объема на частоту дыхательных движений. Частота дыхательных движений у детей различна: у новорожденных составляет 40-50 в мин, у грудных детей 30-40 в мин, в детском возрасте 20-30 в мин. У взрослого человека частота дыхательных движений составляет 14 – 18 в мин.
Следует отметить, что диффузионное давление для О2 составляет около 60 мм. рт.ст, а для СО2 около 6 мм.рт.ст. Однако, необходимо учесть, что СО2 значительно быстрее диффундирует через альвеолярно–капиллярную мембрану в связи с тем, что коэффициент его растворимости в биологической среде в 20 раз больше, чем у кислорода.
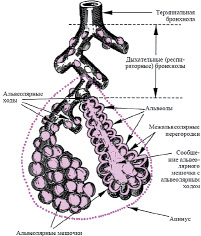
В легких взрослого человека содержится около 300 млн. альвеол, диаметр которых составляет около 0,2 мм. Две соседние альвеолы отделены друг от друга двумя слоями эндотелия и эпителия, расположенными на базальной мембране. Между этими слоями находится интерстициальное пространство. Альвеолярный эпителий и эндотелий капилляров образуют альвеолярно – капиллярную мембрану, через которую происходит диффузия газов; толщина мембраны составляет от 0,2 мкм до 2 мкм в местах скопления эластических и коллагеновых волокон. Площадь газообмена в легких находится в зависимости от возраста и колеблется от 40 до 140 м 2 (рис.4).
Рис.4. Схема строения альвеолярного дерева
Альвеолярно–капиллярная диффузия во многом зависит от эластичности легочной ткани, обеспечивается в значительной мере продукцией сурфактанта.
Различают два типа эпителия, выстилающего альвеолярные клетки. Клетки I типа – это плоский эпителий, занимает до 95 % площади альвеолярной поверхности, содержит небольшое количество органоидов. Клетки IIтипа крупные, имеют округлую форму, ядра и микроворсинки, синтезируют сурфактант.
Сурфактант легких – это смесь поверхностно-активных веществ (ПАВ), состоящая на 70 – 80% из фосфатидилхолина, фосфатидилглицерола, дипальмитолфосфатидилхолина и белков сурфактанта, продуцируемых альвеолоцитами II типа. Молекулы апопротеинов, фосфолипидов имеют гидрофильный и гидрофобные концы, обращенные соответственно в альвеолярную жидкость и альвеолярный воздух. Белки сурфактанта (SPA, SP-R, SP-C,SP-D) не только способствуют снижению поверхностного натяжения альвеол, обеспечиваемому фосфолипидами, но и обладают защитной функцией.
Система легочного сурфактанта играет многоплановую роль, обеспечивая антиателэктатическую функцию, способствует диффузии О2, участвует в регуляции водного обмена в легких, защищает организм от проникновения вредоносных мелкодисперсных аэрозолей, обладает свойствами антиоксиданта.
Сурфактант, как указывалось выше, уменьшает поверхностное натяжение альвеол в 2 – 10 раз, тем самым, предотвращая спадение альвеол. Сурфактант содержится не только на внутренней поверхности альвеол, но и на плевре, брюшине, перикарде, синовиальных оболочках, слизистой глазных яблок. Сурфактант обеспечивает раскрытое состояние мелких дыхательных путей, усиливает фагоцитирующую активность макрофагов, подавляет выделение медиаторов воспаления, обладает свойствами антиоксиданта, оказывает антибактериальное и противовирусное действие.
При дефиците сурфактанта некоторые альвеолы подвергаются ателектазу, другие – перерастягиваются, вентиляция легких становится негомогенной, нарушается вентиляционно – перфузионное отношение.
При спадении альвеолы концентрация сурфактанта на ее поверхности возрастает, возникает снижение поверхностного натяжения, что повышает их стабильность и препятствует дальнейшему спадению альвеол. Стабильность альвеол обеспечивается и так называемым феноменом «взаимозависимости» альвеол, т.е. их взаимной тяги. У недоношенных новорожденных недостаточность синтеза сурфактанта может быть причиной развития респираторного дистресс – синдрома, характеризующегося ригидными легкими.
Как известно, легкие в отличие от трахеи и бронхов являются мощной рефлексогенной зоной, обеспечивающей регуляцию внешнего дыхания в условиях нормы и патологии.
В паренхиме легких имеются различные высоко- и низкочувствительные рецепторы растяжения альвеол, медленно-адаптирующиеся и быстро-адаптирующиеся к структурным изменениям в легких. Медленно-адаптирующиеся рецепторы растяжения альвеол являются высокочувствительными, низкопороговыми механорецепторами, реагирующими на объем вдыхаемого воздуха. Эти рецепторы являются окончанием толстых миелинизированных волокон n.vagus. Афферентация с этих рецепторов при участии ретикулярной формации ствола мозга переключается на инспираторные нейроны дорзальной дыхательной группы продолговатого мозга, обеспечивая развитие рефлекса Геринга-Брейера. Рефлекс Геринга-Брейера участвует во время сна в смене фаз дыхательного цикла. В условиях патологии при участии этого рефлекса формируются испираторная, экспираторная и смешанная одышки.
Другой группой рецепторов паренхимы легких являются быстроадаптирующиеся рецепторы спадения альвеол и юкстакапилярные рецепторы, реагирующие соответственно на спадение альвеол и возрастание уровня тканевой жидкости. Импульсация с этих рецепторов проводится по мало– и немиелинизированным волокнам n.vagus в продолговатый мозг, вызывая развитие тахипное.
При раздражении С-волокон возникают брадикардия, тахи- и апное, гипер- и диссекреция слизи в воздухоносных путях.
2.2. Кровоснабжение и лимфоснабжение легких
Легкие получают кровь от системы легочных сосудов (малый круг кровообращения) и бронхиальных сосудов (большой круг кровообращения). Основной функцией малого круга кровообращения является оксигенация венозной крови и удаление из нее СО2.
Среднее время прохождения крови через малый круг составляет в среднем 4,5 – 5,0 сек.
В состоянии покоя в сосудах легких находится около 500 мл крови (10 % от общего объема). В условиях нагрузки объем крови в легких может возрастать в 5–6 раз, при этом происходит лишь незначительное увеличение давления в сосудах малого круга кровообращения за счет высокой растяжимости. Давление в артериолах легких составляет в среднем 9 – 15 мм. рт. ст.
В покое кровоток в легких неоднороден, большая часть его направлена в нижние зоны.
Система бронхиальных сосудов снабжает кровью дыхательные пути вплоть до терминальных бронхиол, составляя около 3% от величины легочного кровотока.
Гидродинамические параметры бронхиальных сосудов обеспечивают транспорт воды в интерстиций и последующее лимфообразование. В легких осуществляются анастомозы между сосудами большого и малого круга кровообращения.
Суммарно в легких отношение легочной вентиляции и легочной перфузии составляет примерно 0,8 – 1,0. При вертикальном положении человека снижается интенсивность кровотока у верхушек легких.
Лимфатические сосуды расположены в паренхиме легких и на поверхности висцеральной плевры, впадают в лимфатические узлы, расположенные вокруг крупных воздухоносных путей (ВП) и в средостении. Лимфоидная ткань находится в стенках воздухоносных путей. Терминальные мешки лимфатической системы расположены в субплевральной, перибронхиальной соединительной ткани, а затем поступают в собирательные лимфатические сосуды легких.
Регуляция легочного кровотока обеспечивается за счет влияния вегетативной нервной системы, а также ряда гуморальных факторов; в частности вазодилатирующих простагландина J2 – метаболита арахидоновой кислоты, оксида азота и вазоконстрикторных соединений: эндотелинов, тромбоксана.
Эндотелины продуцируются эндотелиальными клетками легочных сосудов и клетками бронхиального эпителия и вызывают вазоконстрикцию, являются медиаторами легочной гипоксической вазоконстрикции, вызывают сокращения гладкой мускулатуры воздухоносных путей.
Сурфактант-БЛ (Surfactant-BL)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Сурфактант-БЛ
Лиофилизат для приготовления эмульсии для ингаляционного введения в виде спрессованной в таблетку массы или порошка белого или белого с желтоватым оттенком цвета, приготовленная эмульсия белого с кремоватым или белого с желтоватым оттенком цвета, однородная, в которой не должны наблюдаться хлопья или твердые частицы.
| 1 фл. | |
| сурфактант | 25 мг |
Фармакологическое действие
Высокоочищенный природный сурфактант, полученный из крупного рогатого скота.
Комплекс веществ из смеси фосфолипидов и сурфактант-ассоциированных белков; снижает поверхностное натяжение легочных альвеол, предотвращая их коллапс и развитие ателектазов. Восстанавливает содержание фосфолипидов на поверхности альвеолярного эпителия, стимулирует вовлечение в дыхание дополнительных участков легочной паренхимы; способствует удалению вместе с мокротой токсических веществ из альвеолярного пространства. Повышает активность альвеолярных макрофагов и угнетает экспрессию и экскрецию цитокинов полиморфноядерными лейкоцитами; стимулирует синтез эндогенного сурфактанта альвеолоцитами II типа и защищает альвеолярный эпителий от повреждений химическими и физическими агентами.
При ингаляционном введении не оказывает влияния на ССС, не оказывает местнораздражающего действия, не влияет на состав крови и кроветворение за исключением кратковременной (1 сут после прекращения введения препарата в дозах 200 и 400 мг/кг) лимфопении и гранулоцитоза за счет увеличения числа палочко- и сегментоядерных нейтрофилов. В дальнейшем состав периферической крови полностью нормализуется. Не влияет на биохимические параметры крови, мочи и свертывающую систему крови, не вызывает патологических изменений функций и структуры внутренних органов.
У недоношенных новорожденных с респираторным дистресс-синдромом эндотрахеальное введение препарата при ИВЛ улучшает газообмен в легочной ткани. Через 30-120 мин после введения уменьшаются признаки гипоксемии, повышается парциальное давление кислорода в артериальной крови и насыщение Hb кислородом, а также уменьшается гиперкапния (парциальное давление углекислого газа), что позволяет перейти на более физиологичные параметры ИВЛ (снизить токсические концентрации кислорода во вдыхаемой газовой смеси до 40%, а также уменьшить общую продолжительность аппаратного дыхания). Значительно снижает летальность и частоту осложнений у новорожденных с респираторным дистресс-синдромом.
Фармакокинетика
Через 6-8 ч после однократного интратрахеального введения концентрация сурфактанта в легких снижается и достигает исходной величины через 12 ч.
Препарат полностью утилизируется в легких и не кумулирует в организме.
Показания активных веществ препарата Сурфактант-БЛ
Респираторный дистресс-синдром новорожденных; синдром острого повреждения легких и респираторный дистресс-синдром у взрослых (в т.ч. на фоне множественной травмы, сепсиса, аспирации желудочного содержимого, эндогенной интоксикации, массивной кровопотери и множественных гемотрансфузий, применения АИК в ходе кардиохирургических операций, тяжелой пневмонии).
Режим дозирования
Правила приготовления эмульсии
Непосредственно перед введением 75 мг лиофилизированного порошка разводят 2.5 мл 0.9% раствора натрия хлорида д/и. Для этого вносят во флакон 2.5 мл теплого (36°С) 0.9% раствора натрия хлорида и дают флакону постоять 2-3 мин, затем суспензию осторожно перемешивают во флаконе, не встряхивая, набирают эмульсию в шприц тонкой иглой, выливают обратно во флакон по стенке несколько раз (4-5) до полного равномерного эмульгирования, избегая образования пены. Флакон нельзя встряхивать. После разведения образуется молочного цвета эмульсия, лишенная хлопьев или твердых частиц.
Новорожденного предварительно интубируют и непосредственно перед введением Сурфактанта-БЛ аспирируют мокроту из дыхательных путей и эндотрахельной трубки. Через адаптер с дополнительным боковым входом в трахею с помощью шприцевого насоса или капельно, в течение 60-90 мин, проводят инфузию приготовленного препарата. Для равномерного распределения сурфактанта по различным отделам легких, во время инфузии препарата ребенку, если позволяет тяжесть состояния, на несколько минут осторожно меняют положение тела: поворот на правый-левый бок, подъем головного конца. Заканчивают процедуру несколькими принудительными вдохами больного. Желательно не проводить санацию трахеи в течение нескольких часов после введения сурфактанта.
Аэрозольное введение осуществляют с помощью небулайзера, включенного в контур аппарата ИВЛ максимально близко к эндотрахеальной трубке для уменьшения потерь препарата. Желательно использовать аппараты, позволяющие подавать аэрозоль сурфактанта синхронно с вдохом. Для получения аэрозоля и введения препарата необходимо использовать только не УЗ-бронхоальвеолярные небулайзеры, т.к. сурфактант разрушается при обработке эмульсии УЗ.
Синдром острого повреждения легких и респираторного дистресс-синдрома взрослых : эндобронхиально, с помощью фибробронхоскопа, в дозе 12 мг/кг массы тела в сутки, разделенной на 2 введения по 6 мг/кг, выполняемых через 12-16 ч. Препарат вводится в виде 1.5% эмульсии (15 мг в 1 мл 0.9% раствора натрия хлорида).Может потребоваться многократное введение препарата (4-6 введений) до стойкого улучшения газообмена (до увеличения индекса оксигенации более 300 мм рт.ст.), рентгенологической картины и возможности проведения ИВЛ с FiO2 менее 40%.
В большинстве случаев продолжительность курса применения Сурфактанта-БЛ не превышает двух суток. У 10-20% пациентов назначение препарата не сопровождается нормализацией газообмена (особенно больных с выраженной полиорганной недостаточностью). Если в течение 2 дней не происходит улучшение оксигенации, введение препарата прекращают.
Правила приготовления эмульсии
75 мг лиофилизированного порошка разводят так же, как для новорожденных, в 2.5 мл 0.9% раствора натрия хлорида. Полученную эмульсию разводят дополнительно 0.9% раствора натрия хлорида до 5 мл, получая 1.5% эмульсию препарата (15 мг в 1 мл 0.9% раствора натрия хлорида).
Эндобронхиальному введению препарата предшествует тщательная санационная бронхоскопия, проводимая по стандартной методике, в конце которой в каждое легкое вводится равное количество эмульсии препарата. Наилучший эффект достигается при введении эмульсии в каждый сегментарный бронх. Объем вводимой эмульсии определяется дозой препарата.
Интратрахеальная инстилляция показана в случае отсутствия возможности проведения бронхоскопии. Эмульсия готовится по описанному выше способу. До введения препарата необходимо провести тщательную санацию трахеобронхиального дерева, предварительно приняв меры для улучшения дренирования мокроты (вибромассаж, постуральная терапия, муколитики при отсутствии противопоказаний к их назначению). Эмульсию вводят через катетер, устанавливаемый в эндотрахеальную трубку так, чтобы конец катетера располагался ниже отверстия эндотрахеальной трубки, но обязательно выше киля трахеи. Эмульсию необходимо вводить в 2 приема (разделив дозу пополам), с интервалом 10 мин.
Побочное действие
Противопоказания к применению
Внутрижелудочковые кровоизлияния III-IV ст. у новорожденных; пневмоторакс; пневмомедиастинум; интерстициальная эмфизема; нарушения газообмена, связанные с недостаточностью ЛЖ и бронхообструкцией.
Экзогенный сурфактант в комплексном лечении тяжелой пневмонии, вызванной вирусом SARS-CoV-2
Полный текст:
Аннотация
Актуальность. Экспериментальные и клинические подтверждения эффективности препаратов сурфактанта при гриппе А/Н1N1 послужили предпосылками для использования экзогенного сурфактанта при лечении пациентов с тяжелым течением COVID-19. Цель исследования. Анализ результатов применения препарата сурфактанта при лечении тяжелой пневмонии, вызванной SARS-CoV-2. Материалы и методы. Представлены данные ретроспективного контролируемого исследования, в которое вошли 68 пациентов с тяжелым течением вирусной пневмонии. Критерии включения: подтвержденная инфекция SARS-CoV-2; двусторонняя пневмония с поражением не менее 2 ст. по данным КТ; SpO2 менее 92 % при ингаляции кислорода через лицевую маску с потоком ≥ 6 л/мин. Критерии невключения: нарушения методики ингаляционного введения препарата Сурфактант-БЛ; инвазивная искусственная вентиляция легких (ИВЛ). Комплексную терапию и ингаляции препарата Сурфактант-БЛ в дозе 1 мг/кг 2–3 раза в сутки на протяжении 3–5 дней получали 28 пациентов основной группы. Только традиционную комплексную терапию получали 40 пациентов контрольной группы. Результаты. В группе пациентов, находившихся на лечении в инфекционном отделении (16 пациентов получали сурфактант, 20 — традиционную терапию), обнаружен значимо больший прирост SaO2 через сутки сурфактант-терапии, меньший риск перевода в отделение реанимации и интенсивной терапии (ОРИТ) (6,25 против 45 %, p = 0,011), тенденция к меньшей летальности (6,25 против 30 %, p = 0,084). В группе пациентов, находившихся на лечении в ОРИТ и получавших неинвазивную масочную ИВЛ или высокопоточную кислородотерапию (12 пациентов получали сурфактант, 20 — традиционную терапию), обнаружены: значимо больший прирост SaO2, значимо меньший риск перевода на ИВЛ (25 против 75 %, p = 0,008) и значимо меньшая летальность (25 против 75 %, p = 0,008). Заключение. Включение сурфактант-терапии в комплексное лечение тяжелой пневмонии, вызванной SARS-CoV-2, позволило улучшить оксигенацию, значимо сократить риск перевода на ИВЛ и снизить летальность. Для подтверждения эффективности методики требуется проведение многоцентровых рандомизированных контролируемых испытаний.
Ключевые слова
Об авторах
Баутин Андрей Евгеньевич, д.м.н., доцент, заведующий научно-исследовательской лабораторией анестезиологии и реаниматологии
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
Аптекарь Валерия Владимировна, клинический ординатор кафедры анестезиологии и реаниматологии
Лапшин Кирилл Борисович, заведующий отделением анестезиологии-реанимации с палатами реанимации и интенсивной терапии № 14
Семенов Андрей Петрович, заведующий кардиологическим отделением № 7
Минеева Евгения Викторовна, к.м.н., заведующая кардиологическим отделением № 6
Анохина Наталья Анатольевна, заведующая отделением ревматологии
Титова Инга Эдуардовна, врач-кардиолог отделения хирургического лечения пациентов онкологического профиля
Тян Наталья Афанасьевна, заведующая кардиологическим отделением Консультативно-диагностического центра
Загородникова Ксения Александровна, к.м.н., заведующая отделом клинической фармакологии
Лестьева Наталья Александровна, к.м.н., заведующая отделением анестезиологии-реанимации
Кашерининов Игорь Юрьевич, к.м.н., заведующий отделением реанимации и интенсивной терапии № 4
Список литературы
1. Wu C, Chen X, Cai Y, et al. Risk factors associated with acute respiratory distress syndrome and death in patients with coronavirus disease 2019 pneumonia in Wuhan, China. JAMA Intern Med. 2020; 180 (7): 934–943.
2. Suleyman G, Fadel RA, Malette KM, et al. Clinical characteristics and morbidity associated with coronavirus disease 2019 in a series of patients in Metropolitan Detroit. JAMA Netw Open. 2020; 3 (6): e2012270.
3. Chand S, Kapoor S, Orsi D, et al. COVID-19associated critical illness-report of the first 300 patients admitted to intensive care units at a New York City Medical Center. J Intensive Care Med. 2020; 35 (10): 963–970.
4. Zhang H, Zhou P, Wei Y, et al. Histopathologic changes and SARS-CoV-2 immunostaining in the lung of a patient with COVID-19. Ann Intern Med. 2020; 172 (9): 629–632.
5. Günther A, Siebert C, Schmidt R, et al. Surfactant alterations in severe pneumonia, acute respiratory distress syndrome, and cardiogenic lung edema. Am J Respir Crit Care Med. 1996; 153 (1): 176–184.
6. Numata M, Kandasamy P, Nagashima Y, et al. Phosphatidylglycerol suppresses influenza A virus infection. Am J Respir Cell Mol Biol. 2012; 46 (4): 479–487.
7. Fukushi M, Yamashita M, Miyoshi-Akiyama T, et al. Laninamivir octanoate and artificial surfactant combination therapy significantly increases survival of mice infected with lethal influenza H1N1 virus. PLoS One. 2012; 7 (8): e42419.
8. Busani S, Girardis M, Biagioni E, et al. Surfactant therapy and intravenous zanamivir in severe respiratory failure due to persistent influenza A/H1N1 2009 virus infection. Am J Respir Crit Care Med. 2010; 182 (10): 1334.
9. Kula R, Maca J, Sklienka P, et al. Exogenous surfactant as a component of complex non-ECMO therapy for ARDS caused by influenza A virus (2009 H1N1). Bratisl Lek Listy. 2011; 112 (4): 218–222.
10. Witczak A, Prystupa A, Kurys-Denis E, et al. Acute respiratory distress syndrome (ARDS) complicating influenza A/H1N1v infection — a clinical approach. Ann Agric Environ Med. 2013; 20 (4): 820–822.
11. Takano H. Pulmonary surfactant itself must be a strong defender against SARS-CoV-2. Med Hypotheses. 2020; 144: 110020.
12. Schousboe P, Wiese L, Heiring C, et al. Assessment of pulmonary surfactant in COVID-19 patients. Crit Care. 2020; 24 (1): 552.
13. Busani S, Dall’Ara L, Tonelli R, et al. Surfactant replacement might help recovery of low-compliance lung in severe COVID-19 pneumonia. Ther Adv Respir Dis. 2020; 14: 1753466620951043.
14. Баутин А.Е., Осовских В.В., Хубулава Г.Г. и др. Многоцентровые клинические испытания сурфактанта-BL для лечения респираторного дистресс-синдрома взрослых. Клинические исследования лекарственных средств в России. 2002; 2: 18–23.
15. Vlasenko A, Osovskikh V, Tarasenko M, et al. Efficiency of surfactant therapy for ALI/ARDS in homogenous nosologic groups of patients. Eur Respir J. 2005; 26 (SUPPL 49): 90.
16. Bautin A, Khubulava G, Kozlov I, et al. Surfactant therapy for patients with ARDS after cardiac surgery. J Liposome Res. 2006; 16: 265–272.
17. Алексеев А.М., Шупинский О.В., Храпов К.Н. Интенсивная терапия больных с тяжелым течением гриппа А(H1N1), осложненного пневмонией. Вестник анестезиологии и реаниматологии. 2009; 6 (6): 35–38.
18. Методические рекомендации по лечению гриппа А/Н1N1/2009 Общероссийской общественной организации «Федерация анестезиологов и реаниматологов». Вестник анестезиологии и реаниматологии. 2011; 8 (1): 41–47.
Для цитирования:
Баутин А.Е., Аптекарь В.В., Лапшин К.Б., Семенов А.П., Минеева Е.В., Анохина Н.А., Титова И.Э., Тян Н.А., Загородникова К.А., Лестьева Н.А., Кашерининов И.Ю. Экзогенный сурфактант в комплексном лечении тяжелой пневмонии, вызванной вирусом SARS-CoV-2. Трансляционная медицина. 2020;7(6):55-64. https://doi.org/10.18705/2311-4495-2020-7-6-55-64
For citation:
Bautin A.E., Aptekar V.V., Lapshin K.V., Semenov A.P., Mineeva E.V., Anokhina N.A., Titova I.E., Tyan N.A., Zagorodnikova K.A., Lesteva N.A., Kasherininov I.Yu. Exogenous surfactant in the treatment of severe pneumonia caused by the SARS-CoV-2 virus. Translational Medicine. 2020;7(6):55-64. (In Russ.) https://doi.org/10.18705/2311-4495-2020-7-6-55-64