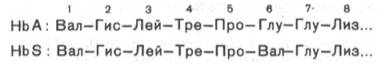Как называется простетическая группа гемопротеинов
Гемопротеины
К группе гемопротеинов относятся гемоглобин и его производные, миогло-бин, хлорофиллсодержащие белки и ферменты (вся цитохромная система, каталаза и пероксидаза). Все они содержат в качестве небелкового компонента структурно сходные железо- (или магний)порфирины, но различные по составу и структуре белки, обеспечивая тем самым разнообразие их биологических функций. Далее более подробно рассмотрено химическое строение гемоглобина, наиболее важного для жизнедеятельности человека и животных соединения.
Гемоглобин в качестве белкового компонента содержит глобин, а небелкового – гем. Видовые различия гемоглобина обусловлены глобином, в то время как гем одинаков у всех видов гемоглобина.
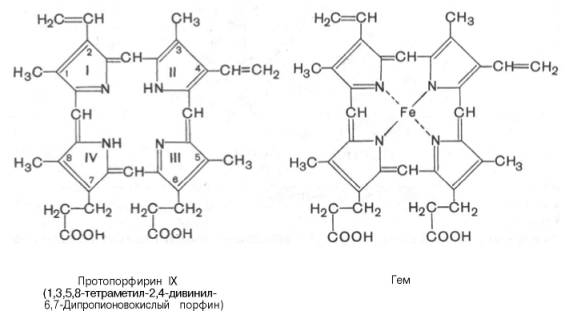
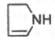
Основу структуры простетической группы большинства гемосодержащих белков составляет порфириновое кольцо, являющееся в свою очередь производным тетрапиррольного соединения – порфирина. Последний состоит из четырех замещенных пирролов:
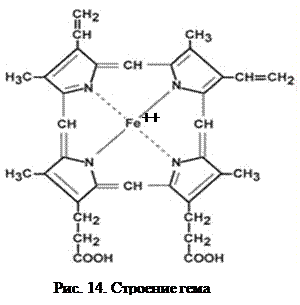
соединенных между собой метиновыми мостиками (—СН=). Незамещенный порфирин называется порфином. В молекуле гема порфин представлен в виде протопорфирина IX, содержащего четыре метильные группы (—СН3), две винильные группы (—СН=СН2) и два остатка пропионовой кислоты. Протопорфирин, присоединяя железо, превращается в гем.
Из формулы видно, что железо связано с двумя атомами азота молекулы протопорфирина ковалентно и с двумя другими – координационными связями, обозначенными пунктирными линиями. В зависимости от химической природы групп, находящихся в боковой цепи, порфирины классифицируют на этио-, мезо-, копро- и протопорфирины. Последние наиболее распространены в природе. Из возможных 15 изомеров протопорфиринов благодаря наличию трех разных заместителей самым распространенным оказался протопорфирин IX.
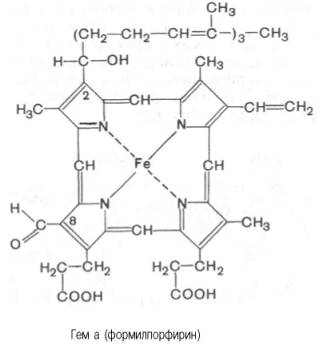
Гем в виде гем-порфирина является простетической группой не только гемоглобина и его производных, но и миоглобина, каталазы, пероксидазы и цитохромов b, с и c1 (см. главу 9); в то же время в цитохромах а и a3, входящих в состав интегрального комплекса, названного цитохромокси-дазой, содержится гем а, называемый также формилпорфирином:
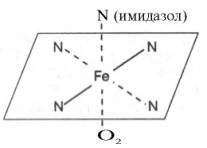
Гем а вместо метильной группы содержит формильный остаток (в 8-м положении) и вместо одной винильной группы (во 2-м положении) – изопре-ноидную цепь. Железо своими четырьмя связями образует комплекс с порфирином, а оставшиеся 5-я и 6-я координационные связи железа в молекулах гемоглобина и цитохромов связываются с белковыми компонентами по-разному. В частности, в гемоглобинах (и миоглобине) благодаря 5-й координационной связи железо соединяется с атомом азота имидазольной группы гистидина белковой молекулы. Шестая координационная связь железа предназначена для присоединения кислорода (с образованием оксигемоглобина и оксимиоглобина) или других лигандов: СО, цианидов и др. (рис. 2.1). В цитохромах, напротив, и 5-я, и 6-я координационные связи железа соединены с остатками гистидина и метио-нина (в цитохроме с обе винильные группы соединены еще и с остатками цистеина) белковой молекулы. Этим, вероятнее всего, могут быть объяснены функции железа в гемоглобине, валентность которого не изменяется при присоединении кислорода (в отличие от валентности железа в цитохромах): в гемоглобине железо остается двухвалентным независимо от присоединения или отдачи кислорода.
Структурная организация гемоглобина (и миоглобина) была описана в главе 1. Дж. Кендрью и М. Перутц расшифровали конформацию этих молекул (Нобелевская премия 1962 г.). Дыхательная функция гемоглобина крови подробно рассматривается в курсе физиологии. Здесь следует указать на уникальную роль гемоглобина в траспорте кислорода от легких к тканям и диоксида углерода от тканей к легким. Это элементарное проявление жизни – дыхание, хотя и выглядит простым, основано на взаимодействии многих типов атомов в гигантской молекуле гемоглобина. Подсчитано, что в одном эритроците содержится около 340000000 молекул гемоглобина, каждая из которых состоит примерно из 10 3 атомов С, Н, О, N, S и 4 атомов железа.
Атом железа расположен в центре гема-пигмента, придающего крови характерный красный цвет. Каждая из 4 молекул гема «обернута» одной полипептидной цепью. В молекуле гемоглобина взрослого человека HbА (от англ. adult – взрослый) содержатся четыре полипептидные цепи, которые вместе составляют белковую часть молекулы – глобин. Две из них, называемые α-цепями, имеют одинаковую первичную структуру и по 141 аминокислотному остатку. Две другие, обозначаемые β-цепями, также идентично построены и содержат по 146 аминокислотных остатков. Таким образом, вся молекула белковой части гемоглобина состоит из 574 аминокислот. Во многих положениях α- и β-цепи содержат разные аминокислотные последовательности, хотя и имеют почти одинаковые пространственные структуры. Получены доказательства, что в структуре гемоглобинов более 20 видов животных 9 аминокислот в последовательности оказались одинаковыми, консервативными (инвариантными), определяющими функции гемоглобинов; некоторые из них находятся вблизи гема, в составе участка связывания с кислородом, другие – в составе неполярной внутренней структуры глобулы.
Рис. 2.1. Координационные связи атома железа в молекуле гема. Все 4 связи с атомами азота пиррольных колец расположены в одной плоскости, 5-я и 6-я координационные связи (с атомом азота имидазольного кольца гистидина и с кислородом соответственно) – по разные стороны перпендикулярно к этой плоскости.
В дополнение к основному гемоглобину HbA1в крови взрослого человека доказано существование мигрирующего с меньшей скоростью при электрофорезе гемоглобина НbА2, также состоящего из 4 субъединиц: двух α-цепей и двух δ-цепей. На долю НbА2 приходится около 2,5% от всего гемоглобина. Известен, кроме того, фетальный гемоглобин (гемоглобин новорожденных), обозначаемый HbF и состоящий из двух α-цепей и двух γ-цепей. Фетальный гемоглобин отличается от HbA1не только составом аминокислот, но и физико-химическими свойствами: спектральным показателем, электрофоретической подвижностью, устойчивостью к щелочной денатурации и др. Кровь новорожденного содержит до 80% HbF, но к концу 1-го года жизни он почти целиком заменяется на НbА (все же в крови взрослого человека открывается до 1,5% HbF от общего количества гемоглобина). Последовательность аминокислот в γ- и δ-цепях гемогло-бинов окончательно не расшифрована.
Установление первичной структуры субъединиц молекулы гемоглобина стимулировало исследования по расшифровке структуры так называемых аномальных гемоглобинов. В крови человека в общей сложности открыто около 150 различных типов мутантных гемоглобинов. Появляются мутантные формы гемоглобинов в крови вследствие мутации генов. Обычно мутации делят на 3 класса в соответствии с топографией измененного участка молекулы. Если замена аминокислоты происходит на поверхности молекулы гемоглобина, то это мутация первого класса; подобные мутации обычно не сопровождаются развитием тяжелой патологии, и болезнь протекает бессимптомно; исключение составляет серповидно-клеточная анемия. При замене аминокислоты вблизи гема нарушается связывание кислорода – это мутация второго класса, сопровождающаяся развитием болезни. И наконец, если замена происходит во внутреннем участке молекулы гемоглобина, говорят о третьем классе мутации; подобные мутации приводят к нарушению пространственной структуры и соответственно функции гемоглобина.
Аномальные гемоглобины, различающиеся по форме, химическому составу и величине заряда, были выделены при помощи электрофореза и хроматографии. Передающиеся по наследству изменения чаще всего являются результатом мутации единственного триплета, приводящей к замене одной какой-либо аминокислоты в полипептидных цепях молекулы гемоглобина на другую. В большинстве случаев происходит замена кислой аминокислоты на основную или нейтральную (табл. 2.1). Поскольку это замещение осуществляется в обеих полипептидных цепях одной из пар (α или β), образовавшийся аномальный гемоглобин будет отличаться от нормального величиной заряда и соответственно электрофоретической подвижностью.
В табл. 2.1 представлены некоторые типы аномальных гемоглобинов, составы их полипептидных цепей с указанием известной или вероятной локализации замены либо в α-, либо в β-цепях. Замены необычной аминокислотой в аномальных гемоглобинах имеют место как в α-, так и в β-цепях. Исключение составляет гемоглобин Н, все 4 полипептида которого представлены β-цепями, идентичными по структуре β-цепям нормального гемоглобина A1.
Следует указать, что некоторые мутации, вызывающие существенное изменение структуры и соответственно функции гемоглобина, оказываются летальными, и индивидуумы с подобным гемоглобином умирают в раннем возрасте. Однако при ряде мутаций замена аминокислот не вызывает заметного изменения функции гемоглобина, в этих случаях болезнь протекает бессимптомно.
Болезни гемоглобинов (их насчитывают более 200) называют гемогло-бинозами. Принято делить их на гемоглобинопатии, в основе развития которых лежит наследственное изменение структуры какой-либо цепи нормального гемоглобина (часто их относят также к «молекулярным болезням»), и талассемии, обусловленные наследственным нарушением синтеза какой-либо нормальной цепи гемоглобина. Различают также же-лезодефицитные анемии.
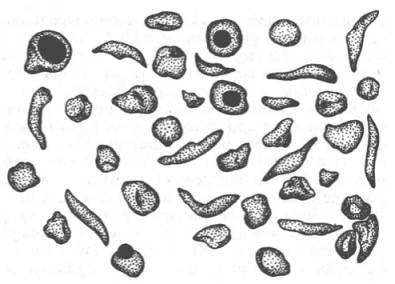
Рис. 2.2. Нормальные и серповидные эритроциты.
Классическим примером наследственной гемоглобинопатии является серповидно-клеточная анемия, широко распространенная в странах Южной Америки, Африки и Юго-Восточной Азии. При этой патологии эритроциты в условиях низкого парциального давления кислорода принимают форму серпа (рис. 2.2). Гемоглобин S, как показали Л. Полинг и др., отличается рядом свойств от нормального гемоглобина: в частности, после отдачи кислорода в тканях он превращается в плохо растворимую дез-окси-форму и начинает выпадать в осадок в виде веретенообразных кристаллоидов, названных тактоидами. Последние деформируют клетку и приводят к массивному гемолизу. Болезнь протекает остро, и дети, гомозиготные по мутантному гену, часто умирают в раннем возрасте.
Химический дефект при серповидно-клеточной анемии был раскрыт В. Ингремом и сводится к замене единственной аминокислоты, а именно глутаминовой, в 6-м положении с N-конца на валин в β-цепях молекулы гемоглобина HbS (см. табл. 2.1, рис. 2.2). Это результат мутации в молекуле ДНК, кодирующей синтез β-цепи гемоглобина. Все остальные аминокислоты располагаются в той же последовательности и в таком же количестве, как и в нормальном гемоглобине НbА:
Одной этой замены оказалось достаточно не только для нарушения формы эритроцита, но и для развития тяжелой наследственной болезни – серповидно-клеточной анемии.
Талассемии, строго говоря, не являются гемоглобинопатиями. Это генетически обусловленное нарушение синтеза одной из нормальных цепей гемоглобина. Если угнетается синтез β-цепей, то развивается β-талассемия; при генетическом дефекте синтеза α-цепей развивается α-талас-семия. При β-талассемии в крови наряду с HbA1появляется до 15% НbА2 и резко повышается содержание HbF – до 15–60%. Болезнь характеризуется гиперплазией и разрушением костного мозга, поражением печени, селезенки, деформацией черепа и сопровождается тяжелой гемолитической анемией. Эритроциты при талассемии приобретают мишеневидную форму. Механизм изменения формы эритроцитов объяснить пока не удалось.
В медицинской практике часто проводят анализ кровяных пигментов, который основан на исследовании спектроскопических свойств гема гемоглобина, точнее продуктов его окисления (хлорида гемина и гематина, образующихся соответственно при обработке гемоглобина уксусной кислотой в присутствии хлорида натрия или разведенными растворами щелочей). При восстановлении гематина сульфитом аммония в присутствии глобина образуется производное гемоглобина – гемохромоген, в котором денатурированный глобин соединен с гемом. Полученный комплекс имеет характерный спектр поглощения. Этот метод широко применяется в судебно-медицинской практике при исследовании кровяных пятен.
Следует отметить, что самым надежным методом качественного определения различных производных гемоглобина является исследование их спектров поглощения.
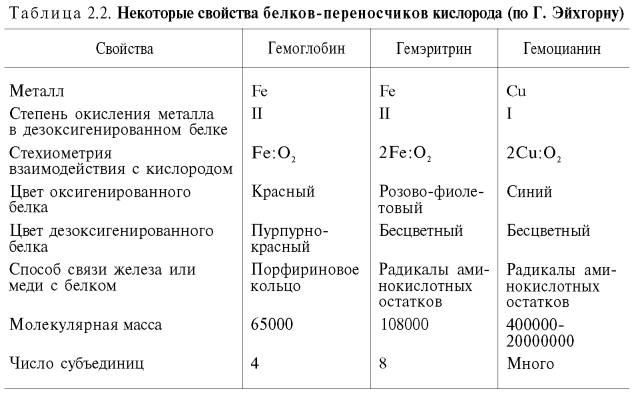
У беспозвоночных роль переносчика кислорода часто выполняют пигменты негеминовой природы – гемэритрин и гемоцианин. Они не относятся к гемсодержащим хромопротеинам, хотя в их названиях содержится корень «гем». Эти белки, как и гемоглобин, несмотря на то что выполняют одну и ту же функцию, сильно различаются между собой по молекулярной массе и четвертичной структуре, химической природе активного центра, характеру связывания железа (гемэритрин) и меди (гемоцианин) с кислородом и др. (табл. 2.2).
Трансферрины (сидерофилины) – группа сложных белков, полученных из разных источников и характеризующихся способностью специфично, прочно и обратимо связывать ионы железа Fe (III) и других переходных металлов. Наиболее подробно из этой группы белков изучен трансферрин сыворотки крови. Функция трансферрина заключается в транспорте ионов железа в ретикулоциты, в которых осуществляется биосинтез гемоглобина. Система трансферрин–ретикулоцит считается весьма перспективной для изучения взаимодействия металла с белком и белковой молекулы с клеткой.
Сложные белки



Это структуры, содержащие белковую часть – апопротеин и небелковый компонент – простетическую группу. В зависимости от строения последней принято различать следующие их варианты.
Фосфопротеины – это сложные белки, простетической группой которых является остаток фосфорной кислоты. Тип связи между апопротеином и небелковым компонентом – сложноэфирная, которая образуется при взаимодействии ОН-группы серина или треонина с фосфорной кислотой. К протеинам этого класса относятся казеиноген молока, фосфорилированные модификации гистонов, ферменты (РНК-полимеразы, некоторые фосфотрансферазы, фосфатазы) и другие, а также вителлин, фосвитин желтка и овальбумин белка яиц, ихтуллин икры рыб.
Остатки фосфорной кислоты, включённые в белки, находятся в диссоциированом состоянии, что придаёт молекуле сильный отрицательный заряд. Поэтому фосфопротеины могут легко взаимодействовать с лигандами или отталкивать их. Так, например, они связывают ионы Са 2+ и транспортируют их.
Но главная особенность данной простетической группы – это возможность изменения конформации и заряда белковой молекулы, что сказывается на её свойствах и функциях. Реакция взаимодействия с фосфорной кислотой называется фосфорилирование или дефосфорилирование и используется, например, для регулирования активности ферментов и изменения функциональной активности биомембран (проницаемости и др.).
Фосфопротеины необходимы для развития зародыша, плода, новорожденного, т.к. содержат оптимальный набор аминокислот, а фосфорная кислота используется для формирования скелета (связывание ионов Са 2+ ), для образования макроэргов – АТФ, АДФ и др., которые требуются в качестве источников энергии в реакциях синтеза, особенно интенсивно протекающих в растущем организме.
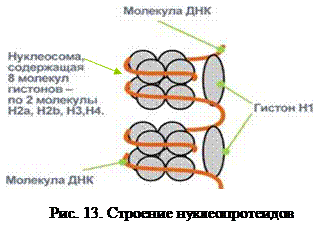
Нуклеопротеины – сложные белки, простетической группой которых являются нуклеотиды, и в первую очередь нуклеиновые кислоты – ДНК и РНК. В качестве апопротеина выступают белки гистоны, реже протамины. Так как эти протеины положительно заряжены, а нуклеиновые кислоты – отрицательно, то связь, образуемая между ними, ионная. Множество октамеров гистонов, комплексируясь с полинуклеотидом, образует нуклеосомы, которые затем компактно укладываются в органоидах (рис. 13).
В функциональном отношении они отвечают за хранение и передачу наследственной информации и процессы биосинтеза белка.
Хромопротеины («цветные белки») своей окраской обязаны простетической группе – пигменту. В зависимости от строения различают следующие подклассы: гемопротеины, флавопротеины, родопсин.

Миоглобин – небольшой глобулярный белок (Mr 16500 Да); молекула его состоит из одной полипептидной цепи (153 а/к) и одного гема. Сродство к кислороду у данного гемопротеида значительно больше, чем у гемоглобина, поэтому он может принимать газ от последнего для сохранения или использования его в мышечных клетках.
Гем b является также структурной единицей ферментов каталазы и пероксидазы, обезвреживающих пероксиды, и цитохромов – митохондриальных белков, участвующих в переносе электронов от окисляемых веществ в конечном итоге на кислород за счёт своей способности изменять валентность железа.
Гем а встречается в растительных гемопротеинах и участвует в процессе фотосинтеза.
Металлопротеины – сложные белки, где роль небелкового компонента выполняют катионы металлов. Связь между ними ионная или координационная (донорно-акцепторная). Типичными представителями таких белков являются железосодержащие белки.
Ферритин. В его составе ионы Fe 3+ депонируются в клетках селезёнки, костного мозга, но богаче всего этим белком печень. Там может накапливаться до 700 мг железа, которое используется по мере надобности для синтеза гема. Гемосидерин – это комплекс гликопротеина и ионов железа, образуется в тканях при кумулировании избытка железа. Трансферрин – растворимый в воде железопротеин, содержащий ещё олигосахариды (металлогликопротеин). Этот белок вырабатывается гепатоцитами и секретируется в кровь, где служит для транспорта катионов этого металла к клеткам других органов. Молекула трансферрина удерживает два иона железа, которые захватывает в кишечнике или местах распада гема, и осуществляет их перенос к точкам депонирования и утилизации. Церулоплазминаналогично трансферрину обеспечивает транспорт катионов металла, только восьми ионов меди.
Гликопротеины,или гликоконъюгаты. В них простетическая группа представлена углеводными компонентами и связана с белком О-гликозидными (реже N-гликозидными) связями. Небелковый фрагмент некоторых гликопротеидов редко бывает представлен одним моносахаридом; как правило, это олиго- или полисахаридные разветвлённые цепочки. Причём на долю углеводов может приходиться от 1 до 85%.
Исходя из вклада в общую копилку, выделяют два подкласса белков, содержащих углеводы: протеогликаныи гликопротеины. Между ними имеются существенные отличия: